解题方法
1 . 如图为元素周期表的一部分,请按要求填空:

(1)表中元素①形成单质的化学式为______ ;
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的______ 相同;
(3)表中11号和9号元素组成的化合物的化学式为______ ;
(4)表中不同种元素最本质的区别是______ 。

(1)表中元素①形成单质的化学式为
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的
(3)表中11号和9号元素组成的化合物的化学式为
(4)表中不同种元素最本质的区别是
您最近一年使用:0次
解题方法
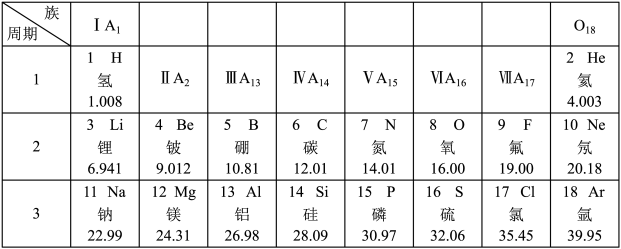
2 . 元素周期表是学习和研究化学的重要工具。下图是元素周期表部分内容,请分析表中信息回答相关问题。___________ ,它属于___________ (填“金属”或“非金属”)元素,在化学反应中容易___________ (填“得到”或“失去”)电子。
(2)不同种元素最本质的区别是___________ ;
(3)在同一族中,各元素的原子最外层电子数___________ (He除外),原子序数为3的元素与第三周期中的___________ (填名称)元素具有相似的化学性质。
(2)不同种元素最本质的区别是
(3)在同一族中,各元素的原子最外层电子数
您最近一年使用:0次
解题方法
3 . 元素周期表是学习和研究化学的重要工具。请分析下图中的信息并回答下列问题。

(1)9 号元素的元素名称为_______ ,易_______ (填“得到”或“失去”)电子。
(2)不同种元素最本质的区别是_______ 不同。
(3)在元素周期表中,同一族(行)的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是______(填字母)。
(4)在元素周期表中,同一周期(横行)中的元素,除 0 族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。则钠和镁的原子半径以及失电子能力关系是:镁原子半径比钠的小,在化学反应中镁原子失电子能力比钠_______ 。(填“强”或“弱”)

(1)9 号元素的元素名称为
(2)不同种元素最本质的区别是
(3)在元素周期表中,同一族(行)的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是______(填字母)。
| A.Ar 和 Ne | B.F 和 Cl | C.Be 和 Mg | D.H 和 Na |
(4)在元素周期表中,同一周期(横行)中的元素,除 0 族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。则钠和镁的原子半径以及失电子能力关系是:镁原子半径比钠的小,在化学反应中镁原子失电子能力比钠
您最近一年使用:0次
2024九年级下·全国·专题练习
解题方法
4 . 如图是元素周期表中第2、3周期的元素,请回答有关问题。
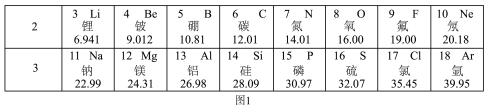
(1)下列各组具有相似化学性质的元素是______(填字母序号);
(2)写出一条第三周期元素原子的核外电子排布规律______ ;
(3)第7号元素与第12号元素的原子形成化合物的化学式为______ ;15号元素的相对原子质量为______ ;
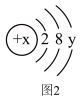
(4)某离子的结构示意图如图2所示,当x﹣y=8时,该粒子的符号为______ ;
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是______(填字母序号)。


(1)下列各组具有相似化学性质的元素是______(填字母序号);
| A.Na、Cl | B.O、S | C.F、Cl | D.Cl、Ar |
(2)写出一条第三周期元素原子的核外电子排布规律
(3)第7号元素与第12号元素的原子形成化合物的化学式为
(4)某离子的结构示意图如图2所示,当x﹣y=8时,该粒子的符号为
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是______(填字母序号)。
| A.NO和O2 | B.CO和N2 |
| C.SO2和CO2 | D. 和 和 |
您最近一年使用:0次
解题方法
5 . 元素周期表是学习化学的重要工具,如图为元素周期表中部分元素的相关信息,利用如图回答相关问题。

(1)原子序数为4的元素符号为_________ 。
(2)C、N、O排在同周期是因为_______ (选填“质子数”“电子层数”或“最外层电数”)相同。
(3)He和Mg的化学性质_______ (选填“相似”或“不相似”)。

(1)原子序数为4的元素符号为
(2)C、N、O排在同周期是因为
(3)He和Mg的化学性质
您最近一年使用:0次
名校
解题方法
6 . 目前,元素周期表的第七周期已被填满。2017年,科学家发现的第113号、115号、117号和118号元素有了中文名称。已知第113号元素与Al元素同主族,根据元素周期律知识,下列预测或说法中合理的是


| A.Nh的最高价氧化物对应的水化物可能具有两性 |
| B.Mc在元素周期表中的位置是第七周期第ⅤB族 |
| C.Ts的同位素原子具有相同的电子数 |
| D.Og在元素周期表的所有元素中非金属性最强 |
您最近一年使用:0次
解题方法
7 . 元素周期表是化学学习和研究的重要工具如图是元素周期表的一部分。

(1)相对原子质量为10.81的元素属___________ 元素(填“金属”或“非金属”)。
(2)科学家宣布,现已人工合成了第135号元素,则此元素的质子数为___________ 。
(3)请标出HClO中氯元素的化合价___________ 。
(4)地壳中含量前两位的非金属元素组成的化合物是___________ (填化学式),含量最多的金属与非金属元素组成的化合物是___________ (填化学式)。

(1)相对原子质量为10.81的元素属
(2)科学家宣布,现已人工合成了第135号元素,则此元素的质子数为
(3)请标出HClO中氯元素的化合价
(4)地壳中含量前两位的非金属元素组成的化合物是
您最近一年使用:0次
名校
解题方法
8 . 部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是


| A.离子半径的大小顺序:e>f>g>h |
| B.与a形成简单化合物的稳定性:b>c>d |
| C.a、c、d元素形成的化合物可能含有离子键 |
D.用电子式表示e和h形成化合物的过程: |
您最近一年使用:0次
解题方法
9 . 分析下列各组微粒结构示意图,下列说法正确的是
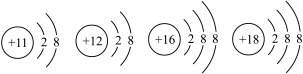
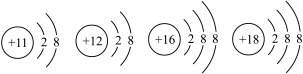
| A.都属于金属元素 | B.都属于阳离子 |
| C.都属于同种元素 | D.在周期表中是同一周期 |
您最近一年使用:0次
解题方法
10 . 5G时代来临,氮化镓是生产芯片的核心材料。图为氮和镓(Ga)的原子结构示意图。下列推断正确的是
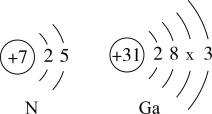
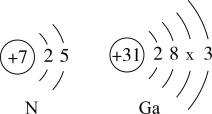
| A.氮元素位于第三周期 | B.图中x=20 |
| C.镓的原子序数为31 | D.N和Ga可形成化合物Ga5N2 |
您最近一年使用:0次



