取一定量的氧化铜与氧化锌的混合物,加入100g质量分数为19.6%的稀硫酸,恰好完全反应。原固体混合物中氧元素的质量为______ ;氧化铜和稀硫酸反应的化学方程式为______ 。
更新时间:2021-05-08 09:10:59
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属具有广泛的应用。
(1)下列金属制品中,利用金属导热性的是_______ (填字母)
A金属硬币 B 铝制导线 C 铜制火锅
(2)将一定量的锌粉加入到硫酸亚铁、硫酸铜的混合溶液中,一段时间后过滤,向滤渣中加入稀盐酸,观察到有气泡产生,则滤液中一定含有的阳离子有_______ 。
(3)将5.0g黄铜(铜锌合金)样品粉末投入到20.0g 稀硫酸的烧杯中,恰好完全反应。称得未溶物质量为3.7g。完成下列计算:
①所用稀硫酸中溶质的质量分数_______ 。
②反应后所得溶液中溶质质量分数_______ (结果保留一位小数)。
(1)下列金属制品中,利用金属导热性的是
A金属硬币 B 铝制导线 C 铜制火锅
(2)将一定量的锌粉加入到硫酸亚铁、硫酸铜的混合溶液中,一段时间后过滤,向滤渣中加入稀盐酸,观察到有气泡产生,则滤液中一定含有的阳离子有
(3)将5.0g黄铜(铜锌合金)样品粉末投入到20.0g 稀硫酸的烧杯中,恰好完全反应。称得未溶物质量为3.7g。完成下列计算:
①所用稀硫酸中溶质的质量分数
②反应后所得溶液中溶质质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属在生产、生活中广泛应用。
(1)将纯铜片和黄铜(铜锌合金)片相互刻画,纯铜片上有划痕说明合金硬度一般______ (填“大于”或“小于”)它的组成金属。
(2)向硫酸铜、硫酸亚铁的混合溶液中加入一定量镁粉,充分反应后过滤,得到滤渣和滤液。若滤液呈无色,则滤渣中一定含有的金属是______ 。
(3)利用“活泼金属”可以制得H2,H2可以作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有______(填字母序号)。
(4)取铁粉与铜粉的均匀混合物10g与100g稀硫酸恰好完全反应,反应后过滤得到干燥固体的质量为2g,则稀硫酸的溶质质量分数为______ 。
(1)将纯铜片和黄铜(铜锌合金)片相互刻画,纯铜片上有划痕说明合金硬度一般
(2)向硫酸铜、硫酸亚铁的混合溶液中加入一定量镁粉,充分反应后过滤,得到滤渣和滤液。若滤液呈无色,则滤渣中一定含有的金属是
(3)利用“活泼金属”可以制得H2,H2可以作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有______(填字母序号)。
| A.金属原料的成本 | B.生成过程中的能源和污染 | C.金属的回收利用 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】铁是在____ 条件下最易生锈,将一枚锈铁钉放入足量的稀硫酸中,依次 观察到的现象___ .有关化学方程式为____ .
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
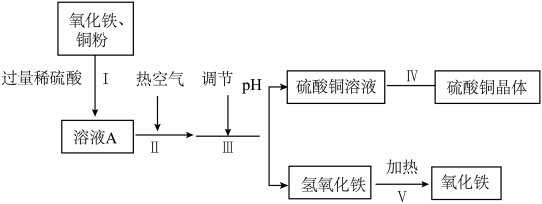
【推荐2】工业上生产硫酸铜的过程如图所示。
已知: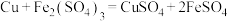
(1)步骤Ⅳ中的操作是蒸发浓缩、___________ 、过滤。
(2)溶液A中一定含有的阳离子有___________ 。
(3)该过程中能够循环利用的物质是___________ (填化学式)
(4)已知步骤V中氢氧化铁加热后生成两种氧化物,写出该反应的化学方程式:___________ 。

已知:
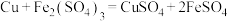
(1)步骤Ⅳ中的操作是蒸发浓缩、
(2)溶液A中一定含有的阳离子有
(3)该过程中能够循环利用的物质是
(4)已知步骤V中氢氧化铁加热后生成两种氧化物,写出该反应的化学方程式:
您最近一年使用:0次




