如图是甲、乙、丙三种固体物质溶解度曲线图,请回答。

(1)t2℃时,甲、乙、丙三种物质的溶解度大小关系是______ 。
(2)将丙的饱和溶液变为不饱和溶液的一种方法是______ 。
(3)t1℃时,将30g甲物质放入50g水中充分溶解,所得溶液中溶质和溶液的质量比为______ (填最简整数比)。
(4)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t2℃,所得溶液中溶质质量分数的大小关系是______ 。

(1)t2℃时,甲、乙、丙三种物质的溶解度大小关系是
(2)将丙的饱和溶液变为不饱和溶液的一种方法是
(3)t1℃时,将30g甲物质放入50g水中充分溶解,所得溶液中溶质和溶液的质量比为
(4)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t2℃,所得溶液中溶质质量分数的大小关系是
更新时间:2021-05-17 22:47:23
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐1】下表是硝酸钾、氯化钠在不同温度时的溶解度。
回答下列问题:
(1)10 ℃时,NaCl 的溶解度是________ g。
(2)由上表可知,________ (填“KNO3”或“NaCl”)的溶解度受温度变化的影响较大。
(3)20 ℃时,先加入7.5 g NaCl,再加入67.5 g水,搅拌至完全溶解,得到的NaCl溶液中溶质的质量分数为________ 。
(4)30 ℃时,为了验证KNO3不能无限溶解:向烧杯中加入100 g水,然后加入15.8 g KNO3,须再加入KNO3的质量为________________ 。
溶解度/g 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)10 ℃时,NaCl 的溶解度是
(2)由上表可知,
(3)20 ℃时,先加入7.5 g NaCl,再加入67.5 g水,搅拌至完全溶解,得到的NaCl溶液中溶质的质量分数为
(4)30 ℃时,为了验证KNO3不能无限溶解:向烧杯中加入100 g水,然后加入15.8 g KNO3,须再加入KNO3的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】下表是NaCl和KNO3物质在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
(1)20℃时,NaCl的溶解度是_____ g/100g水;
(2)以上两种物质溶解度变化受温度影响较小的是_____ (选填“NaCl”或“KNO3”);
(3)20℃时,将20gNaCl固体加入50g水中,充分搅拌,形成的溶液质量为_____ g;
(4)为了将混有少量NaCl杂质的KNO3的饱和溶液提纯,可通过_____ 方法获得较纯净的KNO3晶体;
(5)40℃时,将NaCl和KNO3的饱和溶液各100g降温到20℃,对剩余溶液描述正确的是_____ 。
A 溶质的质量分数:NaCl<KNO3
B 析出固体的质量:NaCl>KNO3
C NaCl和KNO3都是饱和溶液
D 溶剂的质量:NaCl>KNO3
| 温度(℃) | 10 | 20 | 30 | 40 | 60 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 110 |
(2)以上两种物质溶解度变化受温度影响较小的是
(3)20℃时,将20gNaCl固体加入50g水中,充分搅拌,形成的溶液质量为
(4)为了将混有少量NaCl杂质的KNO3的饱和溶液提纯,可通过
(5)40℃时,将NaCl和KNO3的饱和溶液各100g降温到20℃,对剩余溶液描述正确的是
A 溶质的质量分数:NaCl<KNO3
B 析出固体的质量:NaCl>KNO3
C NaCl和KNO3都是饱和溶液
D 溶剂的质量:NaCl>KNO3
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】下图是A、B、C三种物质的溶解度曲线,据图回答:

(1)P点的含义是:______ 。
(2)溶解度随温度升高而减少的物质是______ 。写出两种使C的不饱和溶液转化为饱和溶液的方法:______ 。
(3)t2°C时,三种物质的溶解度由大到小的顺序是:______ 。
(4)t2°C时,A的饱和溶液中溶质的质量分数______ C的饱和溶液中溶质的质量分数(填“>”“<”或“=”)。将t2°C时A、C两种物质恰好饱和的溶液降温到t1 °C所得溶液溶质质量分数的关系是A______ C (填 “>”“<”或“=”)
(5)t2°C时,将30gB物质加入50g水中,经充分溶解所形成的溶液质量为______ g。
(6)B的浓溶液中混有少量的C,提纯B的最佳方法是______ 。若从C的浓溶液中得到C的晶体,最好采用的方法是______ 。

(1)P点的含义是:
(2)溶解度随温度升高而减少的物质是
(3)t2°C时,三种物质的溶解度由大到小的顺序是:
(4)t2°C时,A的饱和溶液中溶质的质量分数
(5)t2°C时,将30gB物质加入50g水中,经充分溶解所形成的溶液质量为
(6)B的浓溶液中混有少量的C,提纯B的最佳方法是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】如图所示,是A、B、C三种固体物质的溶解度曲线,请据图回答下列问题:
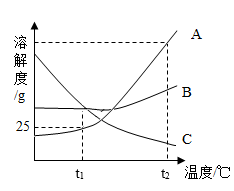
(1)t1℃时,A物质饱和溶液的溶质质量分数为___________ 。
(2)t2℃时,A 、B、C三种物质的溶解度最大的是___________ 。
(3)要从B物质的饱和溶液中得到B物质的晶体,一般采用___________ 的方法,这是因为___________ 。
(4)将t1℃时C物质的不饱和溶液,可以通过减少溶剂、增加溶质或___________ ,可使其变为饱和溶液。
(5)从t2℃降低到t1℃时,等质量的A 、B、C三种物质的饱和溶液,析出晶体最多的是___________ 物质。

(1)t1℃时,A物质饱和溶液的溶质质量分数为
(2)t2℃时,A 、B、C三种物质的溶解度最大的是
(3)要从B物质的饱和溶液中得到B物质的晶体,一般采用
(4)将t1℃时C物质的不饱和溶液,可以通过减少溶剂、增加溶质或
(5)从t2℃降低到t1℃时,等质量的A 、B、C三种物质的饱和溶液,析出晶体最多的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】a、b、c三种物质在水中的溶解度曲线如图。

(1)P点的含义是_____ ;
(2)t1℃时,20g水中最多溶解c物质_____ g;
(3)将t2℃时a、b、c三种物质的饱和溶液降低温度到t1℃时,这三种溶液中溶质质量分数的大小关系是_____ 。

(1)P点的含义是
(2)t1℃时,20g水中最多溶解c物质
(3)将t2℃时a、b、c三种物质的饱和溶液降低温度到t1℃时,这三种溶液中溶质质量分数的大小关系是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】下图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题。
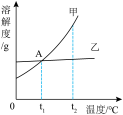
(1)A点的含义是_____________________________________ 。
(2)当甲中含有少量乙时,可采用__________________ 的方法提纯甲。
(3)小明说“t2℃时甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数”,请判断该说法是否正确(填“正确”或“不正确)__________ , 其理由是_____________________________ 。
(4)t1℃时,100g水中溶解20g甲时溶液刚好达到饱和; 那么在t1℃时,向50g水中溶解_____ g乙,溶液可以达到饱和。
(5)硫酸钠在不同温度下的溶解度如下表所示:
试计算40℃时,硫酸钠饱和溶液的溶质质量分数是_______________ 。

(1)A点的含义是
(2)当甲中含有少量乙时,可采用
(3)小明说“t2℃时甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数”,请判断该说法是否正确(填“正确”或“不正确)
(4)t1℃时,100g水中溶解20g甲时溶液刚好达到饱和; 那么在t1℃时,向50g水中溶解
(5)硫酸钠在不同温度下的溶解度如下表所示:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| 硫酸钠溶解度/g | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐1】NaOH、Na2CO3、NaCl在不同溶剂中的溶解度如下表所示。
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
表2 常温下,NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(S/g)
根据表1和表2提供的数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高而 (填“增大”或“减小”)
(2)20℃时,饱和食盐水中溶质的质量分数为 (计算结果精确到0.1﹪);
(3)为证明CO2能与NaOH发生反应,小明同学将CO2通入饱和NaOH的乙醇溶液中。请推测该实验可观察到的现象 ,推测依据是 。
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
| t/℃ | NaOH | Na2CO3 | NaCl |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
| NaOH | Na2CO3 | NaCl |
| 17.3 | <0.01 | 0.1 |
(1)NaOH在水中的溶解度随温度升高而 (填“增大”或“减小”)
(2)20℃时,饱和食盐水中溶质的质量分数为 (计算结果精确到0.1﹪);
(3)为证明CO2能与NaOH发生反应,小明同学将CO2通入饱和NaOH的乙醇溶液中。请推测该实验可观察到的现象 ,推测依据是 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】下图是甲、乙两种固体物质的溶解度曲线。据图回答:
(1)10℃时,甲物质的溶解度_______ 乙物质的溶解度(填“>”或“=”或“<”)。

(2)甲中混有少量的乙,提纯甲可以采用_______ 的方法。
(3)20℃时将20g的甲物质放入50g水中,充分搅拌后,有剩余溶质没有溶解,一段时间后固体消失。请你分析原因是_______ 。
(4)将 30℃时甲、乙两物质饱和溶液各100g分别蒸发10g水后, 降低温度到10℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法中正确的是_______ 。
A都是饱和溶液B溶液质量 a<b
C溶质质量 a=b D溶剂质量 a<b E.溶质质量分数 a=b
(1)10℃时,甲物质的溶解度

(2)甲中混有少量的乙,提纯甲可以采用
(3)20℃时将20g的甲物质放入50g水中,充分搅拌后,有剩余溶质没有溶解,一段时间后固体消失。请你分析原因是
(4)将 30℃时甲、乙两物质饱和溶液各100g分别蒸发10g水后, 降低温度到10℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法中正确的是
A都是饱和溶液B溶液质量 a<b
C溶质质量 a=b D溶剂质量 a<b E.溶质质量分数 a=b
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
名校
【推荐1】甲、乙、丙三种物质的溶解度曲线如图所示。
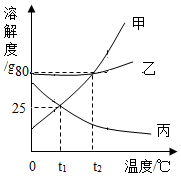
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小顺序为______ ;
(2)t2℃时,乙物质的溶解度为______ g
(3)将t2℃时180g甲的饱和溶液降温到t1℃,析出晶体的质量为______ g,所得甲溶液溶质质量分数为______ 。
(4)取等质量的甲、乙、丙三种物质,分别配制成t2℃时的恰好饱和溶液,所得三种溶液的质量由大到小顺序为______ 。

(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小顺序为
(2)t2℃时,乙物质的溶解度为
(3)将t2℃时180g甲的饱和溶液降温到t1℃,析出晶体的质量为
(4)取等质量的甲、乙、丙三种物质,分别配制成t2℃时的恰好饱和溶液,所得三种溶液的质量由大到小顺序为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】如图是A、B、C三种固体物质的溶解度曲线。

(1)点P表示______ 。
(2)t3℃时,三种物质的饱和溶液的溶质质量分数由小到大为______ 。
(3)将t3℃的A物质的饱和溶液75g降温到t1℃,析出A物质______ g(不含结晶水)。
(4)为除去A中混有的少量B,宜采用______ (填“蒸发结晶”或“降温结晶”)法。
(5)t3℃时,取A、B两物质的等质量饱和溶液分别蒸发等量的水后,恢复到t3℃。下列说法不正确的是______ 。(填序号)
①恢复到原温度后,析出晶体的质量:A>B
②恢复到原温度后,溶剂的质量:A>B
③若再降温到t2℃,溶液的溶质质量分数:A=B
④若再降温到t2℃,溶质的质量:A<B

(1)点P表示
(2)t3℃时,三种物质的饱和溶液的溶质质量分数由小到大为
(3)将t3℃的A物质的饱和溶液75g降温到t1℃,析出A物质
(4)为除去A中混有的少量B,宜采用
(5)t3℃时,取A、B两物质的等质量饱和溶液分别蒸发等量的水后,恢复到t3℃。下列说法不正确的是
①恢复到原温度后,析出晶体的质量:A>B
②恢复到原温度后,溶剂的质量:A>B
③若再降温到t2℃,溶液的溶质质量分数:A=B
④若再降温到t2℃,溶质的质量:A<B
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐3】如表为硝酸钾和氯化钠的部分溶解度数据,某同学进行了如下图所示的两个溶解实验。

(1)由表格数据可知,溶解度随温度升高变化显著的物质是_____ (选填“NaCl”或“KNO3”)。
(2)上述溶液中属于饱和溶液的是_____ (填 A-F 序号)。
(3)BCEF 溶液中溶质质量分数由大到小的关系是_____ (用“<”、“>”、“=”表示)
(4)关于图中有关说法不正确的是_____ 。
A B烧杯的溶液还可以溶解硝酸钾固体
B 将20℃时硝酸钾的不饱和溶液转化为饱和溶液的方法:蒸发溶剂或升高温度
C 氯化钠中混有少量的硝酸钾可以用蒸发结晶的方法除去
| 物质/溶解度/g/温度 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |

(1)由表格数据可知,溶解度随温度升高变化显著的物质是
(2)上述溶液中属于饱和溶液的是
(3)BCEF 溶液中溶质质量分数由大到小的关系是
(4)关于图中有关说法不正确的是
A B烧杯的溶液还可以溶解硝酸钾固体
B 将20℃时硝酸钾的不饱和溶液转化为饱和溶液的方法:蒸发溶剂或升高温度
C 氯化钠中混有少量的硝酸钾可以用蒸发结晶的方法除去
您最近一年使用:0次




