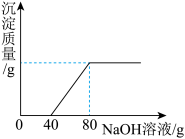
实验室有一份在空气中潮解部分变质的氢氧化钠样品,质量为1.86g。某实验小组将这份样品完全溶解,配成50g溶液,然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如表所示:
请回答下列问题:
(1)检验氢氧化钠是否变质可以用______溶液,请写出你的实验方案(简要说明操作步骤、现象和结论)______。
(2)实验中生成二氧化碳的质量为 g。
(3)求样品中氢氧化钠的质量。(写出计算过程)
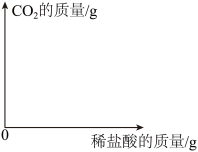
(4)请在如图中画出稀盐酸质量与二氧化碳质量关系的图象(温馨提醒:标出关键点的数据)。
| 测量次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 滴加的盐酸总质量/g | 0 | 5 | 20 | 30 | 35 |
| 溶液总质量/g | 50 | 55 | 69.56 | 79.56 | 84.56 |
| 溶液 pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
(1)检验氢氧化钠是否变质可以用______溶液,请写出你的实验方案(简要说明操作步骤、现象和结论)______。
(2)实验中生成二氧化碳的质量为 g。
(3)求样品中氢氧化钠的质量。(写出计算过程)
(4)请在如图中画出稀盐酸质量与二氧化碳质量关系的图象(温馨提醒:标出关键点的数据)。

2021·江西赣州·一模 查看更多[1]
更新时间:2021-05-27 09:18:30
|
相似题推荐
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】侯氏制碱法的主要反应为:NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl.一定温度下,向92.6g饱和NaCl溶液中先通入足量NH3,再通入一定量CO2发生反应,若参加反应的NH3质量为3.4g,请计算:(写出计算步骤,不考虑溶解在溶液中的NH3和CO2的质量)。
(1)消耗CO2的质量是多少?
(2)反应后称量溶液中析出NaHCO3晶体的质量为11.8g,则剩余溶液的质量是多少?
(3)求剩余溶液中NaHCO3的质量分数(计算结果精确到0.1%)。
(1)消耗CO2的质量是多少?
(2)反应后称量溶液中析出NaHCO3晶体的质量为11.8g,则剩余溶液的质量是多少?
(3)求剩余溶液中NaHCO3的质量分数(计算结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】牙膏中的摩擦剂可以增强牙青对牙齿的摩擦作用和去污效果,已知某品牌牙膏中的的摩擦剂是CaCO3和SiO2的混合物(SiO2不溶于水也不与稀盐酸反应),为了测定这种摩擦剂中CaCO3的质量分数,化学兴趣小组的同学做了如下实验。
称取10g摩擦剂加入到盛有40g稀盐酸的烧杯中,立即将烧杯放在天平上称量。在以后的6min内,每一分钟读一次数。结果如下:
请计算:
(1)生成二氧化碳的质量为______g。
(2)求摩擦剂中CaCO3的质量分数,(写出计算过程)
称取10g摩擦剂加入到盛有40g稀盐酸的烧杯中,立即将烧杯放在天平上称量。在以后的6min内,每一分钟读一次数。结果如下:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 50.0 | 49.0 | 48.4 | 48.1 | 47.9 | 47.8 | 47.8 |
(1)生成二氧化碳的质量为______g。
(2)求摩擦剂中CaCO3的质量分数,(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】“中国天眼”是世界上口径最大的单天线射电望远镜,其“眼镜片”由金刚砂(SiC)制造。生产SiC的化学方程式为SiO2+3C SiC+2CO↑。
SiC+2CO↑。
(1)SiO2中Si元素的化合价为______ 。
(2)生产160kg 的SiC,理论上消耗C的质量为多少?
 SiC+2CO↑。
SiC+2CO↑。(1)SiO2中Si元素的化合价为
(2)生产160kg 的SiC,理论上消耗C的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】取氯酸钾和二氧化锰的混合物 16g 加热制取氧气,随反应时间称量固体物质的质量如下表:
(1)根据上表数据分析充分反应后,产生的氧气为______ 克。
(2)原混合物中氯酸钾的质量是多少克?(写出完整计算过程)
(3)原混合物中氯元素的质量分数是______ (精确到0.1%)。
第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
14.2g | 12.4g | 11.4g | 11.2g | 11.2g |
(1)根据上表数据分析充分反应后,产生的氧气为
(2)原混合物中氯酸钾的质量是多少克?(写出完整计算过程)
(3)原混合物中氯元素的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室有一瓶含有Na2SO4和Na2CO3的混合溶液,某化学兴趣小组设计实验来测定溶液的质量分数。他们经过讨论后设计了如下图一装置进行实验探究:

实验过程中,向100g混合液先加入Ba(NO3)2溶液,再加稀硝酸,得沉淀变化趋势如图二,请你根据题意回答问题:
(1)22.03g沉淀中含有什么物质?_____(填化学式)。针筒注入稀硝酸产生气体的化学方程式为_____。
(2)求原混合液中Na2SO4的质量分数。_____(写出过程)

实验过程中,向100g混合液先加入Ba(NO3)2溶液,再加稀硝酸,得沉淀变化趋势如图二,请你根据题意回答问题:
(1)22.03g沉淀中含有什么物质?_____(填化学式)。针筒注入稀硝酸产生气体的化学方程式为_____。
(2)求原混合液中Na2SO4的质量分数。_____(写出过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】黄铜是铜锌合金。为了测定某黄铜样品中锌的质量分数,化学小组的同学取25 g黄铜样品于烧杯中,并将80g稀硫酸分4次依次加入到黄铜样品中,测得的实验数据如下表:
请完成下列分析与计算:
(1)恰好反应时所用稀硫酸的质量是_____g
(2)计算该黄铜样品中锌的质量分数_____。
| 实验编号 | 第1次 | 第2次 | 第3次 | 第4次 |
| 稀硫酸的质量/g | 20 | 20 | 20 | 20 |
| 充分反应后烧杯中剩余物质的质量/g | 44.8 | 64.6 | 84.5 | 104.5 |
请完成下列分析与计算:
(1)恰好反应时所用稀硫酸的质量是_____g
(2)计算该黄铜样品中锌的质量分数_____。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】家用纯碱常含有少量的氯化钠杂质。为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品1.1g,充分溶解于13g水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示。求:(友情提示:该反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl)

(1)该纯碱样品中碳酸钠的质量______。
(2)恰好完全反应时所得溶液的溶质质量分数。
(3)通过交流反思,同学们认为下列做法会影响样品中碳酸钠的质量分数测定结果的是______
A 加入氯化钙溶液质量太少(少于11.1g)
B 称量完纯碱样品质量后,在放入烧杯的过程部分样品洒出
C 量取溶解纯碱样品的水时仰视读数
D 使用足量稀盐酸代替氯化钙溶液进行实验,测定反应后生成CO2的质量并计算

(1)该纯碱样品中碳酸钠的质量______。
(2)恰好完全反应时所得溶液的溶质质量分数。
(3)通过交流反思,同学们认为下列做法会影响样品中碳酸钠的质量分数测定结果的是______
A 加入氯化钙溶液质量太少(少于11.1g)
B 称量完纯碱样品质量后,在放入烧杯的过程部分样品洒出
C 量取溶解纯碱样品的水时仰视读数
D 使用足量稀盐酸代替氯化钙溶液进行实验,测定反应后生成CO2的质量并计算
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】如图是某种加钙食盐包装标签上的部分内容。 请仔细阅读后回答以下问题:
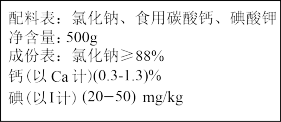
(1)为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是____________。
(2)为了测定此盐中的碳酸钙含量,取50 g这种盐溶于水, 加入足量盐酸, 生成0.66 g二氧化碳。 请计算此加钙食盐中碳酸钙的质量分数____________。
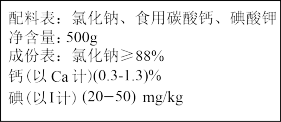
(1)为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是____________。
(2)为了测定此盐中的碳酸钙含量,取50 g这种盐溶于水, 加入足量盐酸, 生成0.66 g二氧化碳。 请计算此加钙食盐中碳酸钙的质量分数____________。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】科学兴趣小组的同学们对鸡蛋壳的成分开展了有关探究。同学们的实验过程如下:①将一定量的鸡蛋壳放入容器中;②往其中加入适量的稀盐酸,观察到有较多的气泡产生;③……;④得出结论:鸡蛋壳的主要成分是碳酸盐(如:碳酸钙)。_________ 。
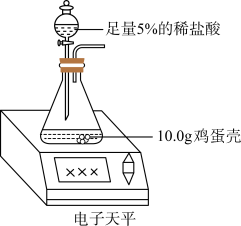
【实验步骤】小朋称取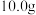 鸡蛋壳样品,加入足量的稀盐酸,按如图装置实验,记录数据如下:
鸡蛋壳样品,加入足量的稀盐酸,按如图装置实验,记录数据如下:
【数据分析】
(2)产生二氧化碳的质量是_________  。
。
【实验结论】
(3)该鸡蛋壳中样品中含有碳酸钙,求样品中含有碳酸钙质量分数是多少?
【实验反思】
(4)经查实,上述方法所测得鸡蛋壳中碳酸钙含量偏大(若实验操作规范),导致偏大的原因可能是 。
【实验步骤】小朋称取
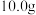 鸡蛋壳样品,加入足量的稀盐酸,按如图装置实验,记录数据如下:
鸡蛋壳样品,加入足量的稀盐酸,按如图装置实验,记录数据如下:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| 装置和药品总质量(g) | 261.0 | 260.0 | 259.3 | 259.0 | 258.8 | 258.8 | 258.8 |
(2)产生二氧化碳的质量是
 。
。【实验结论】
(3)该鸡蛋壳中样品中含有碳酸钙,求样品中含有碳酸钙质量分数是多少?
【实验反思】
(4)经查实,上述方法所测得鸡蛋壳中碳酸钙含量偏大(若实验操作规范),导致偏大的原因可能是 。
| A.有水蒸气逸出 | B.盐酸浓度太大 | C.锥形瓶内残留二氧化碳 |
您最近一年使用:0次

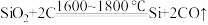 。现有120kg的SiO2,理论上可生产硅的质量为多少?
。现有120kg的SiO2,理论上可生产硅的质量为多少?