电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),以下是某兴趣小组设计的处理该生产过程中产生废液的流程图。据图回答下列问题:
查阅资料: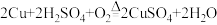 ;
; 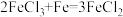
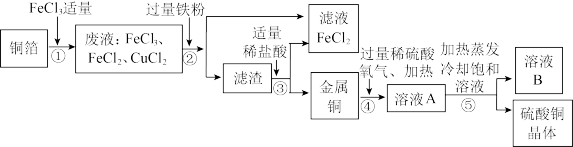
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是______ (写化学式)。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是______ 。步骤②还需要进行的实验操作是______ 。
(3)步骤③加入适量稀盐酸充分反应,当观察到______ 现象时,说明滤渣中只剩下铜。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用。根据质量守恒定律可推测该单质是______ 。
(5)溶液B中含有的溶质是______ 。
查阅资料:
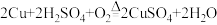 ;
; 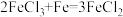

(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是
(3)步骤③加入适量稀盐酸充分反应,当观察到
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用。根据质量守恒定律可推测该单质是
(5)溶液B中含有的溶质是
更新时间:2021-07-05 16:19:12
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】2021辛丑牛年,南京博物院展出战国时期的“牛牛酒壶”﹣错金银铜牺尊。其造型像牛表面装饰了金银图案的青铜酒器。

(1)“牛牛酒壶”的主要材质是青铜,青铜的熔点_______ (选填“高于”、“低于”或“等于”)其组成金属的熔点。
(2)错金银铜牺尊表面的银装饰线已经发黑,原因之一是银与氧气、硫化氢反应生成了硫化银(Ag2S)和水。该反应的化学方程式为_______ 。
(3)历经千年,牺尊表面锈蚀生成了碱式碳酸铜【Cu2(OH)2CO3】。铜的锈蚀是铜与空气中的___ (填化学式)等物质共同作用的过程。

(1)“牛牛酒壶”的主要材质是青铜,青铜的熔点
(2)错金银铜牺尊表面的银装饰线已经发黑,原因之一是银与氧气、硫化氢反应生成了硫化银(Ag2S)和水。该反应的化学方程式为
(3)历经千年,牺尊表面锈蚀生成了碱式碳酸铜【Cu2(OH)2CO3】。铜的锈蚀是铜与空气中的
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】轻质氧化镁广泛应用于耐火材料,是重要的工业原料。某矿石主要成分为Fe2O3、MgO和SiO2,以该矿石为原料按如图所示流程进行生产,可制得轻质氧化镁。

查阅资料得下表相关数据:
(1)步骤①②③用到的共同操作是_____________ 。
(2)步骤①对应的现象有_____________。
(3)为了完全沉淀沉淀B,又不损失沉淀E,则步骤②的pH范围可以为_____________。
(4)写出步骤③生成沉淀E的化学方程式___________ 。
(5)下列说法正确的是___________。

查阅资料得下表相关数据:
| 物质 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 沉淀完全的pH | 3.2 | 11.1 |
(2)步骤①对应的现象有_____________。
| A.固体减少 | B.溶液变为黄色 | C.溶液变为浅绿色 | D.有气泡产生 |
| A.1.5<pH<3.2 | B.3.2<pH<8.6 | C.8.6<pH<11.1 | D.pH>11.1 |
(5)下列说法正确的是___________。
| A.溶液A中阳离子有两种 |
| B.根据以上信息可以判断,SiO2不溶于稀盐酸,但可能易溶于水 |
| C.若步骤④分解成两种氧化物,则另一个产物为H2O |
| D.溶液A中含有的Cl-与滤液D中含有的Cl-个数相等 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
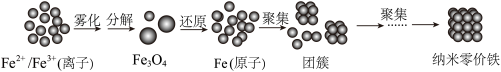
【推荐3】纳米零价铁(nZVI)除废水中金属离子的性能优越,制备示意图为:______ (填“升高”“降低”或“不变”)。
(2)“还原”过程,一定量焦炭与232gFe3O4作用,生成CO2,反应的化学方程式为______ ,若反应后所得固体中焦炭与铁的质量比为1:14,则加入焦炭的质量是______ 。
(3)“雾化”过程,发生反应:
______ (补充完整该方程式)。
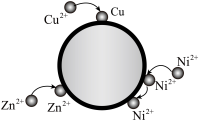
(4)nZVI用于去除废水中金属离子,根据金属活动性顺序可分三种途径(如图所示),第一类是吸附捕捉(如Zn2+),第二类是吸附捕捉再慢慢反应(如Pb2+),第三类是直接反应(如Cu2+)。______ 类;
②若 属于第一类,则金属Cd比金属Ag的活动性
属于第一类,则金属Cd比金属Ag的活动性______ (填“强”“弱”或“接近”);
③废水中CuCl2与nZVI发生的反应属于______ (填基本反应类型)。
(2)“还原”过程,一定量焦炭与232gFe3O4作用,生成CO2,反应的化学方程式为
(3)“雾化”过程,发生反应:

(4)nZVI用于去除废水中金属离子,根据金属活动性顺序可分三种途径(如图所示),第一类是吸附捕捉(如Zn2+),第二类是吸附捕捉再慢慢反应(如Pb2+),第三类是直接反应(如Cu2+)。
②若
 属于第一类,则金属Cd比金属Ag的活动性
属于第一类,则金属Cd比金属Ag的活动性③废水中CuCl2与nZVI发生的反应属于
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐1】向一定质量的AgNO3、Cu(NO3)2和Al(NO3)3的混合溶液中加入26g锌粉,充分反应后过滤,得到滤渣和滤液,将所得滤渣进行干燥并称量,所得滤渣质量为56g。向所得滤渣上滴加稀盐酸时无气泡产生。
(1)滤液中一定含有的溶质是_______ (写化学式,下同),一定不含有的溶质是______ 。
(2)所得滤渣中铜的质量为_________ 。
(1)滤液中一定含有的溶质是
(2)所得滤渣中铜的质量为
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】向一定质量的硝酸银和硝酸铜的混合溶液中加入一定质量的铁粉,充分反应后过滤,得到滤液和滤渣,然后向滤渣中加入稀硫酸,发现有气泡产生。
(1)加入铁粉的过程中,溶液的颜色如何变化?
(2)滤渣中一定含有的成分有哪些?
(3)写出产生气泡的反应的化学方程式。
(1)加入铁粉的过程中,溶液的颜色如何变化?
(2)滤渣中一定含有的成分有哪些?
(3)写出产生气泡的反应的化学方程式。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】某电镀厂排放的废液中含有CuSO4、FeSO4和ZnSO4三种溶质,为减少水污染并节约成本,回收硫酸锌、金属铁和铜,设计流程如图所示,下列说法正确的是

(1)含铁元素的物质(污水除外)有______ (填字母序号A、B、C、D、E)。
(2)向污水中加入过量甲,发生的反应方程式为_______ (任写一个)。
(3)操作④用到的仪器有铁架台、酒精灯、玻璃棒和_______ ,玻璃棒的作用为_______ 。
(4)下列说法正确的是 。

(1)含铁元素的物质(污水除外)有
(2)向污水中加入过量甲,发生的反应方程式为
(3)操作④用到的仪器有铁架台、酒精灯、玻璃棒和
(4)下列说法正确的是 。
| A.操作①、②、③均为过滤 |
| B.不考虑损耗,最终得到ZnSO4的质量与原溶液中ZnSO4的质量相等 |
| C.加入适量稀硫酸后,可观察到固体部分溶解,有气泡生成,溶液不变色 |
| D.可用BaCl2溶液和稀硝酸检验操作③中稀硫酸是否过量 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】现有 A、B、C、D、E、F、G 七种物质,C 是目前年产量最高的金属,A 是黑色固体,B 是气体单质,D 为浅绿色溶液,G 为蓝色溶液,它们之间存在如下关系:
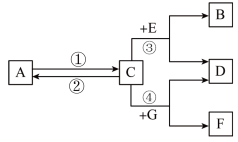
请回答下列问题:
(1)F 的化学式:______ 。
(2)反应③的化学方程式:______ 。
(3)反应②的基本类型:______ 。
(4)反应①在生产生活中的应用:______ 。

请回答下列问题:
(1)F 的化学式:
(2)反应③的化学方程式:
(3)反应②的基本类型:
(4)反应①在生产生活中的应用:
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】金属材料在生产、生活中有广泛的用途。某兴趣小组对金属材料开展项目式学习。
【任务1】金属在地壳中的含量
(1)地壳中含量最多的金属元素与氧元素形成的化合物的化学式为______ 。
【任务2】金属的冶炼
(2)某炼铁厂以赤铁矿为原料炼铁,请写出反应的化学方程式:______ 。
【任务3】金属的化学性质
该兴趣小组将铝片放入盛有一定量稀盐酸的三颈烧瓶中,分别用压强传感器和温度传感器测量压强和温度,它们随时间的变化曲线如图1、图2所示。
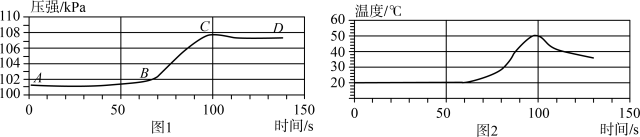
(3)根据曲线分析:AB段压强没有明显的变化可能的原因是______ 。BC段压强增大的原因是______ ;CD段压强减小的原因是______ 。
(4)在任务3的基础上,该兴趣小组将打磨过的铝片放入等浓度的稀硫酸中,发现没有明显的气泡。请你从微观角度分析可能的原因,并设计实验验证你的猜想。
【任务1】金属在地壳中的含量
(1)地壳中含量最多的金属元素与氧元素形成的化合物的化学式为
【任务2】金属的冶炼
(2)某炼铁厂以赤铁矿为原料炼铁,请写出反应的化学方程式:
【任务3】金属的化学性质
该兴趣小组将铝片放入盛有一定量稀盐酸的三颈烧瓶中,分别用压强传感器和温度传感器测量压强和温度,它们随时间的变化曲线如图1、图2所示。

(3)根据曲线分析:AB段压强没有明显的变化可能的原因是
(4)在任务3的基础上,该兴趣小组将打磨过的铝片放入等浓度的稀硫酸中,发现没有明显的气泡。请你从微观角度分析可能的原因,并设计实验验证你的猜想。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】金属钛是重要的航天、航海材料,钛因其硬度大,熔点高,常温下不和非金属、强酸反应,被 誉为“未来金属”。由钛铁矿(主要成分为钛酸亚铁,化学式为 FeTiO3)、焦炭、氧气为原料,提取金属钛的主要工艺过程一般需要经过三个阶段:
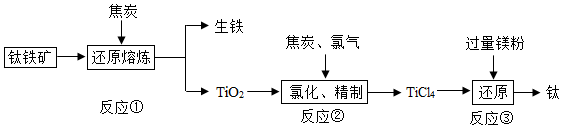
(1)反应前需要将钛酸亚铁和焦炭磨成粉末状的原因是__________________ ;钛酸亚铁(FeTiO3)中钛元素为_________ 价。
(2)反应①中焦炭除了作还原剂还原金属矿物外,另一个重要作用是____________________________ 。
(3)反应②中 TiO2 与 C、Cl2 在高温下反应,生成 TiCl4 和一种有毒气体,该气体是一种氧化物,其化学式为______________ 。
(4)高温条件下,镁可以与 TiCl4 发生置换反应制得金属钛,请写出此反应的化学方程 式___________ ,该反应属于________________ 反应(基本反应类型),该反应需在氩气环境中进行,氩气起的作用是_______________ 。
(5)如何从反应③后的固体中获得金属钛:向固体中加入足量的__________ ,充分反应后_________ ,洗涤,干燥。

(1)反应前需要将钛酸亚铁和焦炭磨成粉末状的原因是
(2)反应①中焦炭除了作还原剂还原金属矿物外,另一个重要作用是
(3)反应②中 TiO2 与 C、Cl2 在高温下反应,生成 TiCl4 和一种有毒气体,该气体是一种氧化物,其化学式为
(4)高温条件下,镁可以与 TiCl4 发生置换反应制得金属钛,请写出此反应的化学方程 式
(5)如何从反应③后的固体中获得金属钛:向固体中加入足量的
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐1】某沿海工业区排放的污水中含有少量的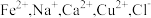 ,为了达到零污染的目标,将污水,进行如下工业流程处理:
,为了达到零污染的目标,将污水,进行如下工业流程处理:
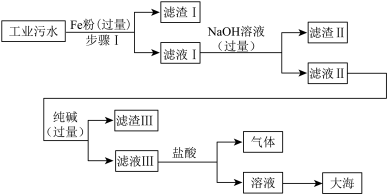
(1)得到滤渣I和滤渣II的操作中所用到的玻璃仪器有玻璃棒、烧杯和______ 。
(2)加入过量 溶液的目的是
溶液的目的是______ .
(3)在滤液Ⅲ中加入盐酸使得到的溶液呈中性,要使用______ 来测定溶液的酸碱度,确保盐酸不过量。
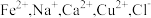 ,为了达到零污染的目标,将污水,进行如下工业流程处理:
,为了达到零污染的目标,将污水,进行如下工业流程处理:
(1)得到滤渣I和滤渣II的操作中所用到的玻璃仪器有玻璃棒、烧杯和
(2)加入过量
 溶液的目的是
溶液的目的是(3)在滤液Ⅲ中加入盐酸使得到的溶液呈中性,要使用
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】黑白复印机用的墨粉中常添加Fe3O4粉末,Fe3O4是由Fe2+、Fe3+和O2-按1:2:4的个数比构成的。如图是氧化沉淀法生产复印用Fe3O4粉末的流程简图。已知第④步反应中各元素化合价保持不变。

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是______ 色。
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为______ 。
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于______ ,才能确保最终生成Fe3O4,操作Y的名称为 ______ 。

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
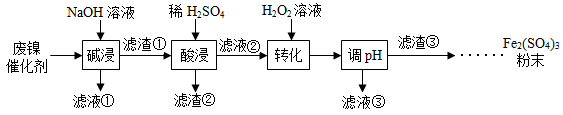
【推荐3】某油脂厂废弃的油脂加氢镍催化剂主要含金属 Ni、Al、Fe 及其他不溶性物质。采用如图工艺流程回收其中的铁制备硫酸铁粉末。
已知:①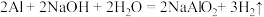
②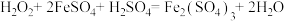
③NiSO4等物质完全生成 Ni(OH)2等沉淀时的 pH 如表所示:
回答下列问题:
(1)碱浸除去的物质是______ (用化学式表示)。
(2)碱浸后的实验操作是___________ ,用到的玻璃仪器有烧杯、______ 、______ 。
(3)写出酸浸的化学反应方程式______ (写一条即可)。
(4)加入 H2O2进行物质转化的目的是______ 。
(5)调 pH 要使 Fe2(SO4)3完全沉淀,pH 最低不能低于______ 。
(6)向滤渣③中加入稀 H2SO4制取产品同时生成一种常见氧化物的反应方程式是______ 。

已知:①
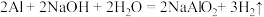
②
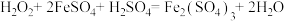
③NiSO4等物质完全生成 Ni(OH)2等沉淀时的 pH 如表所示:
| 物质 | NiSO4 | Al2(SO4)3 | Fe2(SO4)3 | FeSO4 |
| 沉淀 | Ni(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 完全沉淀时的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)碱浸除去的物质是
(2)碱浸后的实验操作是
(3)写出酸浸的化学反应方程式
(4)加入 H2O2进行物质转化的目的是
(5)调 pH 要使 Fe2(SO4)3完全沉淀,pH 最低不能低于
(6)向滤渣③中加入稀 H2SO4制取产品同时生成一种常见氧化物的反应方程式是
您最近一年使用:0次



