古往今来,金属材料和制品在生产生活中应用广泛。
(1)三星堆遗址发据现场出土了华丽的鸟型金饰片,金能被加工成超薄金箔,是因为金具有良好的___________ ;同时出土的铜头像、青铜神树等表面有锈迹,铜生锈的主要原理是: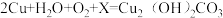 ,X的化学式为
,X的化学式为_____________ 。
(2)向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤,得到滤渣和滤液。
①在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化,则滤液中一定没有的阳离子是__________ 。(填离子符号)
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有__________ 。(填名称)
(1)三星堆遗址发据现场出土了华丽的鸟型金饰片,金能被加工成超薄金箔,是因为金具有良好的
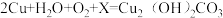 ,X的化学式为
,X的化学式为(2)向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤,得到滤渣和滤液。
①在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化,则滤液中一定没有的阳离子是
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有
2021·内蒙古鄂尔多斯·中考真题 查看更多[5]
内蒙古鄂尔多斯市2021年中考化学试题2022年江苏省无锡市侨谊教育集团中考二模化学试题2022年江苏省无锡市江阴市云亭中学中考考前化学家庭作业 (2)(已下线)课题2 金属的化学性质(共2课时)(好题精练)-2022-2023学年九年级化学下册精品课堂课件精讲及好题精练(人教版)(已下线)2023年重庆市中考化学真题(A卷)变式题(非选择题17~20)
更新时间:2021-07-08 15:32:48
|
相似题推荐
综合应用题
|
较难
(0.4)
解题方法
【推荐1】金属在生产、生活中广泛应用。
(1)不能用铁制容器盛放硫酸铜溶液的原因是_____ (用化学方程式表示)。
(2)纳米铁粉比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。

高温反应器中发生反应的化学方程式为_____ 。
(3)某生铁和钢的样品中,主要元素的质量分数如下表所示
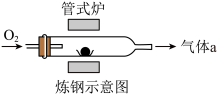
请结合数据及炼钢示意图分析:炼钢时通入过量氧气的目的是_____ ,气体a中一定含有的成分是_____ 。
(4)铝元素与人类关系密切,是现代文明不可或缺的物质基础。
①铝在地壳中的含量居所有金属元素第_____ 位。
②铝片在空气中表面易形成致密的氧化膜,请写出该反应的化学方程式_____ 。将除去氧化膜的铝片浸入硫酸铜溶液中,观察到铝片表面有红色物质析出,并伴随有气泡产生。经检验气体为氢气。该反应中产生氢气,说明硫酸铜溶液呈_____ (填“酸性”“中性”或“碱性”),可用_____ 检验溶液的酸碱度。
(5)金属镓常用于半导体材料制作。如图为镓在元素周期表中的相关信息。

①镓原子核外电子数为_____ 。
②镓与稀硫酸反应,产物中Ga的化合价为+3,写出该反应的化学方程式_____ 。
③高纯氧化镓广泛用于生产半导体材料。在一定条件下灼烧Ga(NH4)(SO4)2固体,可制得高纯氧化镓。Ga(NH4)(SO4)2中的阴离子是_____ (填化学符号)。
(1)不能用铁制容器盛放硫酸铜溶液的原因是
(2)纳米铁粉比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。

高温反应器中发生反应的化学方程式为
(3)某生铁和钢的样品中,主要元素的质量分数如下表所示
| Fe | C | S | |
| 生铁 | 95.94% | 3.52% | 0.06% |
| 钢 | 98.97% | 0.45% | 0.039% |

请结合数据及炼钢示意图分析:炼钢时通入过量氧气的目的是
(4)铝元素与人类关系密切,是现代文明不可或缺的物质基础。
①铝在地壳中的含量居所有金属元素第
②铝片在空气中表面易形成致密的氧化膜,请写出该反应的化学方程式
(5)金属镓常用于半导体材料制作。如图为镓在元素周期表中的相关信息。

①镓原子核外电子数为
②镓与稀硫酸反应,产物中Ga的化合价为+3,写出该反应的化学方程式
③高纯氧化镓广泛用于生产半导体材料。在一定条件下灼烧Ga(NH4)(SO4)2固体,可制得高纯氧化镓。Ga(NH4)(SO4)2中的阴离子是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】氧气和氧的化合物在工农业生产、生活中有广泛的应用。
(一)工业制 O2
(1)工业上根据 O2 和 N2 的_________ 不同,将液态空气分离得到氧气。
(2)揭开盛有液态空气的容器盖,将燃着的木条置于瓶口上方,可观察到 (填字母)。
(二)生活中的 O2
(3)某家庭制氧机上有湿化瓶装置。人吸氧时观察到瓶中有气泡。湿化瓶装置类似于右图。关于该装置,下列说法正确的有 (填字母)。

(三)实验室收集 O2
(4)为研究铁丝在不同浓度氧气中燃烧现象,现欲“收集 3/4 集气瓶的氧气”,请回答:
①下列装置和操作最合理的是_________ (填序号)。
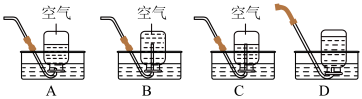
A.收集前集气瓶装 3/4 的水
B.收集前集气瓶中注满水,收集到集气瓶内剩 3/4 的水
C.收集前集气瓶装 3/4 的水
D.收集前集气瓶中注满水,收集到集气瓶内剩 3/4 的水
②空气中的体积分数约为 21%。本实验中集气瓶内的氧气约占总体积的_____ %。
(四)渔业制 O2 运输活鱼时用过氧化钙(CaO2)可增加水中含氧量。
(5)小明提出下列猜想并用如图装置进行实验:

【猜想】CaO2 与 H2O 反应用于实验室制取 O2。
【实验过程】
①连接仪器,检查装置的气密性;
②向试管中加入 CaO2 和 H2O 后,有极微量细小气泡缓慢放出。将导管伸入集气瓶中,几乎收集不到气体。放置到第二天,集气瓶中只收集到少量气体,振荡试管后仍有极微量细小气泡缓慢放出。
【实验结论】CaO2 与 H2O 反应_________ (填“能”或“不能”)用于实验室制取 O2。
【分析与反思】
③小明觉得储存 CaO2,注意的问题有_________ 。
④同学们对 CaO2 与 H2O 反应的生成物猜想如下:I.氢氧化钙和 O2;II.碳酸钙和氧气。小明认为猜想 II 一定是错误的,理由是_________ 。
(五)潜水员供 O2
(6)潜水员使用的供氧装置是用过氧化钠(Na2O2)和呼出的 CO2 反应生成碳酸钠(Na2CO3)和 O2。选择过氧化钠作供氧剂的优点是:①节约能源;②_________ 。
(7)过氧化钠还可以与水反应。该小组组装了如图所示的装置,实验中还观察到,伸入烧杯中的导管有气泡冒出, 其原因可能是_________ 。
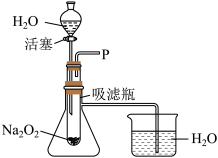
(一)工业制 O2
(1)工业上根据 O2 和 N2 的
(2)揭开盛有液态空气的容器盖,将燃着的木条置于瓶口上方,可观察到 (填字母)。
| A.木条熄灭 | B.木条先熄灭,后燃烧更旺 | C.木条燃烧更旺 |
(二)生活中的 O2
(3)某家庭制氧机上有湿化瓶装置。人吸氧时观察到瓶中有气泡。湿化瓶装置类似于右图。关于该装置,下列说法正确的有 (填字母)。

| A.使用该装置可以观测是否有 O2 输出 |
| B.使用该装置可以观测 O2 输出的速率 |
| C.a 导管连接制氧机 |
| D.a 导管连接人吸 O2 的塑料管 |
(三)实验室收集 O2
(4)为研究铁丝在不同浓度氧气中燃烧现象,现欲“收集 3/4 集气瓶的氧气”,请回答:
①下列装置和操作最合理的是

A.收集前集气瓶装 3/4 的水
B.收集前集气瓶中注满水,收集到集气瓶内剩 3/4 的水
C.收集前集气瓶装 3/4 的水
D.收集前集气瓶中注满水,收集到集气瓶内剩 3/4 的水
②空气中的体积分数约为 21%。本实验中集气瓶内的氧气约占总体积的
(四)渔业制 O2 运输活鱼时用过氧化钙(CaO2)可增加水中含氧量。
(5)小明提出下列猜想并用如图装置进行实验:

【猜想】CaO2 与 H2O 反应用于实验室制取 O2。
【实验过程】
①连接仪器,检查装置的气密性;
②向试管中加入 CaO2 和 H2O 后,有极微量细小气泡缓慢放出。将导管伸入集气瓶中,几乎收集不到气体。放置到第二天,集气瓶中只收集到少量气体,振荡试管后仍有极微量细小气泡缓慢放出。
【实验结论】CaO2 与 H2O 反应
【分析与反思】
③小明觉得储存 CaO2,注意的问题有
④同学们对 CaO2 与 H2O 反应的生成物猜想如下:I.氢氧化钙和 O2;II.碳酸钙和氧气。小明认为猜想 II 一定是错误的,理由是
(五)潜水员供 O2
(6)潜水员使用的供氧装置是用过氧化钠(Na2O2)和呼出的 CO2 反应生成碳酸钠(Na2CO3)和 O2。选择过氧化钠作供氧剂的优点是:①节约能源;②
(7)过氧化钠还可以与水反应。该小组组装了如图所示的装置,实验中还观察到,伸入烧杯中的导管有气泡冒出, 其原因可能是

您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】实验室常用下列装置来制取 、收集气体。仪器 b 是分液漏斗,可通过旋转活塞分次 滴加液体。请回答以下问题.
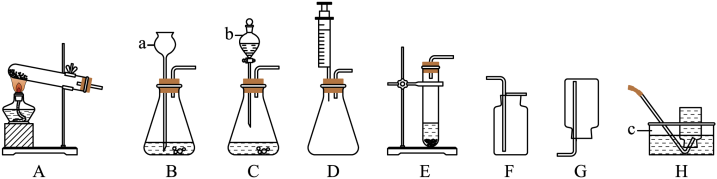
(1)仪器 a、c 的名称是:a_______________ ,c_______________ 。
(2)实验室用KMnO4 制取O2,应选用的发生装置和收集装置的组合为_______________ (填字 母序号),该发生装置的不足之处是_______________ ,该反应的化学方程式是_______________ 。
(3)实验室要制取少量CO2 应选择的较简单的发生装置是_______________ (填字母序号),收 集二氧化碳的装置是_______________ ,用 H 装置_______________ (填“能”或“否”)收集到二氧化碳。
(4)化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、 改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔 (C2H2) 气体和氢氧化钙,该反应的化学方程式是_______________ ,实验室制取乙炔时,须严格控制加水速 度,以免剧烈反应放热引起装置炸裂。图中适合制取乙炔气体的发生装置有_______________ (填装 置序号)。
(5)某可燃性气体可能是乙炔、甲烷、一氧化碳中的一种或两种.已知 13g 该气体在足量 的氧气中充分燃烧生成 44g 二氧化碳和 9g 水,则该气体可能的组成为_______________ 。
A.乙炔
B.乙炔和一氧化碳的混合物
C.甲烷和一氧化碳的混合物
D.甲烷和乙炔的混合物.
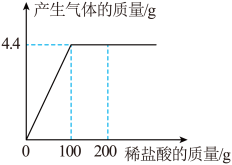
(6)取 CaCl2 和 CaCO3 的混合物 12.5g 于烧杯中,向其中滴加足量的稀盐酸,滴加稀盐酸 的质量与产生气体质量的关系如图所示。求:反应结束后仪器内 CaCl2 的质量为_______________ ?(写出计算过程)

(1)仪器 a、c 的名称是:a
(2)实验室用KMnO4 制取O2,应选用的发生装置和收集装置的组合为
(3)实验室要制取少量CO2 应选择的较简单的发生装置是
(4)化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、 改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔 (C2H2) 气体和氢氧化钙,该反应的化学方程式是
(5)某可燃性气体可能是乙炔、甲烷、一氧化碳中的一种或两种.已知 13g 该气体在足量 的氧气中充分燃烧生成 44g 二氧化碳和 9g 水,则该气体可能的组成为
A.乙炔
B.乙炔和一氧化碳的混合物
C.甲烷和一氧化碳的混合物
D.甲烷和乙炔的混合物.
(6)取 CaCl2 和 CaCO3 的混合物 12.5g 于烧杯中,向其中滴加足量的稀盐酸,滴加稀盐酸 的质量与产生气体质量的关系如图所示。求:反应结束后仪器内 CaCl2 的质量为

您最近一年使用:0次
【推荐1】(一)金属材料广泛应用于生产、生活中。
(1)用铜作导线,利用了铜的延展性和_______ 性。
(2)将等质量的A、B、C三种金属(生成物中金属元素均为+2价)。分别放入质量分数相等且足量的稀盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是_______ ,相对原子质量最大的是______ 。

(3)向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分析正确的是________(填字母序号)。
(二)某研究小组同学对铝和稀盐酸的反应进行了探究。如下图所示实验,先检查装置气密性,再将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如下图所示的气体压强与时间的关系曲线图。
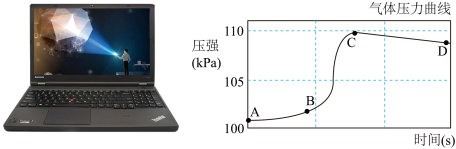
(4)铝与稀盐酸反应的化学方程式为______ 。
(5)AB段气体压强变化不明显的原因是_______ ;CD段气体压强逐渐下降的原因是______ 。
(6)从BC段看反应的速率是先变快后变慢,导致变慢的因素有_______(填序号)。
(1)用铜作导线,利用了铜的延展性和
(2)将等质量的A、B、C三种金属(生成物中金属元素均为+2价)。分别放入质量分数相等且足量的稀盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是

(3)向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分析正确的是________(填字母序号)。
| A.若滤渣只含一种金属,则滤液中的溶质一定有三种 |
| B.若滤液中含有两种金属阳离子,则滤渣中的固体一定有两种 |
| C.若最终得到的滤渣质量仍为mg,则滤液中溶质最多有两种 |
| D.若向滤渣中加入稀盐酸,有气泡产生,则滤液中的溶质最多有两种 |
(二)某研究小组同学对铝和稀盐酸的反应进行了探究。如下图所示实验,先检查装置气密性,再将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如下图所示的气体压强与时间的关系曲线图。

(4)铝与稀盐酸反应的化学方程式为
(5)AB段气体压强变化不明显的原因是
(6)从BC段看反应的速率是先变快后变慢,导致变慢的因素有_______(填序号)。
| A.铝片的表面积 | B.盐酸的浓度 | C.温度 |
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐2】金属铁是目前世界上使用最多的金属,在生产和生活中有着广泛的用途。
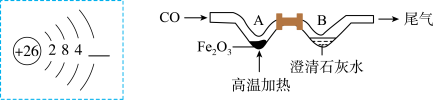
(1)请将上边虚线框内铁原子的结构示意图补画完整______ 。
(2)铁可制成铁锅烹调食物,利用了铁的延展性和_______ 性。
(3)用如图所示微型装置模拟工业炼铁。V形管中A处发生反应的化学方程式是_____ ;B处V形管内可观察到的现象是_____ ;
(4)某化学小组将一定量的铁粉加入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,滤液呈蓝色,则该实验过程中首先发生反应的化学方程式为_____ ;向滤渣中滴加盐酸时______ (填“有”或“没有”)气泡产生;滤液中一定含有的溶质是______ (写化学式);
(5)某实验室用废硫酸与铁反应制取硫酸亚铁。98g废硫酸与足量铁完全反应,生成0.2g气体,废硫酸中溶质的质量分数是_____ 。

(1)请将上边虚线框内铁原子的结构示意图补画完整
(2)铁可制成铁锅烹调食物,利用了铁的延展性和
(3)用如图所示微型装置模拟工业炼铁。V形管中A处发生反应的化学方程式是
(4)某化学小组将一定量的铁粉加入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,滤液呈蓝色,则该实验过程中首先发生反应的化学方程式为
(5)某实验室用废硫酸与铁反应制取硫酸亚铁。98g废硫酸与足量铁完全反应,生成0.2g气体,废硫酸中溶质的质量分数是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】金属材料在生活生产中有着非常广泛的应用。
(1)下列金属应用的事例,主要利用金属的导热性的是:________(填序号)。
(2)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用CO和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
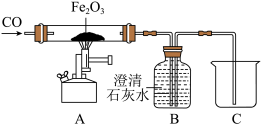
①A装置玻璃管中可观察到的现象为________ ;A装置中反应的化学方程式为________ ;
②该装置不需要添加尾气处理装置的原因________ ;
(3)铜锌合金又称“假黄金”。取40g“假黄金”样品,磨成粉末放入烧杯,向其中加入100g稀硫酸,恰好完全反应,反应后烧杯中物质的总质量为139.6g,请计算该“假黄金”样品中铜的质量分数是________ 。
(1)下列金属应用的事例,主要利用金属的导热性的是:________(填序号)。
| A.电缆 | B.电热壶 | C.金属包装材料 | D.金属乐器 |
(2)早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用CO和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:

①A装置玻璃管中可观察到的现象为
②该装置不需要添加尾气处理装置的原因
(3)铜锌合金又称“假黄金”。取40g“假黄金”样品,磨成粉末放入烧杯,向其中加入100g稀硫酸,恰好完全反应,反应后烧杯中物质的总质量为139.6g,请计算该“假黄金”样品中铜的质量分数是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】铁及其化合物在生产生活中应用非常广泛。
一、铁的相关知识

(1)人类使用金属先后经历了“青铜”时代、“铁器”时代,铝材料到近代才开始大量使用。这反映出 三种金属的活动性由强到弱的顺序是
三种金属的活动性由强到弱的顺序是______ 。
(2)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理______ 。
(3)磁铁矿是早期司南的材料,磁铁矿中所含铁的氧化物主要是______ 。
(4) 可以作为补铁剂,可以防止
可以作为补铁剂,可以防止______ ,其药片表面包裹着糖衣,如无此糖衣, 暴露在空气中易转化成
暴露在空气中易转化成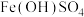 而失效,该转化的化学反应方程式为
而失效,该转化的化学反应方程式为______ 。
二、铁红 的制备
的制备
以 和
和 为原料生产
为原料生产 和铁红
和铁红 颜料,部分流程如下:
颜料,部分流程如下:

(5)流程中加入的“ 溶液”是
溶液”是______ 。
(6)流程中加入“有机溶剂”的作用是______ (填“增大”或“减小”) 的溶解度。
的溶解度。
(7) 晶体需要经过洗涤才能得到高纯度的产品。洗涤时最好选用
晶体需要经过洗涤才能得到高纯度的产品。洗涤时最好选用______ 。
a. 饱和溶液 b.热水 c.
饱和溶液 b.热水 c. 饱和溶液
饱和溶液
(8)在空气中灼烧 可以获得铁红和一种常见气体,反应的化学方程式为
可以获得铁红和一种常见气体,反应的化学方程式为______ 。
三、铁的化合物含量测定
上述流程中制得的 中混有
中混有 ,为确定其组成,兴趣小组称取此样品
,为确定其组成,兴趣小组称取此样品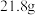 ,在科研人员的指导下用下图装置进行实验。现控制
,在科研人员的指导下用下图装置进行实验。现控制 装置中的温度为
装置中的温度为 对样品进行热分解,直至
对样品进行热分解,直至 装置中剩余固体质量不再变化为止,测量各装置质量,数据见下表。
装置中剩余固体质量不再变化为止,测量各装置质量,数据见下表。
【资料】
① 在
在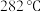 时分解为
时分解为 和
和 。
。
②温度高于 时铁的氧化物才能被
时铁的氧化物才能被 还原。
还原。
③常温下, 能与氯化钯
能与氯化钯 溶液反应。
溶液反应。
④用 还原
还原 的过程大致分为三个阶段:
的过程大致分为三个阶段:
阶段1: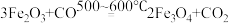
阶段2: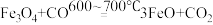
阶段3: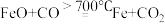

继续向装置中通 ,用
,用 还原铁的氧化物。加热时测得各装置质量随温度变化的情况如下表
还原铁的氧化物。加热时测得各装置质量随温度变化的情况如下表
(9)装置 的作用是
的作用是______ 。
(10)样品中 的质量分数为
的质量分数为______ (精确到0.1%).
(11) 时,装置
时,装置 中固体为纯净物,表格中的
中固体为纯净物,表格中的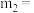
______ 。
(12)当温度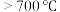 时,测得此时装置
时,测得此时装置 总质量为
总质量为 ,则
,则 中剩余固体的成分及对应的质量
中剩余固体的成分及对应的质量______ 。
一、铁的相关知识

(1)人类使用金属先后经历了“青铜”时代、“铁器”时代,铝材料到近代才开始大量使用。这反映出
 三种金属的活动性由强到弱的顺序是
三种金属的活动性由强到弱的顺序是(2)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理
(3)磁铁矿是早期司南的材料,磁铁矿中所含铁的氧化物主要是
(4)
 可以作为补铁剂,可以防止
可以作为补铁剂,可以防止 暴露在空气中易转化成
暴露在空气中易转化成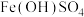 而失效,该转化的化学反应方程式为
而失效,该转化的化学反应方程式为二、铁红
 的制备
的制备以
 和
和 为原料生产
为原料生产 和铁红
和铁红 颜料,部分流程如下:
颜料,部分流程如下:
(5)流程中加入的“
 溶液”是
溶液”是(6)流程中加入“有机溶剂”的作用是
 的溶解度。
的溶解度。(7)
 晶体需要经过洗涤才能得到高纯度的产品。洗涤时最好选用
晶体需要经过洗涤才能得到高纯度的产品。洗涤时最好选用a.
 饱和溶液 b.热水 c.
饱和溶液 b.热水 c. 饱和溶液
饱和溶液(8)在空气中灼烧
 可以获得铁红和一种常见气体,反应的化学方程式为
可以获得铁红和一种常见气体,反应的化学方程式为三、铁的化合物含量测定
上述流程中制得的
 中混有
中混有 ,为确定其组成,兴趣小组称取此样品
,为确定其组成,兴趣小组称取此样品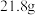 ,在科研人员的指导下用下图装置进行实验。现控制
,在科研人员的指导下用下图装置进行实验。现控制 装置中的温度为
装置中的温度为 对样品进行热分解,直至
对样品进行热分解,直至 装置中剩余固体质量不再变化为止,测量各装置质量,数据见下表。
装置中剩余固体质量不再变化为止,测量各装置质量,数据见下表。【资料】
①
 在
在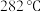 时分解为
时分解为 和
和 。
。②温度高于
 时铁的氧化物才能被
时铁的氧化物才能被 还原。
还原。③常温下,
 能与氯化钯
能与氯化钯 溶液反应。
溶液反应。④用
 还原
还原 的过程大致分为三个阶段:
的过程大致分为三个阶段:阶段1:
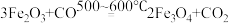
阶段2:
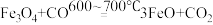
阶段3:
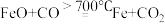

继续向装置中通
 ,用
,用 还原铁的氧化物。加热时测得各装置质量随温度变化的情况如下表
还原铁的氧化物。加热时测得各装置质量随温度变化的情况如下表温度/ | 室温 | 300 | 700 |  |
| A/g | 221.8 |  |  |  |
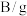 | 200.0 | 202.2 | 206.6 | 213.2 |
 的作用是
的作用是(10)样品中
 的质量分数为
的质量分数为(11)
 时,装置
时,装置 中固体为纯净物,表格中的
中固体为纯净物,表格中的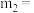
(12)当温度
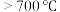 时,测得此时装置
时,测得此时装置 总质量为
总质量为 ,则
,则 中剩余固体的成分及对应的质量
中剩余固体的成分及对应的质量
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐2】某校化学社团的同学为探究金属的化学性质,进行如下实验。_____ 。
(2)小芸同学无意间将两种金属接触(见实验2),她发现铜片表面产生无色无味的气体。根据你已掌握的化学知识判断实验2中的气体不可能是 。
小芸同学又设计了实验3:将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面也产生无色无味的气体,电路中的电流计指针发生偏转。
【资料】
铜锌原电池:把铜、锌同时浸入稀硫酸,锌失去电子生成Zn2+,电子(e-)由锌片通过导线流向铜片,溶液中的氢离子从铜片处获得电子产生气体。
(3)由此推知实验2铜片上产生的气体是______ ,溶液的pH值将______ (填“变小”、“变大”或“不变”)。
(4)甲乙两小组成员用7g锌片与50g质量分数为9.8%的稀硫酸反应制取氢气,生成氢气的速率随时间的变化趋势并绘出图所示曲线。
①对比甲、乙两组数据后发现加入0.1g饱和硫酸铜溶液能够_______ (填“加快”或“减”)生成氢气的速率。结合资料推测该变化可能是锌与铜形成了原电池,在铜表面产生了气体,将_______ 能转化为电能。锌与硫酸铜反应的化学方程式为________ 。
②反应结束后,甲、乙两组发现均有固体剩余,计算甲组生成的氢气质量是多少?______ (写出计算过程)

(2)小芸同学无意间将两种金属接触(见实验2),她发现铜片表面产生无色无味的气体。根据你已掌握的化学知识判断实验2中的气体不可能是 。
| A.氢气 | B.氧气 | C.二氧化硫 | D.二氧化碳 |
小芸同学又设计了实验3:将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面也产生无色无味的气体,电路中的电流计指针发生偏转。
【资料】
铜锌原电池:把铜、锌同时浸入稀硫酸,锌失去电子生成Zn2+,电子(e-)由锌片通过导线流向铜片,溶液中的氢离子从铜片处获得电子产生气体。
(3)由此推知实验2铜片上产生的气体是
(4)甲乙两小组成员用7g锌片与50g质量分数为9.8%的稀硫酸反应制取氢气,生成氢气的速率随时间的变化趋势并绘出图所示曲线。
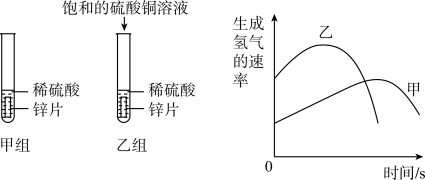
| 组别 | 锌片/g | 9.8%的稀硫酸/g | 是否加饱和硫酸铜溶液 |
| 甲组 | 7 | 50 | 未添加 |
| 乙组 | 7 | 50 | 添加 |
②反应结束后,甲、乙两组发现均有固体剩余,计算甲组生成的氢气质量是多少?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】对于金属材料,我们应该从多角度了解,
I、金属冶炼
(1)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。”鼓入足量空气的目的是______ ,从而提高炉温。
(2)为探究锌、铁、铜三种金属的活动性及它们和氢元素的位置关系。小明设计了如下实验:______ ,该反应属于______ (填基本反应类型)。
②小莉认为省略上述实验中的______ (填字母),也能达到实验目的。
Ⅲ、金属的锈蚀与防护
(3)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。“发蓝”过程属于______ (填“物理”或“化学”)变化。
IV、金属的回收再利用
(4)某学习小组同学欲从废旧电脑的某些零部件中回收金属银,设计流程如图所示。______ 。
②溶液X中只含有一种溶质,该溶质为______ 。(写化学式)
I、金属冶炼
(1)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。”鼓入足量空气的目的是
(2)为探究锌、铁、铜三种金属的活动性及它们和氢元素的位置关系。小明设计了如下实验:

②小莉认为省略上述实验中的
Ⅲ、金属的锈蚀与防护
(3)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。“发蓝”过程属于
IV、金属的回收再利用
(4)某学习小组同学欲从废旧电脑的某些零部件中回收金属银,设计流程如图所示。
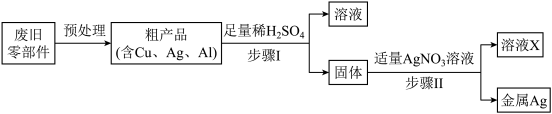
②溶液X中只含有一种溶质,该溶质为
您最近一年使用:0次



