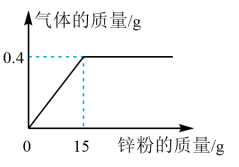
某实验小组同学做中和反应实验时,向160g质量分数为5%的氢氧化钠溶液中逐滴加入稀硫酸,恰好完全反应时,共用去稀硫酸124g,反应原理如下: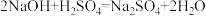 。
。
(1)理论计算:反应后所溶液的溶质的质量分数;
(2)实验分析:请说明如何判断氢氧化钠和稀硫酸恰好完全反应:______。
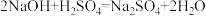 。
。(1)理论计算:反应后所溶液的溶质的质量分数;
(2)实验分析:请说明如何判断氢氧化钠和稀硫酸恰好完全反应:______。
2021·安徽安庆·二模 查看更多[3]
更新时间:2021-07-15 21:25:48
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某实验中学在市场上买了一箱含一定量的NaCl的烧碱用于学生实验,周晓同学取该烧碱样品10.3g完全溶于89.7g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸,在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示。

(1)该烧碱样品中,NaCl的质量分数为 (结果精确到0.1%);
(2)b点时,溶液中含有的溶质是 ;
(3)求a点时,溶液中溶质的质量分数。(写出计算过程)

(1)该烧碱样品中,NaCl的质量分数为 (结果精确到0.1%);
(2)b点时,溶液中含有的溶质是 ;
(3)求a点时,溶液中溶质的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】84消毒液的有效成分是次氯酸钠(NaClO),工业上制取次氯酸钠的反应原理是Cl2+2NaOH=NaClO+NaCl+H2O。某同学将一定质量的Cl2通入185.8g过量的NaOH溶液中,充分反应后得到混合溶液200g,计算所得混合溶液中次氯酸钠的质量分数____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】现有一瓶硫酸铜和稀硫酸的混合溶液 49.0 g,小玉向该混合溶液中逐渐滴加 10%的氢氧化钠溶液至过量。测得所加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示:
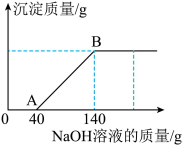
(1)与硫酸铜反应所消耗的氢氧化钠溶液的质量为____________g;
(2)请算出原混合溶液中稀硫酸的质量分数。(要求写出计算过程)

(1)与硫酸铜反应所消耗的氢氧化钠溶液的质量为____________g;
(2)请算出原混合溶液中稀硫酸的质量分数。(要求写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】兴趣小组的同学借助pH传感器测定某氢氧化钠溶液中溶质的质量分数。取20g氢氧化钠溶液于烧杯中,逐滴滴加3.65%的稀盐酸,并用玻璃棒不断搅拌,实验过程及溶液pH的变化曲线如图所示。
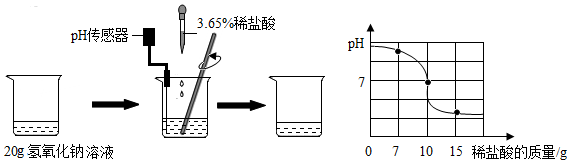
请计算:
(1)恰好反应完时,所消耗的稀盐酸质量为__________ 。
(2)计算该氢氧化钠溶液的溶质质量分数。

请计算:
(1)恰好反应完时,所消耗的稀盐酸质量为
(2)计算该氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某同学用溶质质量分数为10%的 溶液中和50g稀盐酸,反应过程中溶液的酸碱度情况如图所示。
溶液中和50g稀盐酸,反应过程中溶液的酸碱度情况如图所示。______ 。
(2)计算:50g稀盐酸中溶质的质量(写出计算过程)。
 溶液中和50g稀盐酸,反应过程中溶液的酸碱度情况如图所示。
溶液中和50g稀盐酸,反应过程中溶液的酸碱度情况如图所示。
(2)计算:50g稀盐酸中溶质的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】中和反应是放热反应。取10 mL溶质质量分数为10%的NaOH溶液(密度1.10g/mL)置于烧杯中(并滴入2滴酚酞),向烧杯中逐滴加入稀盐酸。随着盐酸的滴入,烧杯中溶液颜色从红色逐渐变浅,当加入10 mL稀盐酸时,溶液恰好变为无色。烧杯中溶液温度与加入盐酸体积之间关系如图所示。

(1)当加入4mL稀盐酸时,烧杯中溶液的溶质为________ (写化学式)
(2)试解释烧杯中溶液温度随加入盐酸的体积发生变化的 原因___________________ 。
(3)当盐酸与氢氧化钠恰好中和时生成氯化钠多少克?__________ (精确到0.1g)

(1)当加入4mL稀盐酸时,烧杯中溶液的溶质为
(2)试解释烧杯中溶液温度随加入盐酸的体积发生变化的 原因
(3)当盐酸与氢氧化钠恰好中和时生成氯化钠多少克?
您最近一年使用:0次