如图所示:向稀流酸中不断滴加氢氧化钡溶液时溶液的导电性变化。现请你设计实验,检验反应过程中溶液的溶质情况以及分别对应右图中的哪个阶段。限选试剂:BaCl2溶液、MgCl2溶液、Na2SO4溶液、Na2CO3溶液、NaOH溶液、稀盐酸、锌粒、氧化铜。
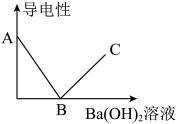

| 导电性 | 实验方案 | 实验操作及现象 |
| A.B段(不含A、B点)反应所得溶液中的离子有 | 阴离子检测:向所得溶液中加入(填物质类别) | 将反应混合物过滤,取少量滤液于试管中,加入 |
| 阳离子检测:向所得溶液中加入(填物质类别) | 将反应混合物过滤,取少量滤液于试管中,加入 | |
| BC段(不含B点)反应所得溶液中的离子有 | 阳离子检测:向所得溶液中加入含SO42-的可溶性盐溶液 | 将反应混合物过滤,取少量滤液于试管中,滴入少量Na2SO4溶液,现象是 |
| 阴离子检测:向所得溶液中加入(填物质类别) | 将反应混合物过滤,取少量滤液于试管中,滴入 |
更新时间:2021-07-26 16:37:03
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】学习小组同学用下图所示实验探究盐的化学性质。
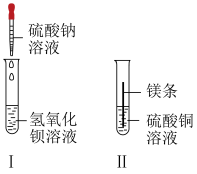
(1)实验Ⅰ中反应的化学方程式为_______ 。
(2)实验Ⅱ观察到镁条表面有______ 色固体析出。
(3)将实验Ⅰ、Ⅱ反应后的上层清液全部倒入同一烧杯,充分反应后过滤,得到白色沉淀和无色溶液。同学们对相关问题分组展开如下探究。
【反思评价】
①小明认为乙组所得结论不合理,理由是______ 。
②请设计实验证明乙组实验中猜想二正确:_______ (写出实验步骤和现象)。

(1)实验Ⅰ中反应的化学方程式为
(2)实验Ⅱ观察到镁条表面有
(3)将实验Ⅰ、Ⅱ反应后的上层清液全部倒入同一烧杯,充分反应后过滤,得到白色沉淀和无色溶液。同学们对相关问题分组展开如下探究。
| 实验探究 | 甲组 | 乙组 |
| 提出问题 | 白色沉淀是什么? | 无色溶液的溶质是什么? |
| 做出猜想 | 猜想一: 猜想二:Mg(OH)2和BaSO4 | 猜想一:Na2SO4 猜想二:Na2SO4、NaOH 猜想三:Na2SO4、MgSO4 |
| 实验操作 | 向白色沉淀中加入稀硝酸至过量 | 取少量无色溶液于试管中,滴加BaCl2溶液 |
| 实验现象 | 白色沉淀部分溶解 | 产生白色沉淀 |
| 实验结论 | 猜想 | 猜想二成立 |
①小明认为乙组所得结论不合理,理由是
②请设计实验证明乙组实验中猜想二正确:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】实施乡村振兴战略是新时代“三农”工作的一项任务。某校实践小组的同学在老师的帮助下,对当地土壤的酸碱度、土壤成分及土壤改良措施等产生了浓厚兴趣并展开了对项目化问题进行科学探究。
任务一:测定土壤酸碱度
【实验准备】在当地土壤中取样。将样品与蒸馏水按1:5的质量比在烧杯内混合,充分搅拌后,静置。
【进行实验】
(1)测液体的酸碱度:在玻璃片上放一小片pH试纸,用玻璃棒蘸取上层清液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,测出土壤呈碱性,pH范围是______ 。
任务二:探究适合生长的植物
【信息检索】下表为几种经济作物土壤生长的pH范围。
【小组交流】
(2)本地土壤不适宜种植的一种作物是______ 。
任务三:探究土壤成分
【查阅资料】当地土壤颜色是白色,含有NaCl、Na2CO3中的1种或2种。
【猜想与假设】①NaCl;②Na2CO3;③NaCl和Na2CO3。
【设计实验】验证当地土壤中是否含有NaCl和Na2CO3。
【教师指导】AgCl和Ag2CO3均为不溶于水的白色固体。
【进行实验】
(3)探究土壤成分,小组同学设计并完成如下实验:
【反思评价】
(4)步骤②中发生反应的化学方程式为______ 。
(5)小组同学对步骤②得出的结论产生了质疑,理由是______ 。
任务四:探究土壤改良
【调查咨询】
(6)近年来,我国应用微生物菌肥、生物有机肥、秸秆还田等方式,改良碱性土壤。根据土壤情况,改良酸性土壤应加入的物质是______ 。
(7)成果分享:改良土壤酸碱性在农业生产中的重要意义是______ (写1点)。
任务一:测定土壤酸碱度
【实验准备】在当地土壤中取样。将样品与蒸馏水按1:5的质量比在烧杯内混合,充分搅拌后,静置。
【进行实验】
(1)测液体的酸碱度:在玻璃片上放一小片pH试纸,用玻璃棒蘸取上层清液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,测出土壤呈碱性,pH范围是
任务二:探究适合生长的植物
【信息检索】下表为几种经济作物土壤生长的pH范围。
| 作物 | 茶树 | 棉花 | 苹果树 | 葱 | 海水稻 |
| 适宜生长的pH范围 | 5.0~5.5 | 6.0~6.8 | 6.0~8.0 | 7.0~7.4 | 8.0~9.2 |
(2)本地土壤不适宜种植的一种作物是
任务三:探究土壤成分
【查阅资料】当地土壤颜色是白色,含有NaCl、Na2CO3中的1种或2种。
【猜想与假设】①NaCl;②Na2CO3;③NaCl和Na2CO3。
【设计实验】验证当地土壤中是否含有NaCl和Na2CO3。
【教师指导】AgCl和Ag2CO3均为不溶于水的白色固体。
【进行实验】
(3)探究土壤成分,小组同学设计并完成如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少许上层清液于试管中,滴加足量 | 有气泡产生 | 含有Na2CO3 |
| ②另取少许上层清液于试管中,向其加入AgNO3溶液 | 含有NaCl |
【反思评价】
(4)步骤②中发生反应的化学方程式为
(5)小组同学对步骤②得出的结论产生了质疑,理由是
任务四:探究土壤改良
【调查咨询】
(6)近年来,我国应用微生物菌肥、生物有机肥、秸秆还田等方式,改良碱性土壤。根据土壤情况,改良酸性土壤应加入的物质是
(7)成果分享:改良土壤酸碱性在农业生产中的重要意义是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】化学兴趣小组的同学在探究碱溶液的化学性质时,进行了如图所示的实验。______________ 。为了进一步探究锥形瓶中NaOH是否有剩余,小组同学向锥形瓶内先加入过量的BaCl2溶液,目的是______ ,再进行一步操作就能得出结论,下列操作可行的是_______ 。
A.加入少量 FeCl3溶液 B.加入少量 MgCl2 溶液
C.加入少量 MgSO4溶液 D.向溶液中通入CO2气体
(2)实验B中发生反应的化学方程式为______________ 。
实验结束后,小组同学对B试管中上层清液的溶质成分产生疑问,作出猜想
猜想一:只含有NaOH;
猜想二:含有 NaOH、Na2CO3;
(3)猜想三:含有NaOH、______ ;
猜想四:含有NaOH、Na2CO3、Ca(OH)2;
(4)根据所学的化学知识,不用实验就可知猜想_______ 错误。
(5)实验C中产生的现象为______________ 。
(6)A、B、C、D四个实验中未能体现碱的化学通性的实验是______ (填字母)。

A.加入少量 FeCl3溶液 B.加入少量 MgCl2 溶液
C.加入少量 MgSO4溶液 D.向溶液中通入CO2气体
(2)实验B中发生反应的化学方程式为
实验结束后,小组同学对B试管中上层清液的溶质成分产生疑问,作出猜想
猜想一:只含有NaOH;
猜想二:含有 NaOH、Na2CO3;
(3)猜想三:含有NaOH、
猜想四:含有NaOH、Na2CO3、Ca(OH)2;
(4)根据所学的化学知识,不用实验就可知猜想
(5)实验C中产生的现象为
(6)A、B、C、D四个实验中未能体现碱的化学通性的实验是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学学习小组在完成“利用氯化钡溶液鉴别氯化钠和碳酸钠”的实验后,将所有废液倒入废液缸中,对废液缸中溶液的溶质成分进行了探究。请完成以下探究过程,并将空白处答案填入答题卡相应位置。
【提出问题】废液缸中溶液的溶质成分是什么?
【作出猜想】猜想 I.溶质仅为氯化钠;猜想Ⅱ.溶质为氯化钡和氯化钠;猜想Ⅲ._______ ;
【设计方案】
【交流反思】
学习小组经过讨论认为,可溶性钡盐有毒。含有可溶性钡盐的废液可以用碳酸钠溶液进行无害化处理。
①请写出硝酸钡与碳酸钠反应的化学方程式_______ 。
②人吃“钡餐”到胃中,可以检查胃是否健康。难溶性钡盐中有一种盐在医院能做钡餐。试判断碳酸钡能否做钡餐?_______ (填“能”或“不能”)。理由是 _______ 。
【提出问题】废液缸中溶液的溶质成分是什么?
【作出猜想】猜想 I.溶质仅为氯化钠;猜想Ⅱ.溶质为氯化钡和氯化钠;猜想Ⅲ.
【设计方案】
| 实验操作 | 现象 | 结论 |
| 取少量废液缸中上层清液,向其中加入一定量的 | 无明显现象 | 猜想 I 正确 |
| 猜想Ⅱ正确 | ||
| 有气泡产生 | 猜想Ⅲ正确 |
【交流反思】
学习小组经过讨论认为,可溶性钡盐有毒。含有可溶性钡盐的废液可以用碳酸钠溶液进行无害化处理。
①请写出硝酸钡与碳酸钠反应的化学方程式
②人吃“钡餐”到胃中,可以检查胃是否健康。难溶性钡盐中有一种盐在医院能做钡餐。试判断碳酸钡能否做钡餐?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】同学们为进一步认知酸、碱、盐的化学性质,进行了如下图所示的实验,请你来参与他们的探究活动,并回答下列问题:

(1)当观察到甲试管中溶液由红色恰好变为无色时,说明二者恰好完全反应;该小组同学改变了药品滴加顺序对稀盐酸和氢氧化钠溶液发生中和反应进行了如下探究:用 传感器测得烧杯内溶液的
传感器测得烧杯内溶液的 变化图像(如图二),同时用温度传感器测得烧杯内温度变化图像(如图三),实验过程中保温良好,忽略热量散失。
变化图像(如图二),同时用温度传感器测得烧杯内温度变化图像(如图三),实验过程中保温良好,忽略热量散失。
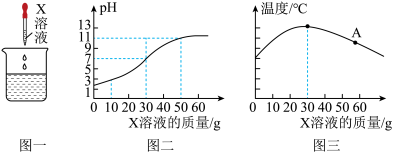
图三中A点对应溶液的溶质成分是______ (填写化学式)。
(2)乙试管中两种溶液不能发生反应,理由是______ ;
(3)实验结束后,同学们将乙、丙两支试管内的物质全部倒入同一个干净的小烧杯中,静置片刻,观察到白色沉淀明显增多。大家对得到的上层溶液的成分产生了兴趣,于是又进行了如下的实验探究。
【提出问题】小烧杯中上层溶液的溶质成分有哪些?
【做出猜想】猜想一:
猜想二: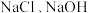
猜想三:______
【设计实验】
【反思拓展】
(4)小烧杯中的白色沉淀成分是______ (写化学式)。

(1)当观察到甲试管中溶液由红色恰好变为无色时,说明二者恰好完全反应;该小组同学改变了药品滴加顺序对稀盐酸和氢氧化钠溶液发生中和反应进行了如下探究:用
 传感器测得烧杯内溶液的
传感器测得烧杯内溶液的 变化图像(如图二),同时用温度传感器测得烧杯内温度变化图像(如图三),实验过程中保温良好,忽略热量散失。
变化图像(如图二),同时用温度传感器测得烧杯内温度变化图像(如图三),实验过程中保温良好,忽略热量散失。
图三中A点对应溶液的溶质成分是
(2)乙试管中两种溶液不能发生反应,理由是
(3)实验结束后,同学们将乙、丙两支试管内的物质全部倒入同一个干净的小烧杯中,静置片刻,观察到白色沉淀明显增多。大家对得到的上层溶液的成分产生了兴趣,于是又进行了如下的实验探究。
【提出问题】小烧杯中上层溶液的溶质成分有哪些?
【做出猜想】猜想一:

猜想二:
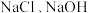
猜想三:
【设计实验】
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加过量稀盐酸 | 猜想一不成立 | |
另取少量溶液于试管中,滴加少量 | 有白色沉淀生产 | 猜想三成立 |
【反思拓展】
(4)小烧杯中的白色沉淀成分是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】金属锌在生产生活中有广泛应用。
Ⅰ、生活中人们常使用的“五号电池”属于锌锰电池,电池内部结构如图 1 所示。

[查阅资料] ①锌皮为金属锌(含有少量的铁)。
②黑色糊状填充物由炭黑、MnO2、ZnCl2、NH4Cl 等组成
③NH4Cl 和 ZnCl2的溶解度数据见下表:
按照图 2 所示实验回收黑色糊状填充物中的部分物质。
(1)溶液 A 中溶质主要有______ (填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者的分离,得到的固体 N 是______ (填化学式)。
(2)欲从固体 M 中得到较纯的 MnO2,操作Ⅲ可采用的方法是______ 。
Ⅱ、小明用纯锌粒和稀盐酸反应制取氢气时,发现加入 CuSO4溶液后,反应速率明显变大,于是他对此反应速率变大的原因进行了实验探究。
【猜想】①加入的 CuSO4溶液中的 使反应速率变大
使反应速率变大
②加入的 CuSO4溶液中的H2O 使反应速率变大
③加入的 CuSO4溶液中的 Cu2+使反应速率变大
④加入 CuSO4溶液后,______ 使反应速率变大。
小明经过思考,认为最不可能的原因是猜想②。
【实验验证】
用 a、b、c、d 四支试管取等质量且过量的纯锌粒,分别向试管中加入等体积等溶质质量分数的稀盐酸后,继续以下实验:
【结论】在锌与稀盐酸反应时,加入铜粉或______ 可加快反应速率。
Ⅲ、尝试定量探究实验
分别用 5 支烧杯各取该稀盐酸 50.00 g,加入锌粒。反应 4 小时后,发现烧杯中锌粒仍在冒气泡。相关数据如下表:
根据以上数据计算实验①参加反应的锌粒质量。______ (写出计算过程,结果精确到 0.01g)
若分别计算实验①②③④中参加反应的锌粒质量并分析计算结果,发现有明显偏差,其可能原因是______ 。
Ⅰ、生活中人们常使用的“五号电池”属于锌锰电池,电池内部结构如图 1 所示。

[查阅资料] ①锌皮为金属锌(含有少量的铁)。
②黑色糊状填充物由炭黑、MnO2、ZnCl2、NH4Cl 等组成
③NH4Cl 和 ZnCl2的溶解度数据见下表:
| 温度/C | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
(1)溶液 A 中溶质主要有
(2)欲从固体 M 中得到较纯的 MnO2,操作Ⅲ可采用的方法是
Ⅱ、小明用纯锌粒和稀盐酸反应制取氢气时,发现加入 CuSO4溶液后,反应速率明显变大,于是他对此反应速率变大的原因进行了实验探究。
【猜想】①加入的 CuSO4溶液中的
 使反应速率变大
使反应速率变大②加入的 CuSO4溶液中的H2O 使反应速率变大
③加入的 CuSO4溶液中的 Cu2+使反应速率变大
④加入 CuSO4溶液后,
小明经过思考,认为最不可能的原因是猜想②。
【实验验证】
用 a、b、c、d 四支试管取等质量且过量的纯锌粒,分别向试管中加入等体积等溶质质量分数的稀盐酸后,继续以下实验:
| 实验 | 现象 | 结论 |
| (1)向a试管中加入少量NaCl晶体 | 产生气泡速率不变 | |
| (2)向b试管中加入少量 | 产生气泡速率不变 | 猜想①不成立 |
| (3)向c试管中加入少量Cu粉 | 产生气泡速率明显变大 | 猜想 |
| (4)向d试管中加入少量Cu粉,立即再加入CuSO4粉末 | 产生气泡速率与c试管的速率几乎一样大 | 猜想 |
Ⅲ、尝试定量探究实验
分别用 5 支烧杯各取该稀盐酸 50.00 g,加入锌粒。反应 4 小时后,发现烧杯中锌粒仍在冒气泡。相关数据如下表:
| 平行实验 | ① | ② | ③ | ④ | ⑤ | |
| 反应前质量/g | 锌粒 | 5.75 | 5.77 | 5.79 | 5.77 | 5.75 |
| 烧杯 | 75.17 | 76.36 | 70.16 | 74.73 | 70.14 | |
| 反应4h后质量/g | 烧杯及烧杯内所有物质 | 128.96 | 130.13 | 123.99 | 128.51 | 123.93 |
若分别计算实验①②③④中参加反应的锌粒质量并分析计算结果,发现有明显偏差,其可能原因是
您最近一年使用:0次



