某同学在实验室制取氧气时,将29.5gKClO3和MnO2的混合物加热到质量不再变化为止,冷却后称量剩余固体的质量为19.9g,请通过计算回答:
(1)写出该反应的化学方程式______ ;
(2)生成氧气的质量为______ ;
(3)写出求解参加反应的KClO3质量(x)的比例式______ ;
(4)原混合物中二氧化锰的质量为______ ;
(5)剩余固体中KCl与MnO2的质量比为______ 。
(1)写出该反应的化学方程式
(2)生成氧气的质量为
(3)写出求解参加反应的KClO3质量(x)的比例式
(4)原混合物中二氧化锰的质量为
(5)剩余固体中KCl与MnO2的质量比为
18-19八年级下·黑龙江哈尔滨·期末 查看更多[3]
(已下线)5.3 利用化学方程式的简单计算(考点解读)-2023-2024学年九年级化学上册同步考点解读与专题训练(人教版)黑龙江省哈尔滨市松北区2022-2023学年八年级下学期期末化学试题黑龙江省哈尔滨市松北区(五四学制)2018-2019学年八年级下学期期末化学试题
更新时间:2021-08-12 23:25:12
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
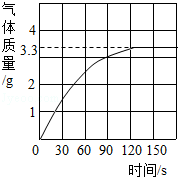
【推荐1】某兴趣小组利用过氧化氢溶液制取氧气。测得相关数据如下图所示:

(1)标出过氧化氢中氧元素的化合价_______ 。
(2)根据质量守恒定律,反应生成氧气的质量为_______ 。
(3)计算该过程中已经分解的过氧化氢的质量。(写出具体的解题步骤)

(1)标出过氧化氢中氧元素的化合价
(2)根据质量守恒定律,反应生成氧气的质量为
(3)计算该过程中已经分解的过氧化氢的质量。(写出具体的解题步骤)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组为测定某锌样品中Zn的质量分数,取10.0g锌样品于烧杯中,再逐滴加入稀H2SO4(杂质不与酸反应),待不再有气泡产生时停止滴加药品,共用去稀H2SO4的质量为200.0g。反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑。反应后测得烧杯中剩余物质的总质量为209.8g(假设生产的气体全部逃逸)。请计算:
(1)生成氢气的质量______ 。
(2)样品中Zn的质量分数______ 。
(1)生成氢气的质量
(2)样品中Zn的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2。某化学兴趣小组有一瓶500g规格的该生氧剂,兴趣小组同学取100g生氧剂放入装置A中,加入足量水使之充分反应,测定反应前后装置A、B的总质量。他们进行了三次实验,测定结果如下:
(1)KO2与水反应生成氢氧化钾和氧气,写出反应的化学方程式_______ 。
(2)100g生氧剂与水反应生成的氧气质量____ g;
(3)该瓶500g的生氧剂KO2的质量____ g。
(4)若去掉装置B,兴趣小组测得生氧剂中KO2的质量______ (填“偏大”“偏小”或“无影响同”)。
| 测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
| 反应前装置A、B总质量(g) | 400.1 | 400.2 | 399.7 | 400.0 |
| 反应后装置A、B总质量(g) | 376.1 | 376.1 | 375.8 | 376.0 |

(1)KO2与水反应生成氢氧化钾和氧气,写出反应的化学方程式
(2)100g生氧剂与水反应生成的氧气质量
(3)该瓶500g的生氧剂KO2的质量
(4)若去掉装置B,兴趣小组测得生氧剂中KO2的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为测定某种贝壳中碳酸钙的质量分数,取12.5g贝壳,逐滴加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应也不溶于水)。请计算:

(1)12.5g这种贝壳中碳酸钙的质量是_____ g。
(2)所用稀盐酸中溶质的质量分数。

(1)12.5g这种贝壳中碳酸钙的质量是
(2)所用稀盐酸中溶质的质量分数。
您最近一年使用:0次