已知A、B、C、D为初中常见的物质,相互之间的关系如图所示(“一”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去)。若A是一种酸,下列说法中,不正确的是


| A.B、C、D可能都是金属单质 | B.B、C可能都是碳酸盐 |
| C.A、D也可能发生反应 | D.D一定不能转化为C |
更新时间:2021-08-15 19:14:48
|
相似题推荐
填空与简答-推断题
|
困难
(0.15)
【推荐1】有一包固体粉末,可能含有镁粉、碳粉、氧化铜、硫酸钾、氢氧化钠中的一种或几种。
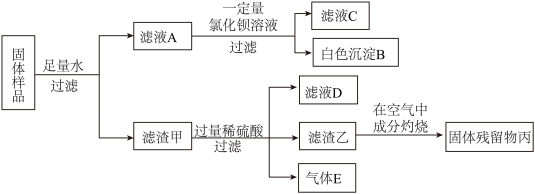
(1)实验中生成白色沉淀B的化学方程式是_______ 。
(2)实验结束后,该小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,则滤液C中一定含有的阳离子有______ (填离子符号)。
(3)测得滤渣乙的质量等于固体残留物丙的质量,由此同学推测出滤渣乙在空气中灼烧时还生成了另外一种物质,通过计算可知该物质与固体残留物丙的质量比为______ 。
(4)综合以上分析可知,原固体混合物中一定含有的物质为_______ 。

(1)实验中生成白色沉淀B的化学方程式是
(2)实验结束后,该小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,则滤液C中一定含有的阳离子有
(3)测得滤渣乙的质量等于固体残留物丙的质量,由此同学推测出滤渣乙在空气中灼烧时还生成了另外一种物质,通过计算可知该物质与固体残留物丙的质量比为
(4)综合以上分析可知,原固体混合物中一定含有的物质为
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐2】浩瀚大海给我们提供很多资源,海水中含有大量氯化钠,工业上可以用氯化钠原料来制取碳酸钠、氢氧化钠、氯气和盐酸等。
(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH_____ (填“<”、“=”或“>”)7。写出碳酸钠与石灰乳反应制备烧碱的化学方程式
_______________________________ 。
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是________________ 。
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
①进行实验a和b的目的是_______________________________________________________ 。
②搅拌速率越快,反应时间越长则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是________ (填选项)。
A.200r/min,3.5h B. 200r/min,4.5h C.175 r/min,4h D. 225 r/min,4h
(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是
A.铁锈锈渍 B.用碳粉还原氧化铜附着的红色固体
C.长时间盛放石灰水留下的白色固体 D.氢氧化钠和硫酸铜反应后的留下的蓝色固体
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度r/min | 反应时间/h | 钙除去率/% |
a | 1.78 | 200 | 3 | 44.8 |
b | 2.32 | 200 | 3 | 60.2 |
c | 2.32 | 125 | 4 | 55.1 |
d | 2.32 | 200 | 4 | 64.6 |
②搅拌速率越快,反应时间越长则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是
A.200r/min,3.5h B. 200r/min,4.5h C.175 r/min,4h D. 225 r/min,4h
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
名校
解题方法
【推荐3】纳米( 米)铁红(
米)铁红( )常用作油漆、粉末冶金的原料等。工业上可用硫铁矿烧渣(主要含有
)常用作油漆、粉末冶金的原料等。工业上可用硫铁矿烧渣(主要含有 、
、 、
、 等)为原料分步制备纳米铁红。
等)为原料分步制备纳米铁红。
【资料卡片】FeO化学性质不稳定,易被氧化生成 或
或 。
。
【处理烧渣】硫铁矿烧渣经过还原焙烧、酸浸、水浴除杂等操作得到含酸的 溶液。
溶液。
(1)还原焙烧是将硫铁矿烧渣和一定量的褐煤经过高温焙烧,生成FeO。 转化率(
转化率( 转化率=
转化率=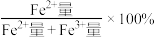 )受焙烧温度及焙烧时间的影响如图-1及图-2所示,分析图像可知:最佳焙烧温度为
)受焙烧温度及焙烧时间的影响如图-1及图-2所示,分析图像可知:最佳焙烧温度为_____ ℃,焙烧时间最好为_____ min,延长焙烧时间, 转化率降低的原因可能是
转化率降低的原因可能是_____ 。 和FeO反应,反应的化学方程式为
和FeO反应,反应的化学方程式为_____ ,属于_____ 反应(填基本反应类型)。
【制备铁红】将处理后的含酸溶液经一系列操作可得纳米铁红,流程如下图所示。 可将
可将 氧化成
氧化成 。稀释煮沸时,发生的反应主要有:
。稀释煮沸时,发生的反应主要有: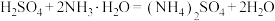 和
和_____ 。
(4)操作Ⅰ的名称_____ ,操作Ⅰ所得溶液中的溶质在农业上可作_____ 。。
(5)水洗时,为验证 是否洗净,最好选用_____(填字母序号)。
是否洗净,最好选用_____(填字母序号)。
(6)沸腾回流时, 受热脱水生成纳米级
受热脱水生成纳米级 。用离心机分离出
。用离心机分离出 ,而不是过滤的原因是
,而不是过滤的原因是_____ 。
(7)pH为7时,产品中会混入FeOOH,令使产品中铁元素的质量分数_____ (填“偏大”或“偏小”)。
(8)用200吨含铁元素42%的硫铁矿渣制备铁红,假设铁元素无损失,理论上能制得纳米
_____ 吨。
 米)铁红(
米)铁红( )常用作油漆、粉末冶金的原料等。工业上可用硫铁矿烧渣(主要含有
)常用作油漆、粉末冶金的原料等。工业上可用硫铁矿烧渣(主要含有 、
、 、
、 等)为原料分步制备纳米铁红。
等)为原料分步制备纳米铁红。【资料卡片】FeO化学性质不稳定,易被氧化生成
 或
或 。
。【处理烧渣】硫铁矿烧渣经过还原焙烧、酸浸、水浴除杂等操作得到含酸的
 溶液。
溶液。(1)还原焙烧是将硫铁矿烧渣和一定量的褐煤经过高温焙烧,生成FeO。
 转化率(
转化率( 转化率=
转化率=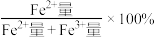 )受焙烧温度及焙烧时间的影响如图-1及图-2所示,分析图像可知:最佳焙烧温度为
)受焙烧温度及焙烧时间的影响如图-1及图-2所示,分析图像可知:最佳焙烧温度为 转化率降低的原因可能是
转化率降低的原因可能是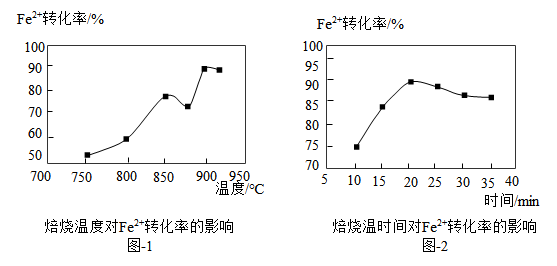
 和FeO反应,反应的化学方程式为
和FeO反应,反应的化学方程式为【制备铁红】将处理后的含酸溶液经一系列操作可得纳米铁红,流程如下图所示。
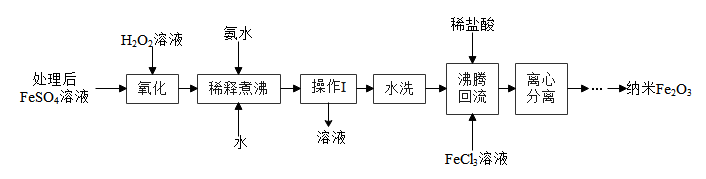
 可将
可将 氧化成
氧化成 。稀释煮沸时,发生的反应主要有:
。稀释煮沸时,发生的反应主要有: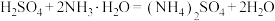 和
和(4)操作Ⅰ的名称
(5)水洗时,为验证
 是否洗净,最好选用_____(填字母序号)。
是否洗净,最好选用_____(填字母序号)。| A.NaOH溶液和湿润的红色石蕊试纸 | B.BaCl2溶液 | C.AgNO3溶液 |
 受热脱水生成纳米级
受热脱水生成纳米级 。用离心机分离出
。用离心机分离出 ,而不是过滤的原因是
,而不是过滤的原因是(7)pH为7时,产品中会混入FeOOH,令使产品中铁元素的质量分数
(8)用200吨含铁元素42%的硫铁矿渣制备铁红,假设铁元素无损失,理论上能制得纳米

您最近一年使用:0次
【推荐1】二氧化碳捕集和资源化利用是碳中和领域研究热点。
碳捕集:捕捉烟气CO2,将其再释出可实现资源化利用,相关物质转化如下:

(1)“颗粒反应室”中反应的化学方程式为___________ 。
(2)上述流程中可循环使用的物质有___________ (填化学式)。
碳的资源化利用 中国科学家已实现由CO2到淀粉的全人工合成,主要过程如下:

(3)检验淀粉的常用试剂是___________ (填名称)。
(4)绿色植物实现CO2到葡萄糖的转化过程称为___________ 。
(5)阶段I反应的微观过程如图1所示。写出甲醇的化学式:___________ 。

(6)阶段Ⅱ的物质转化如图2所示。反应a中四种物质的化学计量数均为1。
①推测分子中氢原子数目:甲醇___________ 甲醛(填“>”、“<”或“=”)。
②为使甲醇持续转化为甲醛,反应b需补充H2O2.理论上需补充的H2O2与反应a中生成的H2O2的分子个数比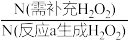 ≥
≥___________ 。
碳捕集:捕捉烟气CO2,将其再释出可实现资源化利用,相关物质转化如下:

(1)“颗粒反应室”中反应的化学方程式为
(2)上述流程中可循环使用的物质有
碳的资源化利用 中国科学家已实现由CO2到淀粉的全人工合成,主要过程如下:

(3)检验淀粉的常用试剂是
(4)绿色植物实现CO2到葡萄糖的转化过程称为
(5)阶段I反应的微观过程如图1所示。写出甲醇的化学式:

(6)阶段Ⅱ的物质转化如图2所示。反应a中四种物质的化学计量数均为1。
①推测分子中氢原子数目:甲醇
②为使甲醇持续转化为甲醛,反应b需补充H2O2.理论上需补充的H2O2与反应a中生成的H2O2的分子个数比
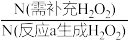 ≥
≥
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐2】现有一白色固体混合物,可能由BaCl2、KOH、KNO3、MgCl2、CuSO4中的几种混合而成。为证明其组成,做如下实验:
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色液体。过滤得白色沉淀①和无色滤液①。则原混合物一定含有_________ ,一定不含有_________ 。
(2)向无色滤液①中加入KOH溶液,无任何现象,再加入过量的某可溶性碳酸盐溶液,充分反应后过滤,得白色沉淀②,无色滤液②,则原混合物中一定还含有_________ 。
(3)向无色滤液②中加入过量的盐酸,然后将所得的液体蒸干,得到固体A。如果固体A中只含有2种元素,A为_________ ,则加入的碳酸盐溶液是_________ ,如果固体A中含有两种金属元素,则加入的碳酸盐溶液是_________ 。
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色液体。过滤得白色沉淀①和无色滤液①。则原混合物一定含有
(2)向无色滤液①中加入KOH溶液,无任何现象,再加入过量的某可溶性碳酸盐溶液,充分反应后过滤,得白色沉淀②,无色滤液②,则原混合物中一定还含有
(3)向无色滤液②中加入过量的盐酸,然后将所得的液体蒸干,得到固体A。如果固体A中只含有2种元素,A为
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐3】某校实验室有一包固体粉末可能由NH4Cl、Na2CO3、Ba(OH)2、BaCl2、Na2SO4中的一种或几种组成。为了确定其组成,某化学兴趣小组做了以下实验:

已知,步骤1中无明显现象。
请回答下列问题:
(1)溶液D呈 性(酸、碱、中),原固体中一定不存在的物质是_______ 。
(2)白色沉淀A全部溶解的化学方程式为_______ 。
(3)步骤4所得红色溶液D中除指示剂外一定含有的溶质是_______ 。
(4)该实验小组实验结束后处理废液时,将无色溶液B、无色溶液F和沉淀E倒在了同一个废液缸里,发现沉淀消失并产生气泡,则废液缸中最终得到的废液中除指示剂外一定含有的离子是____ 。

已知,步骤1中无明显现象。
请回答下列问题:
(1)溶液D呈 性(酸、碱、中),原固体中一定不存在的物质是
(2)白色沉淀A全部溶解的化学方程式为
(3)步骤4所得红色溶液D中除指示剂外一定含有的溶质是
(4)该实验小组实验结束后处理废液时,将无色溶液B、无色溶液F和沉淀E倒在了同一个废液缸里,发现沉淀消失并产生气泡,则废液缸中最终得到的废液中除指示剂外一定含有的离子是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
【推荐1】某化学兴趣小组从某化工厂排污国取得有色废水样品A,并通过如下实验回收处理。其中固体E经测定是一种具有固定熔点和沸点的复合肥料。请根据图示回答:
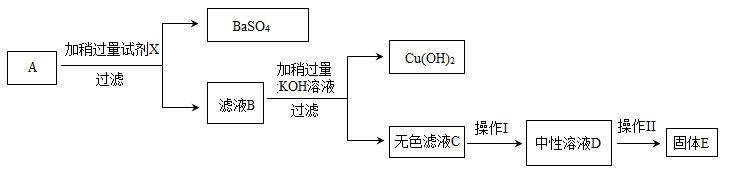
(1)操作Ⅰ的实验步骤是______________ ,反应的化学方程式是__________ 。
(2)操作Ⅱ所需的仪器有_____________ ,得到的固体E是___________ 。
(3)废水样品A中一定含有的溶质是____________ ,可能含有的溶质有____________ 、____________ 、____________ (至少写出三种),此时选择的试剂X为____________ 。
(4)若X选择其他试剂,操作流程和实验现象不变,实验后测得性溶液D中含有两种不同的酸根离子,则此时选择的试剂X为____________ 。

(1)操作Ⅰ的实验步骤是
(2)操作Ⅱ所需的仪器有
(3)废水样品A中一定含有的溶质是
(4)若X选择其他试剂,操作流程和实验现象不变,实验后测得性溶液D中含有两种不同的酸根离子,则此时选择的试剂X为
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐2】有一包白色粉末,可能含有硫酸铜、硫酸钡、碳酸钾、氯化铵和氢氧化钡中的一种或几种。取少量粉末加氢氧化钠溶液共热,无明显现象;另取一定量该粉末加入到盛有足量水的烧杯中,搅拌,静置,观察到烧杯中有白色沉淀和无色溶液。
小明同学认为,白色粉末中一定含有硫酸钡;
小意同学认为小明的结论不准确;
针对上述两位同学的观点,小燕同学进一步设计如图实验方案进行探究:

(1)白色固体中一定不含有_______ (填化学式,下同);
(2)步骤③中,加入酚酞溶液后,若溶液E为无色,则原白色粉末的组成是________ ;步骤③中,加入酚酞溶液后,若溶液E为红色,则滤液A中一定含有的溶质是________ ,原白色粉末的可能组成是______ 或_______ ;
(3)小鹏同学认为,只需取少量滤渣B,加入过量的稀硝酸,若看到的现象是______ ,就足以说明原白色粉末中只含有碳酸钾和氢氧化钡。
小明同学认为,白色粉末中一定含有硫酸钡;
小意同学认为小明的结论不准确;
针对上述两位同学的观点,小燕同学进一步设计如图实验方案进行探究:

(1)白色固体中一定不含有
(2)步骤③中,加入酚酞溶液后,若溶液E为无色,则原白色粉末的组成是
(3)小鹏同学认为,只需取少量滤渣B,加入过量的稀硝酸,若看到的现象是
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐1】有一包粉末,已知由CaCO3、BaCl2、FeCl3、NH4Cl、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀、无色气体M和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如图所示的实验。

请回答下列问题:
(1)无色气体M的化学式_______ ,白色沉淀B的化学式_______ 。
(2)A中一定存在的溶质的化学式是_______ 。
(3)生成白色沉淀D的化学方程式是_______ 。
(4)这包粉末中一定含有的物质是_______ ,一定不存在的物质是_______ ,理由是_______ 。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀、无色气体M和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如图所示的实验。

请回答下列问题:
(1)无色气体M的化学式
(2)A中一定存在的溶质的化学式是
(3)生成白色沉淀D的化学方程式是
(4)这包粉末中一定含有的物质是
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐2】如图所示A为黑色固体,D是红色的金属单质,C是一种蓝色沉淀,B为硫酸盐,E、F为硝酸盐,且F的溶液呈蓝色。各物质间的转化均一步实现。

(1)写出物质C、B、G的化学式:C_____ ,B____ ,G_____ 。
(2)写出A→B的化学反应方程式:_______________ 。
(3)B→C属于_______ 反应(填基本反应类型)。

(1)写出物质C、B、G的化学式:C
(2)写出A→B的化学反应方程式:
(3)B→C属于
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐3】如图所示,A~H是初中化学常见的物质。A俗称纯碱;C可用作补钙剂;G是一种常见的氮肥,含氮量为35%;H、F物质类别相同。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去:

(1)写出B的化学式:_______ 。
(2)若E与G的组成元素相同,则C与E反应的化学方程式为_______ 。
(3)有一包白色粉末,可能由上述物质中的C和CuSO4、BaCl2、NaCl、Na2SO4、(NH4)2CO3中的一种或几种组成,为证明其组成进行如下实验:
步骤一:取少量白色粉末,向其中加入足量水,充分搅碎后过滤,得到白色沉淀和无色滤液。
步骤二:向步骤一中滤出的白色沉淀中加入足量的盐酸,沉淀部分溶解,并产生无色气体。
步骤三:向步骤二所得滤液中加入足量的氢氧化钠溶液,有刺激性气味气体放出。
①固体混合物的组成可能有______ 种。
②向步骤三后的溶液中加入稀硝酸酸化,再加入足量的硝酸钡,发现没有沉淀产生,然后加入硝酸银溶液,出现了白色沉淀,小明同学由此得出原混合物中一定含有氯化钠,小丽同学否定了小明的判断,她的理由是_________ 。

(1)写出B的化学式:
(2)若E与G的组成元素相同,则C与E反应的化学方程式为
(3)有一包白色粉末,可能由上述物质中的C和CuSO4、BaCl2、NaCl、Na2SO4、(NH4)2CO3中的一种或几种组成,为证明其组成进行如下实验:
步骤一:取少量白色粉末,向其中加入足量水,充分搅碎后过滤,得到白色沉淀和无色滤液。
步骤二:向步骤一中滤出的白色沉淀中加入足量的盐酸,沉淀部分溶解,并产生无色气体。
步骤三:向步骤二所得滤液中加入足量的氢氧化钠溶液,有刺激性气味气体放出。
①固体混合物的组成可能有
②向步骤三后的溶液中加入稀硝酸酸化,再加入足量的硝酸钡,发现没有沉淀产生,然后加入硝酸银溶液,出现了白色沉淀,小明同学由此得出原混合物中一定含有氯化钠,小丽同学否定了小明的判断,她的理由是
您最近一年使用:0次




