某兴趣小组同学利用数字化实验探究了酸、碱、盐的部分性质。
【实验一】探究酸碱中和反应。实验开始后将注射器内的液体逐滴注入烧瓶内。
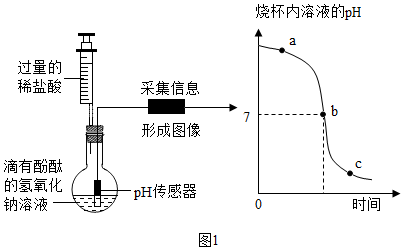
(1)盐酸和氢氧化钠反应的化学方程式为______ ;
(2)c点所示溶液加热蒸干所得固体是_____ (填化学式);
(3)能说明盐酸和氢氧化钠发生化学反应的现象是:
①溶液的颜色从红色变为无色;
②溶液的pH____ :
【实验二】探究NaOH和CO2的反应。
用下图装置进行实验,a点时推入NaOH溶液,b点时推入稀盐酸。瓶内压强变化如下图所示:
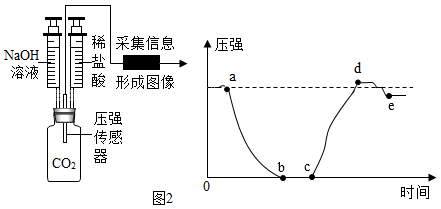
(4)b点的溶质为__ ;
(5)cd段对应反应的化学方程式_____ ;
(6)e点的压强小于a点可能的原因是______ ;
(7)若氢氧化钠溶液中含有酚酞,则图中______ 点时溶液从红色变为无色;
(8)若集气瓶中的CO2共0.88g,要将其完全吸收至少需要溶质质量分数为10%的NaOH溶液多少g?______ (写出计算过程)
【实验一】探究酸碱中和反应。实验开始后将注射器内的液体逐滴注入烧瓶内。

(1)盐酸和氢氧化钠反应的化学方程式为
(2)c点所示溶液加热蒸干所得固体是
(3)能说明盐酸和氢氧化钠发生化学反应的现象是:
①溶液的颜色从红色变为无色;
②溶液的pH
【实验二】探究NaOH和CO2的反应。
用下图装置进行实验,a点时推入NaOH溶液,b点时推入稀盐酸。瓶内压强变化如下图所示:

(4)b点的溶质为
(5)cd段对应反应的化学方程式
(6)e点的压强小于a点可能的原因是
(7)若氢氧化钠溶液中含有酚酞,则图中
(8)若集气瓶中的CO2共0.88g,要将其完全吸收至少需要溶质质量分数为10%的NaOH溶液多少g?
更新时间:2021-08-22 19:30:30
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】无明显现象反应的可视化是一项重要的课题。
(1)某化学研究小组以“探究CO2与NaOH是否反应”为主题展开化学反应可视化研究,设计了如下两个实验。
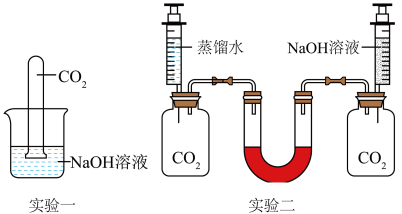
实验一:将一支充满CO2的试管倒扣在盛有NaOH溶液的烧杯中,观察试管中的液面变化情况。
实验二:向两个装湖CO2的同样规格的瓶中分别注入等体积的蒸水和NaOH溶液,充分反应后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况。
试回答下列问题:
①在实验中,需要提前配制NaOH溶液并制备CO2。配制NaOH溶液时,若不慎将氢氧化钠沾到皮肤上,应立即用大量水冲洗,然后涂______ (填“碳酸氢钠”“硼酸”“硫酸”之一)溶液;实验室用石灰石和稀盐酸制备CO2的化学方程式为______ 。
②实验二中若观察到U型管______ (填“左”或“右”)端液面升高,则证明溶液中的NaOH与CO2发生了化学反应。
③与实验一相比,小组同学认为实验二更合理,因为它排除了______ (填化学式)对实验的干扰。
(2)为测定某Na2CO3溶液的溶质质量分数,某小组同学取100g该溶液,向其中逐滴加入溶质质量分数为17.1%的Ba(OH)2溶液,反应中生成沉淀的质量与加入Ba(OH)2溶液的质量关系如图所示。
试回答:
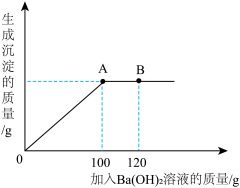
①当加入Ba(OH)2溶液120g时(即B点),所得溶液中一定存在的溶质是______ (填化学式)。
②当加入Ba(OH)2溶液100g时(即A点),恰好完全反应。试通过计算,求所取Na2CO3溶液的溶质质量分数______ 。(计算结果精确至0.1%)
(1)某化学研究小组以“探究CO2与NaOH是否反应”为主题展开化学反应可视化研究,设计了如下两个实验。

实验一:将一支充满CO2的试管倒扣在盛有NaOH溶液的烧杯中,观察试管中的液面变化情况。
实验二:向两个装湖CO2的同样规格的瓶中分别注入等体积的蒸水和NaOH溶液,充分反应后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况。
试回答下列问题:
①在实验中,需要提前配制NaOH溶液并制备CO2。配制NaOH溶液时,若不慎将氢氧化钠沾到皮肤上,应立即用大量水冲洗,然后涂
②实验二中若观察到U型管
③与实验一相比,小组同学认为实验二更合理,因为它排除了
(2)为测定某Na2CO3溶液的溶质质量分数,某小组同学取100g该溶液,向其中逐滴加入溶质质量分数为17.1%的Ba(OH)2溶液,反应中生成沉淀的质量与加入Ba(OH)2溶液的质量关系如图所示。
试回答:

①当加入Ba(OH)2溶液120g时(即B点),所得溶液中一定存在的溶质是
②当加入Ba(OH)2溶液100g时(即A点),恰好完全反应。试通过计算,求所取Na2CO3溶液的溶质质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】化学是一门以实验为基础的科学实验室,选用以下装置制取CO2。

(1)A中反应的化学方程式为___________ ;A装置还可以用于实验室制取其他气体,有关反应的化学方程式为___________ 。
(2)若将A,B连接,A中产生的气体并不能使B中的溶液变浑浊,请写出原因:___________ 。
(3)实验室要制备并收集纯净干燥的二氧化碳气体,所选装置接口的连接顺序为:a接___________ 、___________ 接___________ 、___________ 接___________ 。
(4)相比下图中的G装置,A装置的优点是___________ ;为了解装置具有该优点的原因,在装置A中连接压强传感器(如图H),从而测定实验中试管内气体压强变化的情况(如图L)。ab段试管中液面逐渐___________ (填“上升”或“下降”),c点对应的操作是___________ 。

(5)现有硫酸和硫酸铜的混合溶液100g,向其中不断加入10%的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液质量的变化关系如图所示。图中m的数值是_______


(1)A中反应的化学方程式为
(2)若将A,B连接,A中产生的气体并不能使B中的溶液变浑浊,请写出原因:
(3)实验室要制备并收集纯净干燥的二氧化碳气体,所选装置接口的连接顺序为:a接
(4)相比下图中的G装置,A装置的优点是

(5)现有硫酸和硫酸铜的混合溶液100g,向其中不断加入10%的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液质量的变化关系如图所示。图中m的数值是

您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】海洋是巨大的资源宝库、国防金属——镁,就是利用海水制取的。工业上从海水中提取单质镁的过程如下图所示:
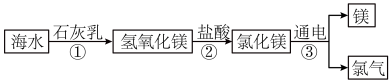
(1)在上述转化过程中发生中和反应的步骤是_____________ (填序号)。
(2)海水中本身就含有氯化镁,请分析①、②两步再得到氯化镁的目的是__________________________ 。
(3)小明同学在实验室中用NaOH溶液替代石灰乳模拟生产过程中的第①步,他取NaCl和MgCl2的固体混合物25g,加入适量水完全溶解后,与溶质质量分数为20%的NaOH溶液混合充分反应,记录生成的沉淀与加入NaOH溶液质量关系如图所示:
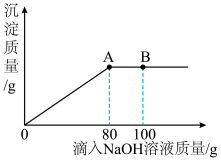
①当滴入上述NaOH溶液至图中B点时,烧杯中溶液里含有的溶质为_______________ (写化学式)。
②当滴入上述NaOH溶液80g时,试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量_______________ (计算结果精确至0.1g)。

(1)在上述转化过程中发生中和反应的步骤是
(2)海水中本身就含有氯化镁,请分析①、②两步再得到氯化镁的目的是
(3)小明同学在实验室中用NaOH溶液替代石灰乳模拟生产过程中的第①步,他取NaCl和MgCl2的固体混合物25g,加入适量水完全溶解后,与溶质质量分数为20%的NaOH溶液混合充分反应,记录生成的沉淀与加入NaOH溶液质量关系如图所示:

①当滴入上述NaOH溶液至图中B点时,烧杯中溶液里含有的溶质为
②当滴入上述NaOH溶液80g时,试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】酸、碱、盐是我们身边重要的化合物。请根据所学知识回答相关问题:
(1)稀硫酸和盐酸具有相似化学性质的原因是它们的水溶液中都含有__________ (写离子符号)。
(2)图中的气球是“魔幻可变气球”。实验前,将某固体X放入广口瓶中,分液漏斗M、N中分别装有一定量的液体药品,若打开M的开关,液体药品流下,气球变瘪,则固体X和M中的液体药品组合可以是_________ (答一种组合即可,下同);若打开N的开关,液体药品流下,气球变大,则固体X和N中的液体药品组合可以是__________ 。

(3)如图是氢氧化钠溶液与稀硫酸反应时溶液pH变化的示意图。

①根据图示判断,该实验是将__________ (填“氢氧化钠溶液”或“稀硫酸”)加入到另一种溶液中。
②当加入溶液的质量为bg时,所得溶液中的溶质是__________ 。(写化学式)
(4)某兴趣小组的同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,每次充分反应后,测得的相关实验数据如表所示:
①表格中m的值为__________ 。
②计算恰好完全反应时所得溶液的溶质的质量分数(写出必要的计算过程)__________ 。
(1)稀硫酸和盐酸具有相似化学性质的原因是它们的水溶液中都含有
(2)图中的气球是“魔幻可变气球”。实验前,将某固体X放入广口瓶中,分液漏斗M、N中分别装有一定量的液体药品,若打开M的开关,液体药品流下,气球变瘪,则固体X和M中的液体药品组合可以是

(3)如图是氢氧化钠溶液与稀硫酸反应时溶液pH变化的示意图。

①根据图示判断,该实验是将
②当加入溶液的质量为bg时,所得溶液中的溶质是
(4)某兴趣小组的同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,每次充分反应后,测得的相关实验数据如表所示:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 氢氧化钠溶液的质量/g | 20 | 20 | 20 | 20 | 20 |
| 所得沉淀质量/g | 4.9 | 9.8 | 14.7 | m | 19.6 |
②计算恰好完全反应时所得溶液的溶质的质量分数(写出必要的计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】通过化学学习,同学们发现有些化学反应发生时没有明显的现象,为了证明这些化学反应的发生,某化学课外小组设计了以下探究实验:

实验一 二氧化碳和水反应
(1)实验一的图示装置中,①③为喷水的石蕊试纸,②为干燥的石蕊试纸,通入二氧化碳后,首先观察到___________ (填序号)试纸先变红。
实验二 二氧化碳和氢氧化钠溶液反应
(2)向二氧化碳和氢氧化钠溶液反应后的溶液中滴加稀盐酸,观察到有___________ 产生,说明两者发生了反应,写出二氧化碳和氢氧化钠溶液反应的化学方程式:___________ 。
(3)小明认为通过压强变化也可以证明二氧化碳和氢氧化钠溶液发生了反应,设计了如图所示的实验二装置,可观察到U形管内___________ (填“左”或“右”)端液面升高。
实验三 氢氧化钠溶液和稀硫酸反应
(4)课外活动小组同学做该实验时,忘记滴入的是哪种溶液,利用pH传感器测得溶液pH的变化如实验三图2所示。根据图像可判断出滴入的溶液是______ ,在c点时,溶液中的溶质是______ 。
(5)该反应的实质是___________ 。
(6)化学活动小组记录的数据如下表所示,计算:烧杯中原溶液的溶质质量分数。

实验一 二氧化碳和水反应
(1)实验一的图示装置中,①③为喷水的石蕊试纸,②为干燥的石蕊试纸,通入二氧化碳后,首先观察到
实验二 二氧化碳和氢氧化钠溶液反应
(2)向二氧化碳和氢氧化钠溶液反应后的溶液中滴加稀盐酸,观察到有
(3)小明认为通过压强变化也可以证明二氧化碳和氢氧化钠溶液发生了反应,设计了如图所示的实验二装置,可观察到U形管内
实验三 氢氧化钠溶液和稀硫酸反应
(4)课外活动小组同学做该实验时,忘记滴入的是哪种溶液,利用pH传感器测得溶液pH的变化如实验三图2所示。根据图像可判断出滴入的溶液是
(5)该反应的实质是
(6)化学活动小组记录的数据如下表所示,计算:烧杯中原溶液的溶质质量分数。
| 原溶液的质量 | pH为7时滴入溶液的质量 | 滴入溶液的溶质质量分数 |
| 100g | 100g | 9.8% |
您最近一年使用:0次
【推荐3】(I)下图是小红同学设计的一组“吹气球”的实验。请回答:

(1)甲装置中,向a中加水会看到气球胀大,一段时间内观察到___ ,说明该装置气密性良好。
(2)乙装置中,若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是___ 。
(3)丙装置中,若锥形瓶中盛满CO2,欲使气球胀大,分液漏斗中的液体可以是___ 。
(II)实验室配制50g16%的氯化钠溶液的操作如下图所示。
①中玻璃棒的作用是__ ;称量的食盐质量为__ ;该实验的正确操作顺序为____ (填序号)。

(Ⅲ)某实验小组利用下图所示装置进行研究CO2性质和燃烧条件的实验。

(1)研究CO2与水反应:进行此实验时,将C装置a、b两端分别与B、D装置连接,A中液体为紫色石蕊溶液,B中固体为碳酸钠,C中液体为浓硫酸,D中放一朵干燥的紫色石蕊小花。将分液漏斗中的稀硫酸滴入B中。A中发生反应的化学方程式为____ ;观察到____ ,说明使紫色石蕊变色的是碳酸、不是CO2。
(2)研究燃烧的条件:进行此实验时,将C装置b、a两端分别与B、 D装置连接,A和C的液体底部靠近导管口分别固定一小块白磷,B中固体为二氧化锰。将分液漏斗中的液体滴入B中。B中发生反应的化学方程式为____ ;A液体为冷水,C中液体为热水;观察到____ ,说明可燃物燃烧需要与氧气接触、温度达到着火点。

(1)甲装置中,向a中加水会看到气球胀大,一段时间内观察到
(2)乙装置中,若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是
(3)丙装置中,若锥形瓶中盛满CO2,欲使气球胀大,分液漏斗中的液体可以是
(II)实验室配制50g16%的氯化钠溶液的操作如下图所示。
①中玻璃棒的作用是

(Ⅲ)某实验小组利用下图所示装置进行研究CO2性质和燃烧条件的实验。

(1)研究CO2与水反应:进行此实验时,将C装置a、b两端分别与B、D装置连接,A中液体为紫色石蕊溶液,B中固体为碳酸钠,C中液体为浓硫酸,D中放一朵干燥的紫色石蕊小花。将分液漏斗中的稀硫酸滴入B中。A中发生反应的化学方程式为
(2)研究燃烧的条件:进行此实验时,将C装置b、a两端分别与B、 D装置连接,A和C的液体底部靠近导管口分别固定一小块白磷,B中固体为二氧化锰。将分液漏斗中的液体滴入B中。B中发生反应的化学方程式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】实验室有一瓶标签模糊的烧碱溶液,小杰设计实验测定了其溶质质量分数。请根据下图所示的实验过程和提供的数据进行分析和计算。(注:滴入酚酞试液的质量忽略不计)

(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好________________ 时,停止滴液。反应所消耗稀盐酸的质量为_______ g。
(2)通过计算确定该瓶烧碱溶液的溶质质量分数。(写出计算步骤)________
(3)问题讨论:小红做同样的实验得到的结果比小杰得到的结果偏小,从实验操作的角度分析产生这种误差的原因可能是_______________________ (填写一条即可)。

(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好
(2)通过计算确定该瓶烧碱溶液的溶质质量分数。(写出计算步骤)
(3)问题讨论:小红做同样的实验得到的结果比小杰得到的结果偏小,从实验操作的角度分析产生这种误差的原因可能是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】初中化学兴趣小组用稀盐酸处理工业废水中的氢氧化钠。取100g工业废水于烧杯中,逐滴加入溶质质量分数为3.65%的稀盐酸,利用pH传感器和温度传感器记录反应过程相关物理量的变化情况,如图所示:

(1)分析温度曲线,推测该反应为______ 反应(选填“放热”或“吸热”)。
(2)观察pH曲线,当实验进行到点时______ (选填“A”或“B”),盐酸和氢氧化钠恰好完全反应,消耗稀盐酸20g。请计算:工业废水中氢氧化钠的质量分数。______ (写出计算过程)
(3)下列为市面上浓盐酸和浓硫酸的相关数据:
某工厂每天用硫酸处理100吨上述工业废水大约需要花费600元,请通过计算,你会建议该工厂购买(选填“浓盐酸”或“浓硫酸”)______ 更划算。

(1)分析温度曲线,推测该反应为
(2)观察pH曲线,当实验进行到点时
(3)下列为市面上浓盐酸和浓硫酸的相关数据:
| 商品 | 纯度 | 价格(元/吨) |
| 浓盐酸 | 36.5% | 400 |
| 浓硫酸 | 98% | 600 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】某化学兴趣小组利用图1研究稀盐酸与氢氧化钠溶液反应的过程,利用pH和温度传感器测量反应过程中相关量的变化,得图2和图3。

(1)图2中b点所示溶液中的溶质是__________ 。(写化学式)
(2)取图2中d点所示溶液,滴加紫色石蕊试液,观察到的现象是__________ 。
(3)图3中V的数值最接近_________ (填“5”、“10”或“12.5”),图3中溶液温度发生变化的原因是_________ 。
(4)若向8g氢氧化钠溶液中加入溶质质量分数为7.3%的稀盐酸10g,恰好完全反应。试计算氢氧化钠溶液的溶质质量分数。______

(1)图2中b点所示溶液中的溶质是
(2)取图2中d点所示溶液,滴加紫色石蕊试液,观察到的现象是
(3)图3中V的数值最接近
(4)若向8g氢氧化钠溶液中加入溶质质量分数为7.3%的稀盐酸10g,恰好完全反应。试计算氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】为了探究敞口放置的氢氧化钠固体变质情况,取少量固体配制成溶液,进行如下实验。(已知BaCl2溶液呈中性)

(1)在试管①中滴加足量BaCl2溶液目的是______ 。若氢氧化钠部分变质,图甲试管④中可观察到______ 。
(2)为了进一步确定该氢氧化钠变质程度,取10g样品进行如图乙的实验,测得的相关数据如表格所示。请计算该样品中氢氧化钠的质量分数。
(3)下列情况会造成样品中氢氧化钠的质量分数比实际数据偏小的有______。

(1)在试管①中滴加足量BaCl2溶液目的是
(2)为了进一步确定该氢氧化钠变质程度,取10g样品进行如图乙的实验,测得的相关数据如表格所示。请计算该样品中氢氧化钠的质量分数。
| 样品质量(克) | 装有氢氧化钠溶液的广口瓶质量(克) | |
| 反应前 | 反应后 | |
| 10 | 200 | 202.2 |
(3)下列情况会造成样品中氢氧化钠的质量分数比实际数据偏小的有______。
| A.反应过程中盐酸会挥发出氯化氢气体 |
| B.氢氧化钠溶液从空气中吸收二氧化碳 |
| C.A内残留二氧化碳不能被氢氧化钠吸收 |
| D.反应太快导致二氧化碳气体未被完全吸收 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】金属的用途很广,我们应该保护好金属资源。回答以下问题:
(1)金属能用于做炊具,是因为金属具有___________ (填“导电性”或“导热性”);
(2)铁制品生锈是由于铁制品同时与空气中的氧气和___________ 接触而诱蚀。
(3)向一定量的Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和溶液。对滤渣和滤液分析正确的有 (填序号)。
(4)除去ZnSO4溶液中少量CuSO4杂质,下列试剂中最好的是 。
(1)金属能用于做炊具,是因为金属具有
(2)铁制品生锈是由于铁制品同时与空气中的氧气和
(3)向一定量的Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和溶液。对滤渣和滤液分析正确的有 (填序号)。
| A.若滤液呈蓝色,则滤渣中一定含有Ag,一定不含有Cu |
| B.若滤液中只含有一种溶质,则滤渣中一定含有Ag、Cu,可能含有Zn |
| C.若滤渣中只含有一种金属,则溶液中一定含有Zn(NO3)2、Cu(NO3)2,一定不含有AgNO3 |
| D.若向滤渣中滴加稀盐酸无气体产生,则滤液中一定含有Zn(NO3)2,可能含有AgNO3、Cu(NO3)2 |
| A.NaOH溶液 | B.Fe | C.CuO | D.Zn |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.《天工开物》是我国古代一部科技巨著。书中介绍了锌的冶炼方法:将炉甘石 (ZnCO3 )和煤炭饼装入炼锌罐,泥封后其底铺薪,发火煅红
以下是模拟该过程的流程图。

(1)流程中“粉碎”炉甘石的目的是_____ 。
(2)反应区内碳酸锌高温分解的化学方程式为_____ 。
(3)冷凝区中将气态锌转化成液态锌,理论上该区应控制的温度范围是_____ 。
(4)“冷定”后方能“毁罐”取出,从化学变化角度解释其原因是_____ 。
Ⅱ.A﹣E 是初中化学常见的五种物质,它们的变化关系如图所示其中A、E均为黑色固体,C是红色固体,在常温下,B和D均是由两种元素组成的气体。

(5)A的化学式为_____ 。
(6)D→B的化学反应方程式为_____ ,从反应能量变化的角度看此反应属于_____ (填“放热”或“吸热”)反应。
(7)请写出B与E具有的相似化学性质_____ 。
以下是模拟该过程的流程图。

| 资料卡片 碳酸锌高温分解的反应原理 与碳酸钙相似 锌的熔点419℃,沸点907℃ |
(1)流程中“粉碎”炉甘石的目的是
(2)反应区内碳酸锌高温分解的化学方程式为
(3)冷凝区中将气态锌转化成液态锌,理论上该区应控制的温度范围是
(4)“冷定”后方能“毁罐”取出,从化学变化角度解释其原因是
Ⅱ.A﹣E 是初中化学常见的五种物质,它们的变化关系如图所示其中A、E均为黑色固体,C是红色固体,在常温下,B和D均是由两种元素组成的气体。

(5)A的化学式为
(6)D→B的化学反应方程式为
(7)请写出B与E具有的相似化学性质
您最近一年使用:0次



