将一定质量的锌粉加入到硝酸铜、硝酸银和硝酸铝的混合溶液中、如图是盛放混合溶液的烧杯中固体质量在反应过程中的变化情况。
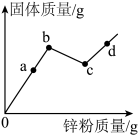
(1)写出ab段发生反应的化学方程式:______ 。
(2)bc段固体总质量减少的原因是什么?
(3)请分析并解释cd段烧杯内溶液质量的变化情况。

(1)写出ab段发生反应的化学方程式:
(2)bc段固体总质量减少的原因是什么?
(3)请分析并解释cd段烧杯内溶液质量的变化情况。
2021·河南商丘·模拟预测 查看更多[2]
更新时间:2021-08-25 21:53:00
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】金属在日常生活和工农业生产方面应用广泛。糖果等食品常用银白色、被称为“锡纸”的材料进行包装,“锡纸”实际上是铝箱纸。
(1)铝可以制成铝箔,是因为它具有良好的__________ 性。
(2)将砂纸打磨过的“锡纸”放入 (填字母)中,根据实验现象,结合金属活动性可证明“锡纸”非锡。
(3)某化学兴趣小组的同学想从含有A12(SO4)3、CuSO4的废液中回收金属铜,设计了如图实验。
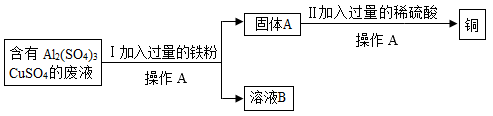
①写出操作A的名称__________ 。
②溶液B中所含的物质除水外还含有的物质是__________ (填化学式)。
③Ⅱ中加入过量的稀硫酸的目的是__________ 。
(1)铝可以制成铝箔,是因为它具有良好的
(2)将砂纸打磨过的“锡纸”放入 (填字母)中,根据实验现象,结合金属活动性可证明“锡纸”非锡。
| A.稀盐酸 | B.稀硫酸 | C.硫酸铜溶液 | D.硫酸亚铁溶液 |

①写出操作A的名称
②溶液B中所含的物质除水外还含有的物质是
③Ⅱ中加入过量的稀硫酸的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】很多金属都能与氧气、盐酸、稀硫酸等发生反应,但反应的难易和剧烈程度不同。
(1)虽然金属铝的化学性质活泼,但铝制品却很耐用,原因是铝会与氧气反应,在其表面生成一层致密的薄膜,此反应的化学方程式是_____ 。铝与硝酸银溶液能发生置换反应,反应的化学方程式是 _____ 。
(2)在金属活动性顺序中,排在Fe和Pb之间的金属是_____ (填名称)。
(3)某银白色金属放入稀硫酸中后,其表面会有大量气泡生成。若将此金属放入硫酸铜溶液中,可以观察到其表面会有_____ 。
(4)有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,Y表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y、Z的金属活动性由强到弱的顺序:_____ (用“>”连接)。
(5)金属资源合理开发及回收利用是绿色化学发展的重要方向。工业常通过废锂电池(主要成份为LiCoO2、炭粉和铝箔)回收可得到草酸钴晶体。
在实验室中研究不同条件下Co2+的浸出率(样品质量、加入盐酸体积均相同),结果如表。从实验结果看,在仅考虑提高Co2+的浸出率的情况下,回答下列问题:
Ⅰ.本实验研究了哪些因素对钴元素浸出率的影响:反应时间、_____ 。
Ⅱ.实验⑤⑥的目的是_____ 。
Ⅲ.实验_____ 为最优反应条件。
(1)虽然金属铝的化学性质活泼,但铝制品却很耐用,原因是铝会与氧气反应,在其表面生成一层致密的薄膜,此反应的化学方程式是
(2)在金属活动性顺序中,排在Fe和Pb之间的金属是
(3)某银白色金属放入稀硫酸中后,其表面会有大量气泡生成。若将此金属放入硫酸铜溶液中,可以观察到其表面会有
(4)有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,Y表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y、Z的金属活动性由强到弱的顺序:
(5)金属资源合理开发及回收利用是绿色化学发展的重要方向。工业常通过废锂电池(主要成份为LiCoO2、炭粉和铝箔)回收可得到草酸钴晶体。
在实验室中研究不同条件下Co2+的浸出率(样品质量、加入盐酸体积均相同),结果如表。从实验结果看,在仅考虑提高Co2+的浸出率的情况下,回答下列问题:
| 编号 | 温度/℃ | 时间/min | 盐酸浓度/% | 钴浸出率/% |
| ① | 80 | 120 | 10.5 | 90.82 |
| ② | 80 | 150 | 8.5 | 100 |
| ③ | 80 | 180 | 10.5 | 100. |
| ④ | 80 | 150 | 5.4 | 80.26 |
| ⑤ | 70 | 150 | 8.5 | 86.85 |
| ⑥ | 90 | 150 | 8.5 | 100 |
Ⅱ.实验⑤⑥的目的是
Ⅲ.实验
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
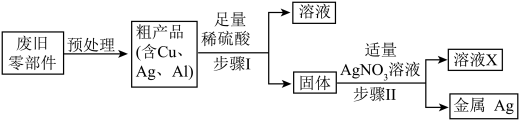
【推荐1】现代生活中,铜被广泛用于制作导线、电缆、印刷电路板等。手机、电脑的线路板中含有铝、铁、铜等金属,以及少量金、银等贵重金属。金属的回收利用,既可以保护金属资源,又可以减少环境污染。化学小组仿照废旧线路板处理流程中的部分方法,利用实验废液(液体成分为硝酸铝、硝酸亚铁、硝酸铜)提取铜,实验步骤如下图所示。

(1)步骤I充分反应后的固体成分为_____________ 。
(2)步骤Ⅱ中发生反应的化学方程式为___________ ,该反应的基本反应类型是__________ 。
(3)步骤I反应后的浅绿色液体中一定不含___________ ,结合实验现象进行分析____________ 。

(1)步骤I充分反应后的固体成分为
(2)步骤Ⅱ中发生反应的化学方程式为
(3)步骤I反应后的浅绿色液体中一定不含
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学源于生活,生活中蕴含着许多化学知识:
(1)点燃蚊香闻到气味,这是因为分子_______ 。
(2)打开汽水瓶盖时,汽水会自动喷出来,其中气体是_______ 。
(3)“真金不怕火炼”是指金即使在高温下也不与_______ 反应。
(4)金刚石与石墨可称为“同素异形体”,物理性质存在差异的原因是_______ 。
(5)钢铁车身喷漆处理既美观又防锈,喷漆防锈的原理是_______ 。
(6)燃料:近些年厨房燃料的更新换代如下图所示:

①煤燃烧可能产生的污染物有_______ (填标号)。
A.二氧化碳 B.二氧化硫 C.一氧化碳 D.粉尘固体颗粒
②天然气主要成分是_______ (填化学名称),其完全燃烧,产物不会对空气有污染,请你写出其燃烧的化学方程式是_______ 。
(1)点燃蚊香闻到气味,这是因为分子
(2)打开汽水瓶盖时,汽水会自动喷出来,其中气体是
(3)“真金不怕火炼”是指金即使在高温下也不与
(4)金刚石与石墨可称为“同素异形体”,物理性质存在差异的原因是
(5)钢铁车身喷漆处理既美观又防锈,喷漆防锈的原理是
(6)燃料:近些年厨房燃料的更新换代如下图所示:

①煤燃烧可能产生的污染物有
A.二氧化碳 B.二氧化硫 C.一氧化碳 D.粉尘固体颗粒
②天然气主要成分是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,溶液质量与加入锌的质量关系如图所示。
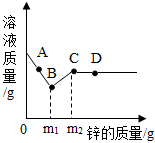
(1)写出A点时发生反应的化学方程式_____ 。
(2)当加入锌的质量在m1-m2g时,溶液的质量为什么会增加:_____ 。

(1)写出A点时发生反应的化学方程式
(2)当加入锌的质量在m1-m2g时,溶液的质量为什么会增加:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】将等质量的锌粉和铁粉分别与溶液质质量分数相同且相等质量的稀硫酸充分反应,产生H2的质量与时间的关系如下图所示。请回答下列问题:
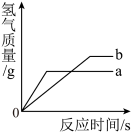
(1)表示锌粉与稀盐酸反应的曲线为_______ (填“a”或“b”);
(2)对于a曲线表示的反应,物质_______ (填化学式)有剩余;
(3)若有一种金属有剩余,则剩余的金属一定是_______ (填化学式)。

(1)表示锌粉与稀盐酸反应的曲线为
(2)对于a曲线表示的反应,物质
(3)若有一种金属有剩余,则剩余的金属一定是
您最近一年使用:0次