“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质。某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶。请回答:
(1)溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在蒸发操作中的作用是什么?
(2)加入Na2CO3溶液的目的是什么?
(3)以上方案还需完善,请说明原因并加以补充。
(1)溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在蒸发操作中的作用是什么?
(2)加入Na2CO3溶液的目的是什么?
(3)以上方案还需完善,请说明原因并加以补充。
更新时间:2021-10-02 15:17:01
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】我国盐碱地规模大,水稻、小麦等粮食作物难以在这些盐碱地生长。近年来,由袁隆平院士领衔的青岛海水稻研究发展中心致力于“海水稻”研发,通过基因测序技术,筛选出天然抗盐、抗碱、抗病基因,通过常规育种、杂交与分子标记辅助育种技术,已经取得阶段性成果。“海水稻”的灌溉可以使用半咸水,且“海水稻”在条件恶劣的盐碱地生长很少会患普通稻的病虫害。
(1)盐碱地(含较多NaCl、Na2CO3)可通过施加适量________ (填“硫黄”或“熟石灰”)以降低土壤碱性。
(2)关于未来推广海水稻的意义有________ (任写一条)。
(1)盐碱地(含较多NaCl、Na2CO3)可通过施加适量
(2)关于未来推广海水稻的意义有
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下面科普短文。
“碳中和”是指人类活动的碳排放通过森林碳汇和人工手段加以捕集、利用和封存,使排放到大气中的温室气体净增量为零。CaO可在较高温度下捕集CO2,在更高温度下将捕集的CO2释放利用。CaC2O4·H2O在较高温度下可分解制备氧化钙,同时得到其他三种氧化物。研究表明:用该反应生成的氧化钙比用碳酸钙分解得到的氧化钙更加疏松多孔,捕集二氧化碳效果更好。
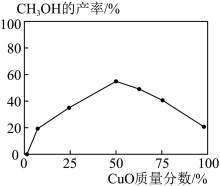
目前,CO2捕集技术的关键是将CO2从排放物中分离出来。分离方法主要分为物理吸收法和化学吸收法。物理吸收法中的一种是用甲醇作溶剂进行吸收。化学吸收法用氨水(NH3⋅H2O)作为吸收剂,控制30℃左右,采用喷氨技术吸收CO2生成碳酸氢铵(NH4HCO3)。分离后的CO2与H2一定条件下反应生成甲醇(CH3OH) 和水,CH3OH的产率除受浓度、温度、压强等因素影响外,还受催化剂CuO质量分数的影响,如图所示。
我国科学家们撰文提出“液态阳光”概念,即将太阳能转化为可稳定存储并且可输出的燃料,实现燃料零碳化。随着科学技术的发展,今后的世界,每天的阳光将为我们提供取之不尽、用之不竭的热、电,还有可再生燃料!
依据文章内容,回答下列问题:
(1)森林碳汇主要是指绿色植物通过光合作用将(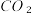 吸收并固定的过程。此过程将太阳能转化为
吸收并固定的过程。此过程将太阳能转化为______ 能。
(2)CaC2O4⋅H2O分解的化学方程式为:CaC2O4⋅H2O CaO+CO2↑+X↑+H2O↑。其中X的化学式为
CaO+CO2↑+X↑+H2O↑。其中X的化学式为______ 。该反应生成的 CaO比石灰石分解制得的CaO更加疏松多孔,原因是______ 。
(3)用CO2与H2制取甲醇的化学方程式为______ 。
(4)由文中图可得到的结论是______ 。
(5)采用喷氨技术吸收CO2时,温度要控制在30℃左右,可能的原因是______ 。
(6)请你举一例替代含碳燃料的新能源______ 。
(7)下列说法不正确的是______ (填字母)。
a.碳中和的“碳”指的是碳单质
b.“液态阳光”将实现燃料零碳化
c.控制化石燃料的使用可减少碳排放
(8)下列关于二氧化碳的性质和用途相对应的用“—”链接。
干冰会升华 气体肥料
二氧化碳不燃烧,不支持燃烧 人工降雨
二氧化碳能参与光合作用 灭火剂
“碳中和”是指人类活动的碳排放通过森林碳汇和人工手段加以捕集、利用和封存,使排放到大气中的温室气体净增量为零。CaO可在较高温度下捕集CO2,在更高温度下将捕集的CO2释放利用。CaC2O4·H2O在较高温度下可分解制备氧化钙,同时得到其他三种氧化物。研究表明:用该反应生成的氧化钙比用碳酸钙分解得到的氧化钙更加疏松多孔,捕集二氧化碳效果更好。
目前,CO2捕集技术的关键是将CO2从排放物中分离出来。分离方法主要分为物理吸收法和化学吸收法。物理吸收法中的一种是用甲醇作溶剂进行吸收。化学吸收法用氨水(NH3⋅H2O)作为吸收剂,控制30℃左右,采用喷氨技术吸收CO2生成碳酸氢铵(NH4HCO3)。分离后的CO2与H2一定条件下反应生成甲醇(CH3OH) 和水,CH3OH的产率除受浓度、温度、压强等因素影响外,还受催化剂CuO质量分数的影响,如图所示。

我国科学家们撰文提出“液态阳光”概念,即将太阳能转化为可稳定存储并且可输出的燃料,实现燃料零碳化。随着科学技术的发展,今后的世界,每天的阳光将为我们提供取之不尽、用之不竭的热、电,还有可再生燃料!
依据文章内容,回答下列问题:
(1)森林碳汇主要是指绿色植物通过光合作用将(
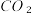 吸收并固定的过程。此过程将太阳能转化为
吸收并固定的过程。此过程将太阳能转化为(2)CaC2O4⋅H2O分解的化学方程式为:CaC2O4⋅H2O
 CaO+CO2↑+X↑+H2O↑。其中X的化学式为
CaO+CO2↑+X↑+H2O↑。其中X的化学式为(3)用CO2与H2制取甲醇的化学方程式为
(4)由文中图可得到的结论是
(5)采用喷氨技术吸收CO2时,温度要控制在30℃左右,可能的原因是
(6)请你举一例替代含碳燃料的新能源
(7)下列说法不正确的是
a.碳中和的“碳”指的是碳单质
b.“液态阳光”将实现燃料零碳化
c.控制化石燃料的使用可减少碳排放
(8)下列关于二氧化碳的性质和用途相对应的用“—”链接。
干冰会升华 气体肥料
二氧化碳不燃烧,不支持燃烧 人工降雨
二氧化碳能参与光合作用 灭火剂
您最近一年使用:0次
【推荐3】碳酸锂(Li2CO3)是制备锂电池的重要原料。工业上用锂辉石精矿(主要成分为Li2O)为原料制备Li2CO3的流程如下图所示。______ 。
(2)为了探究酸浸槽中的最佳条件,技术人员做了4组实验,酸浸时间4h,其余相关数据见表。
本实验中______ (填“B、C”或“C、D”)两组实验对比能说明温度对锂元素的浸出率有影响。
(3)反应器中加入饱和K2CO3溶液的目的是______ 。
(4)沉锂池中进行的操作后用到的玻璃仪器有漏斗、烧杯和______ 。
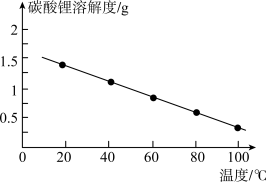
(5)根据Li2CO3的溶解度曲线图,分析洗涤槽中应采用的试剂是______ (填“冰水”或“热水”)。

(2)为了探究酸浸槽中的最佳条件,技术人员做了4组实验,酸浸时间4h,其余相关数据见表。
| 组别 | 矿酸比 | 硫酸浓度(%) | 温度(℃) | 锂元素浸出率(%) |
| A | 1:1 | 90 | 100 | 70.34 |
| B | 1:1 | 98 | 100 | 73.89 |
| C | 1:1 | 98 | 150 | 78.24 |
| D | 1:3 | 98 | 200 | 85.53 |
(3)反应器中加入饱和K2CO3溶液的目的是
(4)沉锂池中进行的操作后用到的玻璃仪器有漏斗、烧杯和
(5)根据Li2CO3的溶解度曲线图,分析洗涤槽中应采用的试剂是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】从盐湖中提取的某种矿物主要含有氯化钾,还有少量硫酸镁、氯化钙和二氧化硅,从该矿物中提取氯化钾的流程如下图。
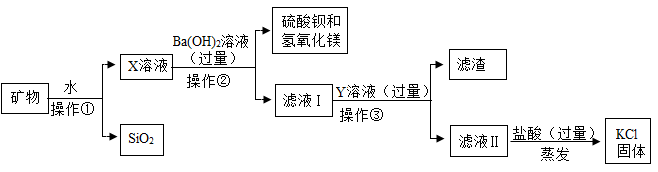
查阅资料:SiO2不溶于水。请回答下列问题 :
(1)操作①的名称是_____ ;
(2)操作②中加入过量Ba(OH)2溶液的主要目的是除去X溶液中的___ (填离子符号)
(3)Y溶液中溶质的化学式为_____ ;
(4)蒸发溶液得到氯化钾固体的过程中,要用玻璃棒不断搅拌,目的是___ 。

查阅资料:SiO2不溶于水。请回答下列问题 :
(1)操作①的名称是
(2)操作②中加入过量Ba(OH)2溶液的主要目的是除去X溶液中的
(3)Y溶液中溶质的化学式为
(4)蒸发溶液得到氯化钾固体的过程中,要用玻璃棒不断搅拌,目的是
您最近一年使用:0次
【推荐2】1926年我因著名化学家侯德榜先生创立了侯氏制破法,促进了世界制碱技术的发展,侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

(1)t1°C时,NaCl的溶解度______ Na2CO3的溶解度(填“大于”“等于”“小于”之一);
(2)t°C时,50g水中加入10gNa2CO3充分溶解,所得溶液中溶质和溶液的质量比为______ (填最简整数比);
(3)t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温至t2℃,此时所得碳酸钠溶液溶质质量分数______ 氯化钠溶液溶质质量分数(填“大于”“等于”“小于”“无法判断”之一)。
(4)若Na2CO3中混有少量NaCl,欲提纯Na2CO3晶体,宜采用的方法是______ (项 “蒸发结晶”、“降温结晶”之一)。
(5)欲除去某氯化钠样品中的可溶性杂质(杂质为CaCl2、Na2SO4),取该样品加适量水完全溶解,再向其中加入两种溶液,a.稍过量的BaCl2溶液。b.稍过量的Na2CO3溶液。将杂质离子转化为沉淀,过滤去除沉淀后,再加适量的稀盐酸,常温下,将溶液的pH调为7,然后蒸发结晶,得到精制氯化钠。上述加入a、b两种溶液的先后顺序应该是______ (选填"a→b"、“b→a”之一)。

(1)t1°C时,NaCl的溶解度
(2)t°C时,50g水中加入10gNa2CO3充分溶解,所得溶液中溶质和溶液的质量比为
(3)t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温至t2℃,此时所得碳酸钠溶液溶质质量分数
(4)若Na2CO3中混有少量NaCl,欲提纯Na2CO3晶体,宜采用的方法是
(5)欲除去某氯化钠样品中的可溶性杂质(杂质为CaCl2、Na2SO4),取该样品加适量水完全溶解,再向其中加入两种溶液,a.稍过量的BaCl2溶液。b.稍过量的Na2CO3溶液。将杂质离子转化为沉淀,过滤去除沉淀后,再加适量的稀盐酸,常温下,将溶液的pH调为7,然后蒸发结晶,得到精制氯化钠。上述加入a、b两种溶液的先后顺序应该是
您最近一年使用:0次
【推荐3】海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源,工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料,部分流程如图:

Ⅰ、海水晒“盐”:
(1)海水经过蒸发池、结晶池,得到的母液是当时温度下氯化钠的______ 溶液(选填“饱和”或“不饱和”)。
Ⅱ、粗盐提纯:
(2)经溶解、过滤、蒸发后得到的精盐还含有可溶性的MgCl2、CaCl2、Na2SO4,为除去杂质得到纯净的氯化钠,将精盐溶解后,加入试剂的合理顺序为______ (A过量的Na2CO3溶液; B过量的BaCl2溶液;C过量的NaOH溶液。用以上字母序号填空),过滤,再向滤液中加入足量稀盐酸,蒸发即可。
Ⅲ、海水制“镁”:
(3)在氢氧化镁中加入的试剂a是______ (填名称)。
(4)写出电解熔融状态的MgCl2制取Mg的化学方程式______ 。
Ⅳ、海水制“碱”:
(5)我国科学家侯德榜以饱和食盐水为原料发明了侯氏制碱法,其主要反应原理之一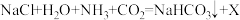 ,X的化学式为
,X的化学式为______ 。

Ⅰ、海水晒“盐”:
(1)海水经过蒸发池、结晶池,得到的母液是当时温度下氯化钠的
Ⅱ、粗盐提纯:
(2)经溶解、过滤、蒸发后得到的精盐还含有可溶性的MgCl2、CaCl2、Na2SO4,为除去杂质得到纯净的氯化钠,将精盐溶解后,加入试剂的合理顺序为
Ⅲ、海水制“镁”:
(3)在氢氧化镁中加入的试剂a是
(4)写出电解熔融状态的MgCl2制取Mg的化学方程式
Ⅳ、海水制“碱”:
(5)我国科学家侯德榜以饱和食盐水为原料发明了侯氏制碱法,其主要反应原理之一
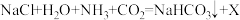 ,X的化学式为
,X的化学式为
您最近一年使用:0次



