纯碱是一种非常重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。然后再焙烧NaHCO3制得纯碱(Na2CO3)。生产纯碱的工艺流程示意图如下:
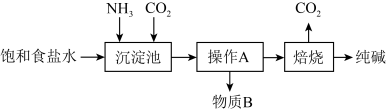
请回答下列问题:
①操作A的名称为_______ 。
②可用_______ 方法获得物质B固体
③向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,其原因是___ 。
④析出NaHCO3晶体中可能含有少量氯离子杂质,实验室确定NaHCO3晶体表面杂质洗净的方法___
(2)常温下在10mL10.6g·L-1Na2CO3溶液中逐滴加入3.65g·L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图所示。
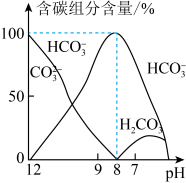
根据图示回答下列问题:
①在同一溶液中, 、
、 、H2CO3
、H2CO3_______ (填“能”或“不能”)大量共存。
②当pH=7时,溶液中含碳元素的主要微粒为_______ (填化学式)。
(3)浓盐酸的溶质质量分数为36%,密度是1.18g/cm3,现要配制0.365%的稀盐酸(该稀盐酸密度近似为水的密度)200ml,需要该浓盐酸_______ 毫升, 配制时还应加入_______ 毫升水。(水的密度为1.00g/cm3)(保留2位小数)
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。然后再焙烧NaHCO3制得纯碱(Na2CO3)。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A的名称为
②可用
③向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,其原因是
④析出NaHCO3晶体中可能含有少量氯离子杂质,实验室确定NaHCO3晶体表面杂质洗净的方法
(2)常温下在10mL10.6g·L-1Na2CO3溶液中逐滴加入3.65g·L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图所示。

根据图示回答下列问题:
①在同一溶液中,
 、
、 、H2CO3
、H2CO3②当pH=7时,溶液中含碳元素的主要微粒为
(3)浓盐酸的溶质质量分数为36%,密度是1.18g/cm3,现要配制0.365%的稀盐酸(该稀盐酸密度近似为水的密度)200ml,需要该浓盐酸
更新时间:2021-10-10 15:15:16
|
相似题推荐
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐1】胆矾的化学式为CuSO4·5H2O,它是一种结晶水合物。为测量t℃时,饱和硫酸铜溶液的质量分数,进行如下实验操作:
I、称量空蒸发皿的质量(m1 g)。
II、取一定量饱和硫酸铜溶液于蒸发皿中,称量饱和硫酸铜溶液与蒸发皿的质量(m2 g)。
III、用酒精灯充分加热,直至蒸发皿中固体完全变白。
IV、待蒸发皿冷却至室温后,称量剩余固体与蒸发皿的质量(m3 g)。实验结果及CuSO4的溶解度如表:
上述实验方案与结果是否合理?若合理,请计算该饱和硫酸铜溶液的质量分数;若不合理,请阐述你的理由。
I、称量空蒸发皿的质量(m1 g)。
II、取一定量饱和硫酸铜溶液于蒸发皿中,称量饱和硫酸铜溶液与蒸发皿的质量(m2 g)。
III、用酒精灯充分加热,直至蒸发皿中固体完全变白。
IV、待蒸发皿冷却至室温后,称量剩余固体与蒸发皿的质量(m3 g)。实验结果及CuSO4的溶解度如表:
| t | m1 | m2 | m3 | |
| 实验数据 | 18℃ | 36.7g | 97.1g | 47.1g |
| 温度(℃) | 10 | 20 | ||
| CuSO4 的溶解度(g/100g 水) | 17.4 | 20.7 | ||
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
真题
解题方法
【推荐2】下表是KNO3在不同温度时的溶解度,回答问题。
(1)影响固体物质溶解度大小的因素有__________ (填一种)。
(2)30℃时KNO3溶液的溶质质量分数的最大值是_______ (只列出表达式)。
(3)90℃时,将一定质量的KNO3溶液按图示进行操作:

90℃时的KNO3溶液是_____ (填“饱和”或“不饱和”)溶液。图中n的数值为__ 。
温度/℃ | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 |
(1)影响固体物质溶解度大小的因素有
(2)30℃时KNO3溶液的溶质质量分数的最大值是
(3)90℃时,将一定质量的KNO3溶液按图示进行操作:

90℃时的KNO3溶液是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】列表法和作图法是常用的数据处理方法。请根据下列图表进行分析。
(1)代表NaCl溶解度曲线的是_____ (填“a”或“b”或“c”)。
(2)将30℃一定质量NaCl的饱和溶液降温至20℃,析出3g氯化钠,则该溶液中溶剂质量为_________ g。
(3)在20℃-30℃之间NaCl和KNO3具有相等的溶解度S,S的最小取值范围是______ 。
(4)下列说法正确的是___________(填字母)。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 27.6 | 31.0 | 36.0 | 37.0 | 37.3 | 37.3 | 37.8 | |
(1)代表NaCl溶解度曲线的是
(2)将30℃一定质量NaCl的饱和溶液降温至20℃,析出3g氯化钠,则该溶液中溶剂质量为
(3)在20℃-30℃之间NaCl和KNO3具有相等的溶解度S,S的最小取值范围是
(4)下列说法正确的是___________(填字母)。
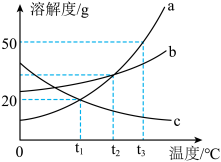
| A.将t3℃时a、b、c的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小关系为a=c<b |
| B.将三种物质等质量的饱和溶液从t2℃降温至t1℃,所得溶液的质量关系为a<b<c |
| C.将t1℃时c的饱和溶液稀释,需要用到的仪器有托盘天平、量筒、胶头滴管、烧杯、玻璃棒 |
| D.t3℃时,向100g溶质质量分数为20%的a溶液中加入a物质60g,溶质质量分数变为50% |
您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
解题方法
【推荐1】追踪科学家的足迹
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标。下面是实验室模拟侯氏制碱法生产原理的主要过程:
①0℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4Cl晶体,过滤,得到NH4Cl。
材料2:四种盐在不同温度下的溶解度表。
试回答下列问题:
(1)在实验室中,你选择的制备CO2反应的化学方程式为_______ 。在工业生产中,要获得生产纯碱的原料CO2 你认为最经济实用的方法是以________ 为原料,该反应的化学方程式为________ 。
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是_______ 。
A生产过程中部分反应产物可作为原料循环使用
B副产品是一种氮肥
C反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是________ 。
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同)____ 。在③中,将析出的晶体过滤后,溶液中数量减少的离子有______ ;滤液中仍然存在的离子有_____ 。②中反应的化学方程式为______ 。
(5)在20℃时向含NH4HCO321g的饱和溶液中加入足量食盐。试通过计算说明,随着食盐的逐渐加入,为什么会有NaHCO3晶体析出,而没有NH4Cl晶体析出?_________________________________ 理论上能析出多少克NaHCO3?_______ (友情提示:可能用到的相对分子质量:NH4HCO3: 79;NaCl: 58.5;NaHCO3: 84;NH4CI: 53.5)
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标。下面是实验室模拟侯氏制碱法生产原理的主要过程:
①0℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4Cl晶体,过滤,得到NH4Cl。
材料2:四种盐在不同温度下的溶解度表。
温度 溶解度 盐 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NH4HCO3 | 15.8 | 21.0 | 27.0 | ------ | ------ |
NaHCO3 | 8.1 | 9.6 | 11.1 | 12.7 | ---- |
NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(1)在实验室中,你选择的制备CO2反应的化学方程式为
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是
A生产过程中部分反应产物可作为原料循环使用
B副产品是一种氮肥
C反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同)
(5)在20℃时向含NH4HCO321g的饱和溶液中加入足量食盐。试通过计算说明,随着食盐的逐渐加入,为什么会有NaHCO3晶体析出,而没有NH4Cl晶体析出?
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】纯碱是重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。然后再焙烧NaHCO3制得纯碱(Na2CO3)。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A的名称为______ 。
②可用______ 结晶的方法获得物质B固体。
③向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,其原因是______ 。
④析出NaHCO3晶体中可能含有少量氯离子杂质,实验室确定NaHCO3晶体表面杂质洗净的方法______
(2)常温下在10mL10.6g·L-1Na2CO3溶液中逐滴加入3.65g·L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图所示。

根据图示回答下列问题:
①在同一溶液中, 、
、 、H2CO3
、H2CO3______ (填“能”或“不能”)大量共存。
②当pH=7时,溶液中含碳元素的主要微粒为______ 和______ (填化学式)。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。然后再焙烧NaHCO3制得纯碱(Na2CO3)。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A的名称为
②可用
③向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,其原因是
④析出NaHCO3晶体中可能含有少量氯离子杂质,实验室确定NaHCO3晶体表面杂质洗净的方法
(2)常温下在10mL10.6g·L-1Na2CO3溶液中逐滴加入3.65g·L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图所示。

根据图示回答下列问题:
①在同一溶液中,
 、
、 、H2CO3
、H2CO3②当pH=7时,溶液中含碳元素的主要微粒为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。我国制碱工业先驱侯德榜发明了“侯氏联合制碱法”,在充分利用海洋资源的基础上,结合“侯氏联合制碱法”的基本原理,可模拟实现工业生产纯碱的过程如下(某些反应产物略去)

(1)操作a的名称是_______
(2)反应②为_______ 反应(填“放热”或“吸热”),反应③的化学方程式为:_______
(3)向精制饱和食盐水中通入两种气体的顺序是:先通氨气形成饱和氨盐水,然后在加压条件下通入CO2.这样操作的目的是______ 。
(4)仔细观察流程图其中可循环利用的物质除CO2气体外,还有_______ 。

(1)操作a的名称是
(2)反应②为
(3)向精制饱和食盐水中通入两种气体的顺序是:先通氨气形成饱和氨盐水,然后在加压条件下通入CO2.这样操作的目的是
(4)仔细观察流程图其中可循环利用的物质除CO2气体外,还有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)甲、乙两车间的废水中含有K+、Ag+、Cu2+、 、OH-、
、OH-、 六种离子,乙车间废水呈蓝色,其中的阴离子为
六种离子,乙车间废水呈蓝色,其中的阴离子为___________ ,如果加入足量的铁可以回收的金属有_____________ 。
(2)用铁、氧化铁、氢氧化铁、稀硫酸、硫酸镁溶液、硫酸铜溶液六种物质两两进行反应,能得到硫酸铁的方法有_____________ 种,能发生___________ 个置换反应。
 、OH-、
、OH-、 六种离子,乙车间废水呈蓝色,其中的阴离子为
六种离子,乙车间废水呈蓝色,其中的阴离子为(2)用铁、氧化铁、氢氧化铁、稀硫酸、硫酸镁溶液、硫酸铜溶液六种物质两两进行反应,能得到硫酸铁的方法有
您最近一年使用:0次
【推荐2】在宏观、微观和符号之间建立联系,是化学学科独特的思维方式。学习了有关酸碱盐的知识后,某化学小组对这部分内容进行了归纳总结,列出了以下关系图。
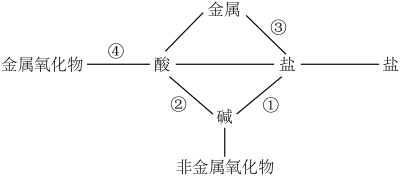
(1)关系图中总共涉及到_______ 种基本反应类型;
(2)图中①发生反应,生成两种沉淀,若参加反应的一种物质为CuSO4,则另一种物质为_____ (填化学式);
(3)反应②为中和反应,其实质可以表示为: 。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式中,反应前离子带电荷总数等于反应后离子带电荷总数。反应③的一个实例如图1所示,请用离子方程式表示该反应
。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式中,反应前离子带电荷总数等于反应后离子带电荷总数。反应③的一个实例如图1所示,请用离子方程式表示该反应_______ ;
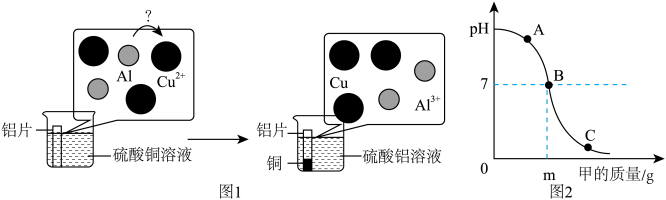
(4)用溶质质量分数均为10%的稀硫酸和氢氧化钠溶液进行实验,将甲溶液逐滴滴入100 g乙溶液中,测得溶液酸碱度变化如图2所示。则A点所含溶质的化学式为___ ,m的数值____ 100(填“>”、“<”或“=”);
(5)下列各组离子在指定的溶液中,能大量共存的是_______(填字母符号);
(6)请列举反应④的一条实际应用_______ 。

(1)关系图中总共涉及到
(2)图中①发生反应,生成两种沉淀,若参加反应的一种物质为CuSO4,则另一种物质为
(3)反应②为中和反应,其实质可以表示为:
 。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式中,反应前离子带电荷总数等于反应后离子带电荷总数。反应③的一个实例如图1所示,请用离子方程式表示该反应
。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式中,反应前离子带电荷总数等于反应后离子带电荷总数。反应③的一个实例如图1所示,请用离子方程式表示该反应
(4)用溶质质量分数均为10%的稀硫酸和氢氧化钠溶液进行实验,将甲溶液逐滴滴入100 g乙溶液中,测得溶液酸碱度变化如图2所示。则A点所含溶质的化学式为
(5)下列各组离子在指定的溶液中,能大量共存的是_______(填字母符号);
A.无色溶液中:K+、Na+、 、Fe2+ 、Fe2+ |
B.酸性溶液中:Mg2+、Na+、 、Cl- 、Cl- |
C.pH=11的溶液中:Ba2+、Mg2+、 、Cl- 、Cl- |
D.能使紫色石蕊溶液变红的溶液中:Na+、Ba2+、 、Cl- 、Cl- |
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
【推荐3】初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-===H2O。如图,像这种用实际参加反应的离子符号表示反应的式子叫离子方程式。离子方程式的书写一般步骤如下:(以碳酸钠与氯化钙反应为例)

Ⅰ.写出反应的化学方程式_________________________ 。
Ⅱ.把易溶于水、易电离的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成2Na++ +Ca2++2Cl-===CaCO3↓+2Na++2Cl-
+Ca2++2Cl-===CaCO3↓+2Na++2Cl-
Ⅲ.删除方程式两边不参加反应的离子Ca2++ ===CaCO3↓
===CaCO3↓
Ⅳ.检查方程式两边各元素的原子个数和电荷数是否相等。
试回答:
(1)酸、碱、盐在水溶液中发生的复分解反应实质就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或水或____________ 生成,反应就能发生。
(2)写出稀盐酸滴在大理石上所发生反应的离子方程式_____________________ 。
(3)用pH试纸测量稀盐酸的酸碱度时,先用水湿润试纸,则测得的结果将________ (填“偏大”“偏小”或“无影响”)。
(4)下列各组离子,能在溶液中大量共存的是______ 。
A.Na+、H+、 、OH- B.Na+、Ca2+、
、OH- B.Na+、Ca2+、 、Cl-
、Cl-
C.Na+、H+、 、Cl- D.K+、Cu2+、
、Cl- D.K+、Cu2+、 、Cl-
、Cl-
(5)写出一个能用Fe+2H+===Fe2++H2↑表示的化学方程式________________________ 。

Ⅰ.写出反应的化学方程式
Ⅱ.把易溶于水、易电离的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成2Na++
 +Ca2++2Cl-===CaCO3↓+2Na++2Cl-
+Ca2++2Cl-===CaCO3↓+2Na++2Cl-Ⅲ.删除方程式两边不参加反应的离子Ca2++
 ===CaCO3↓
===CaCO3↓Ⅳ.检查方程式两边各元素的原子个数和电荷数是否相等。
试回答:
(1)酸、碱、盐在水溶液中发生的复分解反应实质就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或水或
(2)写出稀盐酸滴在大理石上所发生反应的离子方程式
(3)用pH试纸测量稀盐酸的酸碱度时,先用水湿润试纸,则测得的结果将
(4)下列各组离子,能在溶液中大量共存的是
A.Na+、H+、
 、OH- B.Na+、Ca2+、
、OH- B.Na+、Ca2+、 、Cl-
、Cl-C.Na+、H+、
 、Cl- D.K+、Cu2+、
、Cl- D.K+、Cu2+、 、Cl-
、Cl-(5)写出一个能用Fe+2H+===Fe2++H2↑表示的化学方程式
您最近一年使用:0次



