金属钛是重要的航天、航海材料,钛因其硬度大,熔点高,常温下不和非金属、强酸反应,被誉为“未来金属”。由钛铁矿(主要成分为钛酸亚铁,化学式为FeTiO3)、焦炭、氧气为原料,提取金属钛的主要工艺过程一般需要经过三个阶段:
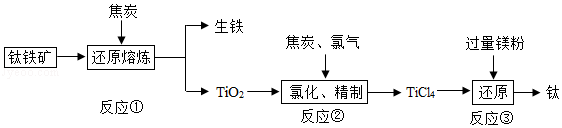
(1)反应前需要将钛酸亚铁和焦炭磨成粉末状的原因是______ ;钛酸亚铁(FeTiO3)中钛元素为____ 价。反应①中焦炭除了作还原剂还原金属矿物外,另一个重要作用是作燃料,提供反应所需要的能量。
(2)反应②中TiO2与C、Cl2在高温下反应,生成TiCl4和一种有毒气体,该气体是一种氧化物,其化学式为_______ ,请写出此反应的化学方程式____________ 。
(3)高温条件下,镁可以与TiCl4发生反应制得金属钛,同时生成氯化镁,请写出此反应的化学方程式________ ,该反应属于_______ 反应(基本反应类型),该反应需在氩气环境中进行,氩气起的作用是防止高温条件下镁和钛被氧化。
(4)如何从反应③后的固体中获得金属钛:向固体中加入足量的稀硫酸,充分反应后______ (填操作名称),洗涤,干燥。请写出此反应的化学方程式__________ 。

(1)反应前需要将钛酸亚铁和焦炭磨成粉末状的原因是
(2)反应②中TiO2与C、Cl2在高温下反应,生成TiCl4和一种有毒气体,该气体是一种氧化物,其化学式为
(3)高温条件下,镁可以与TiCl4发生反应制得金属钛,同时生成氯化镁,请写出此反应的化学方程式
(4)如何从反应③后的固体中获得金属钛:向固体中加入足量的稀硫酸,充分反应后
更新时间:2021-10-14 18:21:26
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】如图是初中化学中几种常见物质间的转化关系已知每种物质中都含有相对原子质量为40的一种元素,且A、D均含有两种元素。转化①至⑥的化学反应中,不包含的基本反应类型是______ ;C→D的化学方程式为______ ;物质B在生产、生活中的一种用途是______ 。


您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】已知A~F是初中化学常见的六种物质。他们之间的关系如图所示,图中“—”表示相连的两种物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物、反应条件及反应关系已略去),其中E物质是人体内胃酸的主要成分,B是应用最广泛的金属,A是红棕色粉末,D是理想的“绿色能源”,C与E、C与F反应都有白色沉淀生成。回答下列问题:

(1)写出物质B、D的化学式:B_____ ,D _____ ;
(2)写出A与E发生反应方程式为_____ ,该反应在生产中的应用是 _____ ;
(3)写出C与F反应的化学方程式为_____ ;
(4)写出F→E反应的化学方程式为_____ ;
(5)A与D发生反应的基本类型是属于_____ ;
(6)A~F六种物质中没有涉及到的物质种类是_____ (单质、酸、碱、盐或氧化物)。

(1)写出物质B、D的化学式:B
(2)写出A与E发生反应方程式为
(3)写出C与F反应的化学方程式为
(4)写出F→E反应的化学方程式为
(5)A与D发生反应的基本类型是属于
(6)A~F六种物质中没有涉及到的物质种类是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】整理归纳是良好的学习方法。初中化学很多反应可用“甲+乙→丙+丁”表示。甲、乙、丙、丁均为常见物质。
(1)若甲、丙的组成元素相同,丁是世界年产量最高的金属。则甲的化学式为___________ 。
(2)若甲、乙、丙的溶液均能使无色酚酞溶液变红,乙为纯碱。则甲、乙两物质的溶液反应的现象是___________ 。
(3)若甲、乙、丙、丁为四种不同类别的化合物,均含氧元素,则该反应的化学方程式为___________ 。(写一个)
(4)对于反应“甲+乙→丙+丁”,下列说法正确的是___________。(填标号)
(1)若甲、丙的组成元素相同,丁是世界年产量最高的金属。则甲的化学式为
(2)若甲、乙、丙的溶液均能使无色酚酞溶液变红,乙为纯碱。则甲、乙两物质的溶液反应的现象是
(3)若甲、乙、丙、丁为四种不同类别的化合物,均含氧元素,则该反应的化学方程式为
(4)对于反应“甲+乙→丙+丁”,下列说法正确的是___________。(填标号)
| A.甲、乙、丙、丁可以是同一类别化合物 |
| B.若乙为单质,则该反应一定是置换反应 |
| C.若丙为Cu(NO3)2,则甲可能为单质、氧化物、酸、碱或盐 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】海洋是一座巨大的宝库,海水中有丰富的水生生物和化学资源,海水晒盐后,以其母液(卤水)和贝壳为原料,还可生产具有特殊用途的材料—一纳米氧化镁,其简要流程如下:

(1)海水晒盐是______ (填“物理“或“化学”)变化,包含蒸发、______ 等过程。
(2)写出食盐的一种用途:______ 。
(3)A步骤反应的化学方程式是______ 。
(4)实验室进行a操作时,需要的玻璃仪器有烧杯、漏斗、______ 。
(5)下图是甲、乙两种固体物质的溶解度曲线。

①P点的意义是______ 。
②甲物质中含有少量乙物质,可用______ 的方法提纯甲(选填“降温结晶”、“蒸发结晶)将饱和甲溶液变为不饱和甲溶液,除了采用添加溶剂(水)的方法外,还可以采用的方法______ 。

(1)海水晒盐是
(2)写出食盐的一种用途:
(3)A步骤反应的化学方程式是
(4)实验室进行a操作时,需要的玻璃仪器有烧杯、漏斗、
(5)下图是甲、乙两种固体物质的溶解度曲线。

①P点的意义是
②甲物质中含有少量乙物质,可用
您最近一年使用:0次
【推荐2】有一包白色固体,可能含有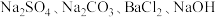 中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中啇加盐酸,现象如下图所示(
中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中啇加盐酸,现象如下图所示(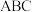 表示沉淀变化,
表示沉淀变化,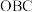 表示气体变化):
表示气体变化):
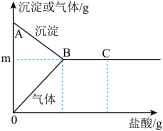
(1)由此推断原白色固体中一定含有_____ ,可能含有_____ 。
(2)在C点时,所得溶液中的溶质一定有_____ 。
(3)产生气体的化学方程式为_____ 。
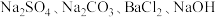 中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中啇加盐酸,现象如下图所示(
中的一种或几种。取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中啇加盐酸,现象如下图所示( 表示沉淀变化,
表示沉淀变化, 表示气体变化):
表示气体变化):
(1)由此推断原白色固体中一定含有
(2)在C点时,所得溶液中的溶质一定有
(3)产生气体的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐1】工业上用闪锌矿(主要成分是ZnS、FeS)冶炼锌,主要流程如下:

(1)焙烧炉中,ZnS转化为ZnO。补全该反应的化学方程式。
□ZnS+□_______  □ZnO+□SO2
□ZnO+□SO2
(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液。反应过程中需不断搅拌,其目的是________ 。
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价)。底吹炉中,主要发生如下反应:
① 3ZnFe2O4+C 2Fe3O4+3ZnO+CO↑ ② ZnFe2O4+CO
2Fe3O4+3ZnO+CO↑ ② ZnFe2O4+CO 2FeO+ZnO+CO2
2FeO+ZnO+CO2
③ ZnO+CO Zn(蒸气)+ CO2
Zn(蒸气)+ CO2
反应①~③中,化合价发生改变的元素有__________ 。
(4)最终可以获得锌的设备有__________ 。

(1)焙烧炉中,ZnS转化为ZnO。补全该反应的化学方程式。
□ZnS+□
 □ZnO+□SO2
□ZnO+□SO2(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液。反应过程中需不断搅拌,其目的是
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价)。底吹炉中,主要发生如下反应:
① 3ZnFe2O4+C
 2Fe3O4+3ZnO+CO↑ ② ZnFe2O4+CO
2Fe3O4+3ZnO+CO↑ ② ZnFe2O4+CO 2FeO+ZnO+CO2
2FeO+ZnO+CO2 ③ ZnO+CO
 Zn(蒸气)+ CO2
Zn(蒸气)+ CO2反应①~③中,化合价发生改变的元素有
(4)最终可以获得锌的设备有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
【推荐2】中国航天工业飞速发展,金属钛常被用于航空航天工业。下图是以钛铁矿为主要原料冶炼金属钛的生产工艺流程:

已知:钛铁矿主要成分为钛酸亚铁(FeTiO3)。请回答下列问题:
(1)FeTiO3中钛元素的化合价为_______ 。
(2)钛铁矿溶浸在浓硫酸中发生反应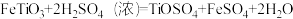 ,反应前需将钛铁矿粉碎的目的是
,反应前需将钛铁矿粉碎的目的是_______ 。
(3)溶液Ⅱ的主要溶质为TiOSO4,加热时和水发生反应。经过滤得到H2TiO3。写出化学方程式:_______ 。
(4)TiO2、C12和焦炭发生反应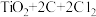

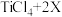 ,X的化学式为
,X的化学式为_______ 。
(5)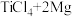

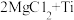 ,此反应中气体Ar的作用是
,此反应中气体Ar的作用是_______ 。
(6)在流程中,可用Na代替Mg制取Ti,其原因是_______ 。

已知:钛铁矿主要成分为钛酸亚铁(FeTiO3)。请回答下列问题:
(1)FeTiO3中钛元素的化合价为
(2)钛铁矿溶浸在浓硫酸中发生反应
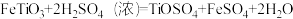 ,反应前需将钛铁矿粉碎的目的是
,反应前需将钛铁矿粉碎的目的是(3)溶液Ⅱ的主要溶质为TiOSO4,加热时和水发生反应。经过滤得到H2TiO3。写出化学方程式:
(4)TiO2、C12和焦炭发生反应
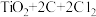

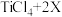 ,X的化学式为
,X的化学式为(5)
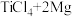

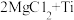 ,此反应中气体Ar的作用是
,此反应中气体Ar的作用是(6)在流程中,可用Na代替Mg制取Ti,其原因是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】铁红(Fe2O3)常用于油漆、油墨、橡胶等工业中,现以FeSO4·7H2O为原料制备铁红(Fe2O3)的一种方法如下:
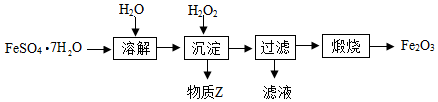
已知沉淀时的主要反应为: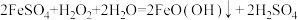
(1)FeO(OH)中铁元素的化合价为______ 。
(2)沉淀时需调节溶液的初始pH约为4,过程中需不断加入物质Z调节溶液的pH,保持溶液的pH为3.0-4.5,Z应该具备的性质是______ (填字母)。
A.不与FeO(OH)反应 B.能与酸反应 C.能与碱反应
(3)为保证产品纯度,需对沉淀进行洗涤。检验沉淀是否洗涤干净的方法:用适量蒸馏水淋洗过滤器中的沉淀2-3次,取少量最后一次淋洗下来的液体,______ (写出操作和现象),则沉淀已洗涤干净。
(4)在煅烧过程中需要不断加热,以达到高温条件,说明该反应可能属于______ 反应(选填“放热”或“吸热”)。为了加快煅烧的反应速率,可以将固体______ (填操作名称)。
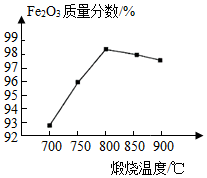
(5)如图为其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响。当煅烧温度达______ ℃时,Fe2O3的质量分数最高。若继续升高温度,所得产品发黑且铁元素质量分数升高,同时有无色气体产生,其可能原因是______ (用化学反应方程式表示)。

已知沉淀时的主要反应为:
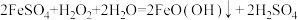
(1)FeO(OH)中铁元素的化合价为
(2)沉淀时需调节溶液的初始pH约为4,过程中需不断加入物质Z调节溶液的pH,保持溶液的pH为3.0-4.5,Z应该具备的性质是
A.不与FeO(OH)反应 B.能与酸反应 C.能与碱反应
(3)为保证产品纯度,需对沉淀进行洗涤。检验沉淀是否洗涤干净的方法:用适量蒸馏水淋洗过滤器中的沉淀2-3次,取少量最后一次淋洗下来的液体,
(4)在煅烧过程中需要不断加热,以达到高温条件,说明该反应可能属于
(5)如图为其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响。当煅烧温度达

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】金属制品与我们的日常生活密不可分。
(1)钢铁是应用最普遍的金属材料,某些铁制零件防锈措施是涂油,其防锈原理是_______ 。
(2)铝的化学性质比铁活泼,但是铝制品具有很好的防腐蚀性能,其原因是铝表面容易形成_______ 。
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是_______
①Zn、CuSO4溶液、Ag ②ZnSO4溶液、Cu、AgNO3溶液 ③Zn、Cu、AgNO3溶液
(4)将一定量的铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。滤渣中一定含有____ ,滤液中溶质的组成可能是_____ 或____ (填化学式)。
(1)钢铁是应用最普遍的金属材料,某些铁制零件防锈措施是涂油,其防锈原理是
(2)铝的化学性质比铁活泼,但是铝制品具有很好的防腐蚀性能,其原因是铝表面容易形成
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是
①Zn、CuSO4溶液、Ag ②ZnSO4溶液、Cu、AgNO3溶液 ③Zn、Cu、AgNO3溶液
(4)将一定量的铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。滤渣中一定含有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途以含锌废渣(主要成分为ZnO,杂质为FeO、CuO)为原料制备七水硫酸锌(ZnSO4•7H2O)的流程如图。

(1)粉碎的目的是_____ 。
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管、玻璃棒、_____ 和_____ ,此处玻璃棒的作用是_____ 。
(3)物质X是_____ ,滤渣中含有的金属单质有_____ ,除铜时发生的反应属于_____ 反应(填基本反应类型)
(4)流程中获得七水硫酸锌前省略的操作是_____ 、冷却结晶、_____ 、洗涤和低温烘干。
(5)某温度下,Fe(OH)3分解得到一种铁、氧质量比21:8的氧化物,该氧化物的化学式_____ 。
(6)除铁过程中,温度、pH对除铁效果的影响分别对如图所示.由如图可知,除铁时温度应控制在_____ ℃为宜,pH应控制在_____ 。为宜。

(1)粉碎的目的是
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管、玻璃棒、
(3)物质X是
(4)流程中获得七水硫酸锌前省略的操作是
(5)某温度下,Fe(OH)3分解得到一种铁、氧质量比21:8的氧化物,该氧化物的化学式
(6)除铁过程中,温度、pH对除铁效果的影响分别对如图所示.由如图可知,除铁时温度应控制在
您最近一年使用:0次





