为了测定某石灰石的纯度,某研究学习小组取用 6g石灰石样品,用实验室不知溶质质量分数的稀盐酸50g。分四次加入,每次充分反应后,经过滤、干燥等操作后称量剩余固体的质量(假设过滤、干燥等操作中固体物质的质量不损耗),有关物质质量见下表:
计算:
(1)石灰石的纯度为_____ 。
(2)所用稀盐酸的溶质质量分数?______
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入12.5g | 4.5g |
| 第二次加入12.5g | 3g |
| 第三次加入12.5g | 1.5g |
| 第四次加入12.5g | 0.6g |
计算:
(1)石灰石的纯度为
(2)所用稀盐酸的溶质质量分数?
更新时间:2021-10-23 16:52:23
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】兴趣小组的同学想测定某石灰石样品中碳酸钙的质量分数,他们取9克石灰石于烧杯中并慢慢加入盐酸,测得反应过程剩余固体质量与加入盐酸的质量关系如下图所示(石灰石中的杂质不与盐酸反应也不溶于水)

请回答下列问题:
(1)石灰石中所含杂质的质量是_____g
(2)通过计算求所用石灰石中含碳酸钙的质量分数以及生成二氧化碳质量_____、_____(该结果精确到0.1g)
(3)当加入_____克盐酸时,反应恰好停止。
(4)根据以上数据画出产生的气体与加入的盐酸质量的关系图__________。

请回答下列问题:
(1)石灰石中所含杂质的质量是_____g
(2)通过计算求所用石灰石中含碳酸钙的质量分数以及生成二氧化碳质量_____、_____(该结果精确到0.1g)
(3)当加入_____克盐酸时,反应恰好停止。
(4)根据以上数据画出产生的气体与加入的盐酸质量的关系图__________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解,蛋壳中的其它成分不与盐酸反应),实验测得烧杯中剩余物质的质量与加入盐酸的质量的关系如图所示,求:

(1)产生CO2的总质量为_____g。
(2)鸡蛋壳中碳酸钙的质量分数_____。
(3)反应到B点时,烧杯中含有的物质(蛋壳中的其它成分除外)有水和_____、_____。(写化学式)

(1)产生CO2的总质量为_____g。
(2)鸡蛋壳中碳酸钙的质量分数_____。
(3)反应到B点时,烧杯中含有的物质(蛋壳中的其它成分除外)有水和_____、_____。(写化学式)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】石灰石的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定石灰石中碳酸钙的含量,做如下实验。反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。
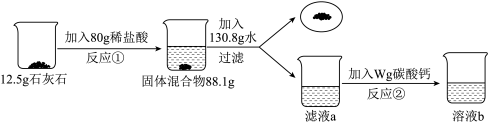
请回答下列问题:
(1)反应①的化学方程式为___________________________ ;
(2)根据已知条件列出求解反应①碳酸钙质量(X)的比例式______________ ;
(3)该石灰石中碳酸钙的质量分数为_______ ;
(4)溶液 b 中溶质的质量分数为_______ ;
(5)用 36.5%的浓盐酸配制 80g 上述稀盐酸需加水的质量为_______ ;
(6)W 的数值为_______ 。

请回答下列问题:
(1)反应①的化学方程式为
(2)根据已知条件列出求解反应①碳酸钙质量(X)的比例式
(3)该石灰石中碳酸钙的质量分数为
(4)溶液 b 中溶质的质量分数为
(5)用 36.5%的浓盐酸配制 80g 上述稀盐酸需加水的质量为
(6)W 的数值为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】计算与分析题:
(1)“钙尔奇”是一种补钙的药物,它的主要成分是碳酸钙,为了测定钙尔奇中碳酸钙的含量,小丽称取30g干燥的钙尔奇放入烧杯中,并向其中加入了80g稀盐酸恰好完全反应(假设钙尔奇中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量为101.2g。我能完成下列计算:
①钙尔奇中碳酸钙的质量______;
②当碳酸钙恰好完全反应时所得溶液中溶质的质量分数_____。(结果保留一位小数)
(2)有两种外观类似黄金的①Cu-Zn合金和②Cu-Ag合金制品,若实验室只提供一瓶稀硫酸和必要仪器。你认为能测出合金____(填序号)中铜的质量分数;
取上述题干中的合金粉末22g放入烧杯中,加入100g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为121.8g。求:
①产生氢气的质量_____;
②求出该合金中铜的质量 ________。
③反应后所得溶液的溶质质量分数是多少________?(保留一位小数)·
(1)“钙尔奇”是一种补钙的药物,它的主要成分是碳酸钙,为了测定钙尔奇中碳酸钙的含量,小丽称取30g干燥的钙尔奇放入烧杯中,并向其中加入了80g稀盐酸恰好完全反应(假设钙尔奇中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量为101.2g。我能完成下列计算:
①钙尔奇中碳酸钙的质量______;
②当碳酸钙恰好完全反应时所得溶液中溶质的质量分数_____。(结果保留一位小数)
(2)有两种外观类似黄金的①Cu-Zn合金和②Cu-Ag合金制品,若实验室只提供一瓶稀硫酸和必要仪器。你认为能测出合金____(填序号)中铜的质量分数;
取上述题干中的合金粉末22g放入烧杯中,加入100g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为121.8g。求:
①产生氢气的质量_____;
②求出该合金中铜的质量 ________。
③反应后所得溶液的溶质质量分数是多少________?(保留一位小数)·
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入192.0g某浓度的稀硫酸,恰好完全反应,最终所得溶液质量为200.0g。(已知:CuO+H2SO4=CuSO4+H20)
(1)所取样品中含铜的质量为 g.
(2)计算最终所得溶液中溶质的质量分数。(请写出计算过程)
(1)所取样品中含铜的质量为 g.
(2)计算最终所得溶液中溶质的质量分数。(请写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为测定某稀硫酸的溶质质量分数,小华取一定量碳酸钠放入烧杯中,称量烧杯及碳酸钠的总质量为121.2g,将150g稀硫酸分五次加入烧杯中,并称量每次反应后烧杯及烧杯内物质的总质量,数据如下表,请根据相关知识和数据回答下列问题:
(1)碳酸钠的水溶液显___________ (填“酸”、“碱”或“中”)性。
(2)反应完全后产生气体的质量为___________ g。
(3)该稀硫酸的溶质质量分数是多少?(结果精确到0.1%)
| 实验次数 | 加入稀硫酸的质量/g | 反应后烧杯及烧杯内物质的总质量/g |
| 1 | 30 | 150.1 |
| 2 | 30 | 179 |
| 3 | 30 | 207.9 |
| 4 | 30 | 236.8 |
| 5 | 30 | 266.8 |
(1)碳酸钠的水溶液显
(2)反应完全后产生气体的质量为
(3)该稀硫酸的溶质质量分数是多少?(结果精确到0.1%)
您最近一年使用:0次



