实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。
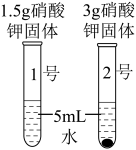
【定性研究】同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。要使2号试管中的固体全部溶解,可采取的方法有______ 。(列举一条即可)。
【定量研究】实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下:
请根据数据进行分析:
(1)请计算实验2所得溶液中硝酸钾的质量分数是____________ 。
(2)现将实验2中的溶液稀释成10%的硝酸钾溶液,需要加水的质量为____________ g。
(3)请判断实验2中硝酸钾溶液是____________ 溶液。(选填“饱和”或“不饱和”)
(4)实验4中M的数值是____________ 。

【定性研究】同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。要使2号试管中的固体全部溶解,可采取的方法有
【定量研究】实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下:
| 实验序号 | 实验1 | 实验2 | 实验3 | 实验4 |
| 水的质量(g) | 100 | 100 | 100 | 100 |
| 加入硝酸钾的质量(g) | 80 | 100 | 120 | 140 |
| 溶液质量(g) | 180 | 200 | 210 | M |
(1)请计算实验2所得溶液中硝酸钾的质量分数是
(2)现将实验2中的溶液稀释成10%的硝酸钾溶液,需要加水的质量为
(3)请判断实验2中硝酸钾溶液是
(4)实验4中M的数值是
21-22九年级上·山东青岛·期中 查看更多[6]
(已下线)第九单元 溶液(单元检测卷)-2022-2023学年九年级化学下册精品课堂课件精讲及好题精练(人教版)(已下线)课题3 溶液的浓度-2022-2023学年九年级化学下册教材知识点梳理讲练测(人教版)(已下线)第九单元 溶液(B卷能力提升练)-【单元测试】2022-2023学年九年级化学下册分层训练AB卷(天津专用)山东省青岛市四校联考2021-2022学年九年级上学期期中化学试题(已下线)第3单元 走进溶液世界(A卷·基础过关练)-2022-2023学年九年级化学上学期单元AB卷(沪教版.上海)山东省青岛市市北区2021-2022学年九年级上学期期中化学试题
更新时间:2021-11-08 13:25:09
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】在“探究稀盐酸和稀硫酸的化学性质”实验中,小科发现镁带与稀盐酸反应后的试管内出现了灰白沉淀。
【提出问题】灰白色沉淀是什么物质?
【提出猜想】小科在老师指导下,猜想灰白色沉淀是下列物质中的一种或几种:
①镁;②氯化镁;③氢氧化镁;④碱式氯化镁[Mg(OH)Cl]。
老师肯定了小科的猜想,并鼓励他继续进行实验探究。
【实验探究】步骤一:将上述镁带与稀盐酸反应后试管内的物质过滤,得到滤液和灰白色滤渣。
步骤二:取滤液于试管中,加入适量的氯化镁粉末,粉末全部溶解。
步骤三:取少量灰白色滤渣于试管中,加入适量稀盐酸,沉淀全部溶解,无其他现象。
步骤四:将剩余滤渣用蒸馏水充分洗涤。取洗涤后的滤渣于试管中,加入过量稀硝酸,滤渣全部溶解,再加入硝酸银溶液,有白色沉淀产生。
【实验反思及结论】
(1)从步骤二可知,灰白色沉淀不可能是氯化镁,因为滤液是氯化镁的_____ (填“饱和”或“不饱和”)溶液。
(2)从步骤三可知,该沉淀中没有_____ 。
(3)步骤四中将滤渣用蒸馏水充分洗涤是为了_____ 。
(4)根据实验探究可知,该反应产生的灰白色沉淀中一定含有_____ 。
【提出问题】灰白色沉淀是什么物质?
【提出猜想】小科在老师指导下,猜想灰白色沉淀是下列物质中的一种或几种:
①镁;②氯化镁;③氢氧化镁;④碱式氯化镁[Mg(OH)Cl]。
老师肯定了小科的猜想,并鼓励他继续进行实验探究。
【实验探究】步骤一:将上述镁带与稀盐酸反应后试管内的物质过滤,得到滤液和灰白色滤渣。
步骤二:取滤液于试管中,加入适量的氯化镁粉末,粉末全部溶解。
步骤三:取少量灰白色滤渣于试管中,加入适量稀盐酸,沉淀全部溶解,无其他现象。
步骤四:将剩余滤渣用蒸馏水充分洗涤。取洗涤后的滤渣于试管中,加入过量稀硝酸,滤渣全部溶解,再加入硝酸银溶液,有白色沉淀产生。
【实验反思及结论】
(1)从步骤二可知,灰白色沉淀不可能是氯化镁,因为滤液是氯化镁的
(2)从步骤三可知,该沉淀中没有
(3)步骤四中将滤渣用蒸馏水充分洗涤是为了
(4)根据实验探究可知,该反应产生的灰白色沉淀中一定含有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某实验小组用石墨做电极进行电解水实验,为增加导电性,改用氢氧化钙饱和溶液进行电解,实验时除两个电极均有气泡冒出外,在正极石墨电极的附近溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
[资料]
Ⅰ.氢氧化钙的溶解度曲线如图所示。

Ⅱ.氢氧化钙饱和溶液通电后温度约上升5℃。
[猜想]
①电解过程中溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
②电解过程中水减少导致Ca(OH)2析出而出现白色浑浊。
③与石墨电极(主要成分是碳)有关。
[实验]
(1)Ca(OH)2的溶液度随温度升高而__________ (填“减少”或“增大”);实验1中当液温度上升5℃后得到的溶液为Ca(OH)2 __________ (填“饱和”或“不饱和”)溶液。
(2)实验1得出的结论是___________________________________________________________ 。
(3)实验2,取b试管中白色浑浊溶液,加10mL水,振荡,发现试管中白色浑浊不溶解,据此证明猜想_______ (填序号)不合理。
(4)实验3中更换石墨电极为铜电极的目的是__________________________________________ ;与电源正极相连的铜电极变黑的原因是 _____________________________________________ (用化学方程式表示);为除去铜电极上的黑色物质,需要的试剂是 _____________ (写一种即可)。
(5)通过探究过程,用石墨做电极进行实验时,正极石墨电极附近Ca(OH)2溶液出现白色浑浊的原因是__________________________________________________________________________ 。
[资料]
Ⅰ.氢氧化钙的溶解度曲线如图所示。

Ⅱ.氢氧化钙饱和溶液通电后温度约上升5℃。
[猜想]
①电解过程中溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
②电解过程中水减少导致Ca(OH)2析出而出现白色浑浊。
③与石墨电极(主要成分是碳)有关。
[实验]
| 实验 | 实验装置 | 主要实验操作 | 实验现象 |
| 1 | 取10mL Ca(OH)2饱和溶液,稍加热,溶液温度上升5℃ | 溶液中未出现白色浑浊 | |
| 2 |  | 用石墨做电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生;a试管中溶液未出现白色浑浊;b试管中溶液明显出现白色浑浊 |
| 3 | 更换石墨电极为铜电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生;与电源正极相连的铜电极变黑,a、b试管中溶液未出现白色浑浊 |
(1)Ca(OH)2的溶液度随温度升高而
(2)实验1得出的结论是
(3)实验2,取b试管中白色浑浊溶液,加10mL水,振荡,发现试管中白色浑浊不溶解,据此证明猜想
(4)实验3中更换石墨电极为铜电极的目的是
(5)通过探究过程,用石墨做电极进行实验时,正极石墨电极附近Ca(OH)2溶液出现白色浑浊的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】在人类的生活、生产活动中处处离不开溶液。如图是硝酸钾和食盐两种固体物质的溶解度曲线。

(1)硝酸钾溶液中的溶剂是___________ 。
(2)___________ ℃时,上述两种物质的溶解度相等。
(3) t3℃,将等质量的硝酸钾和食盐固体加水溶解配制成饱和溶液,所得溶液的质量关系为:硝酸钾___________ 食盐(填“>”、“<”或“=”)。
(4)把硝酸钾的不饱和溶液变为饱和溶液,下列有关说法正确的是___________ (填序号)。
A 溶剂的质量一定变小
B 溶质的质量可能不变
C 溶液的溶质质量分数一定变大
D 溶液的质量一定变大
E 该饱和溶液还可以溶解其他物质
(5)硝酸钾中混有少量的氯化钠,想要得到纯净的硝酸钾的方法是___________ 。
(6)t1℃时,向l00g水中加入25g氯化钠,充分溶解后,得到的溶液为___________ (填“饱和”或“不饱和”)溶液,溶液中溶质质量分数为___________ 。
(7)通常情况下,在实验室用固体硝酸钾配制一定溶质质量分数的硝酸钾溶液,需用到的仪器有:托盘天平(含砝码)、烧杯和___________ (填序号)。
A 酒精灯 B 药匙 C 玻璃棒 D 漏斗 E 铁架台 F 量筒 G 胶头滴管

(1)硝酸钾溶液中的溶剂是
(2)
(3) t3℃,将等质量的硝酸钾和食盐固体加水溶解配制成饱和溶液,所得溶液的质量关系为:硝酸钾
(4)把硝酸钾的不饱和溶液变为饱和溶液,下列有关说法正确的是
A 溶剂的质量一定变小
B 溶质的质量可能不变
C 溶液的溶质质量分数一定变大
D 溶液的质量一定变大
E 该饱和溶液还可以溶解其他物质
(5)硝酸钾中混有少量的氯化钠,想要得到纯净的硝酸钾的方法是
(6)t1℃时,向l00g水中加入25g氯化钠,充分溶解后,得到的溶液为
(7)通常情况下,在实验室用固体硝酸钾配制一定溶质质量分数的硝酸钾溶液,需用到的仪器有:托盘天平(含砝码)、烧杯和
A 酒精灯 B 药匙 C 玻璃棒 D 漏斗 E 铁架台 F 量筒 G 胶头滴管
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】高锰酸钾在生产、生活中有广泛应用。实验小组对高锰酸钾进行研究。
(1)①如图所示进行实验,高锰酸钾受热分解的化学方程式为_______ 。

②取一定量的高锰酸钾固体,充分加热,发现实际产生氧气的质量远高于理论数值。则可能的原因有_______ (测定过程中产生的误差可忽略)。
(2)浓度为0.05%的高锰酸钾溶液有消炎、防感染扩散等作用。
①若用10g1%的高锰酸钾溶液稀释成0.05%的高锰酸钾溶液需要蒸馏水_______ mL(水的密度是1g/mL)。
②在量取蒸馏水时,若俯视读数,则会导致高锰酸钾溶液得溶质质量分数_______ (选填“大于”或“小于”)0.05%。
(3)经查阅资料得知KMnO4溶液呈中性、有腐蚀性,小组成员进行了以下实验:将铜片分别浸泡在4种不同的溶液中18小时,现象如下表。
【解释与结论】
①通过对比实验Ⅱ和Ⅳ,得出的结论是_______ 。
②欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要进行对比实验的编号为_______ 。
③该实验中铜片被腐蚀的反应如下,补全该反应的化学方程式:

______
(1)①如图所示进行实验,高锰酸钾受热分解的化学方程式为

②取一定量的高锰酸钾固体,充分加热,发现实际产生氧气的质量远高于理论数值。则可能的原因有
(2)浓度为0.05%的高锰酸钾溶液有消炎、防感染扩散等作用。
①若用10g1%的高锰酸钾溶液稀释成0.05%的高锰酸钾溶液需要蒸馏水
②在量取蒸馏水时,若俯视读数,则会导致高锰酸钾溶液得溶质质量分数
(3)经查阅资料得知KMnO4溶液呈中性、有腐蚀性,小组成员进行了以下实验:将铜片分别浸泡在4种不同的溶液中18小时,现象如下表。
| 编号 | Ⅰ | Ⅱ | Ш | Ⅳ | |
| 实验 | 25mL、0.1% KMnO4溶液 | 25mL、0.1% KMnO4溶液 +10滴浓硫酸 | 25mL蒸馏水+10滴浓硫酸 | 25mL、1% KMnO4溶液 +10滴浓硫酸 | |
| 铜片质量 | 实验前 | 0.54g | 0.54g | 0.54g | 0.54g |
| 实验后 | 0.54g | 0.52g | 0.54g | 0.43g | |
①通过对比实验Ⅱ和Ⅳ,得出的结论是
②欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要进行对比实验的编号为
③该实验中铜片被腐蚀的反应如下,补全该反应的化学方程式:

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”:
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100mL10%的盐酸(密度为1.05g/mL)
实验步骤:
(1)计算:需要37%的浓盐酸的体积为________________ mL(精确到0.01mL,下同);需要蒸馏水的体积为________________ mL(水的密度为1.0g/mL);
量取浓盐酸和蒸馏水;
混合配制;
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
(2)表中 的值为
的值为________________ ;
(3)试绘出溶液温度变化与加入盐酸体积之间的关系图;
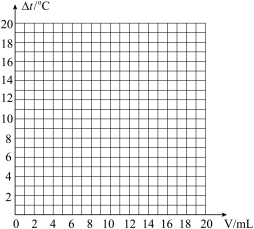
(4)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是________ ;
(5)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素):
横坐标及猜想理由:________________ ;
纵坐标及猜想理由:________________ 。
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100mL10%的盐酸(密度为1.05g/mL)
实验步骤:
(1)计算:需要37%的浓盐酸的体积为
量取浓盐酸和蒸馏水;
混合配制;
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
| 加入盐酸的体积(V)/mL | 1 | 2 | 4 | 6 | 8 | 10 |
溶液温度变化 |  | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 |
| 加入盐酸的体积(V)/mL | 12 | 14 | 16 | 18 | 20 | |
溶液温度变化 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
(2)表中
 的值为
的值为(3)试绘出溶液温度变化与加入盐酸体积之间的关系图;

(4)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是
(5)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素):
横坐标及猜想理由:
纵坐标及猜想理由:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】无土栽培是一种新型农业生产技术。无土栽培的重要物质是植物生长营养液。兴趣小组对一瓶用于番茄无土栽培的营养液展开了研究。已知该浓缩营养液的配方如下:
(1)该番茄无土栽培营养液成分中属于复合肥的是________________ 。
(2)NH4NO3________ (填“能”或“不能”)与常见的碱性农家肥草木灰(主要成分K2CO3)混合使用。
(3)小林取少量营养液B于试管中,向其中滴加无色酚酞溶液,观察到________________ ,证明营养液B呈酸性。
【质疑评价】
(4)鹏鹏对小林的结论产生了质疑,理由是________________ ;为证明小林的结论正确,应将操作方法修改为________________ 。
(5)营养液不能直接用于蔬菜种植,需加水稀释。经检测,小方稀释的溶液溶质质量分数偏小,可能的原因是 (填字母序号)。
(6)KNO3、K2SO4均为白色晶体,请写出鉴别这两种物质的实验方案:________________ 。
(7)实验室要配制100g溶质质量分数为16%的硝酸钾溶液,现有80g溶质质量分数为20%的硝酸钾溶液、80g溶质质量分数为10%的硝酸钾溶液及足够多的硝酸钾晶体和蒸馏水,请选用上述药品,再设计两种配制方案填入下表。
番茄无土栽培营养液配方(用量单位:mg/L) | |||||
MgSO4 | Ca(NO3)2 | KNO3 | KH2PO4 | NH4NO3 | K2SO4 |
466 | 1216 | 395 | 208 | 42.1 | 395 |
(2)NH4NO3
(3)小林取少量营养液B于试管中,向其中滴加无色酚酞溶液,观察到
【质疑评价】
(4)鹏鹏对小林的结论产生了质疑,理由是
(5)营养液不能直接用于蔬菜种植,需加水稀释。经检测,小方稀释的溶液溶质质量分数偏小,可能的原因是 (填字母序号)。
| A.溶解时烧杯内壁有水珠 |
| B.量取溶剂时,仰视读数 |
| C.装瓶时有少量溶液洒出 |
(7)实验室要配制100g溶质质量分数为16%的硝酸钾溶液,现有80g溶质质量分数为20%的硝酸钾溶液、80g溶质质量分数为10%的硝酸钾溶液及足够多的硝酸钾晶体和蒸馏水,请选用上述药品,再设计两种配制方案填入下表。
配制方案(只要说明配制时所需的各种药品及用量即可) | |
方案一 | 16g硝酸钾和84g水 |
方案二 | |
方案三 |
您最近一年使用:0次



