人教版新课标化学九年级上册教材中“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?如果能,其效果如何?
【实验结论】
(1)实验Ⅱ、Ⅲ证明:氧化铁的______ 和______ 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(2)写出氧化铁催化过氧化氢分解的文字表达式:______ 。
【实验评价】
(3)设计实验Ⅳ的目的是______ 。
(4)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此可以得到的结论是______ 。
【实验延伸】
(5)二氧化锰还可以作为氯酸钾制取氧气的催化剂,请写出该反应的文字表达式:______ 。
(6)测定空气中氧气的含量,通常会选择红磷进行反应,请写出红磷燃烧的文字表达式:______ 。
【提出问题】氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?如果能,其效果如何?
| 实验步骤 | 实验现象 |
| Ⅰ、分别量取5 mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象 |
| Ⅱ、待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
| Ⅲ、将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
| Ⅳ、分别量取5 mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
【实验结论】
(1)实验Ⅱ、Ⅲ证明:氧化铁的
(2)写出氧化铁催化过氧化氢分解的文字表达式:
【实验评价】
(3)设计实验Ⅳ的目的是
(4)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此可以得到的结论是
【实验延伸】
(5)二氧化锰还可以作为氯酸钾制取氧气的催化剂,请写出该反应的文字表达式:
(6)测定空气中氧气的含量,通常会选择红磷进行反应,请写出红磷燃烧的文字表达式:
更新时间:2021-11-18 22:44:35
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】学习了二氧化锰对过氧化氢分解有催化作用的知识后,我们对催化剂已有了初步的认识。某同学想:氧化铜(CuO)能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
【猜想】
Ⅰ、氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生改变;
Ⅲ、氧化铜是反应的催化剂,反应前后______ 。
【实验】
用天平称量 0.2 g CuO,取 5 mL 5%的过氧化氢溶液于试管中,进行如图实验:
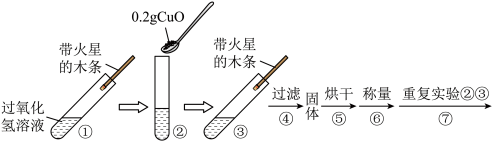
【结论】 猜想Ⅲ成立。
(1)请补充能证明猜想Ⅲ成立的实验现象:步骤③现象为______ ,步骤⑥中固体质量为______ g。
(2)步骤⑦的目的是______ 。
(3)过氧化氢能被 CuO 催化分解放出 O2的文字表达式为______ 。
【拓展探究】
(4)欲比较催化剂氧化铜和二氧化锰对过氧化氢分解速率的影响,实验时需要控制相同的量有______ (填字母序号)。
A.过氧化氢溶液的浓度、体积 B.过氧化氢溶液的温度
C.催化剂的质量 D.催化剂的种类
【猜想】
Ⅰ、氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生改变;
Ⅲ、氧化铜是反应的催化剂,反应前后
【实验】
用天平称量 0.2 g CuO,取 5 mL 5%的过氧化氢溶液于试管中,进行如图实验:

【结论】 猜想Ⅲ成立。
(1)请补充能证明猜想Ⅲ成立的实验现象:步骤③现象为
(2)步骤⑦的目的是
(3)过氧化氢能被 CuO 催化分解放出 O2的文字表达式为
【拓展探究】
(4)欲比较催化剂氧化铜和二氧化锰对过氧化氢分解速率的影响,实验时需要控制相同的量有
A.过氧化氢溶液的浓度、体积 B.过氧化氢溶液的温度
C.催化剂的质量 D.催化剂的种类
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】击新冠肺炎疫情是一项长期的工作,我们要采取有效防疫措施免受病毒侵害。医用口罩、84消毒液、过氧化氢消毒剂和医用酒精在新冠病毒防疫中起到重要的作用。


(1)一次性医用三层口罩是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到_____ (填一种实验操作名称)作用。
(2)84消毒液的成分为次氯酸钠(NaClO)、表面活性剂和水等,次氯酸钠中氯元素的化合价为_____ 。
(3)某兴趣小组对84消毒液和过氧化氢消毒剂进行如下探究活动。
【实验1】取少量84消毒液于试管中,滴加过氧化氢消毒剂,发现有大量气泡产生;然后________ (填写实验操作和现象),证明产生的气体是氧气。
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】
猜想一:作反应物,NaClO与过氧化氢消毒剂发生化学反应;
猜想二:作催化剂,与分解过氧化氢溶液制氧气时二氧化锰类似。
【实验2】①按图2所示组装实验装置,并_____ 。
②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL过氧化氢溶液。
③将注射器中的过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见表。
分析表中数据得出“猜想一正确”,其依据是_____ 。
【拓展反思】生活中常用的消毒剂除84消毒液、过氧化氢消毒剂外,还有医用酒精、过氧乙酸等,在使用各种消毒剂时,要考虑它们的性质,切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是_____ 。
A不同的消毒剂可随意混合使用
B使用84消毒液的浓度越高越好
C使用医用酒精消毒应远离明火,防止火灾
D 84消毒液、医用酒精等消毒剂均应密封保存


(1)一次性医用三层口罩是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到
(2)84消毒液的成分为次氯酸钠(NaClO)、表面活性剂和水等,次氯酸钠中氯元素的化合价为
(3)某兴趣小组对84消毒液和过氧化氢消毒剂进行如下探究活动。
【实验1】取少量84消毒液于试管中,滴加过氧化氢消毒剂,发现有大量气泡产生;然后
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】
猜想一:作反应物,NaClO与过氧化氢消毒剂发生化学反应;
猜想二:作催化剂,与分解过氧化氢溶液制氧气时二氧化锰类似。
【实验2】①按图2所示组装实验装置,并
②向锥形瓶中加入30mL 84消毒液,注射器中吸入25mL过氧化氢溶液。
③将注射器中的过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见表。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 收集气体的总体积/mL | 140 | 280 | 365 | 370 | 375 |
【拓展反思】生活中常用的消毒剂除84消毒液、过氧化氢消毒剂外,还有医用酒精、过氧乙酸等,在使用各种消毒剂时,要考虑它们的性质,切记:科学使用,注意安全!生活中下列使用消毒剂的做法正确的是
A不同的消毒剂可随意混合使用
B使用84消毒液的浓度越高越好
C使用医用酒精消毒应远离明火,防止火灾
D 84消毒液、医用酒精等消毒剂均应密封保存
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】同学们知道KClO3分解用MnO2作催化剂,于是想研究氧化铜能否对KClO3分解起催化作用,进行了以下实验:
【实验一】氧化铜能否在氯酸钾制取氧气的实验中加快反应速率。
(1)实验③中加CuO的质量X应该为________ g,以上实验采用了对照实验的探究方法,其中①和③对照,说明的结论是____________________ ;
(2)写出实验③反应的化学方程式____________________ ;
【实验二】为了证明CuO是KClO3的催化剂,同学们完成以下实验:
【资料】KClO3和KCl都溶于水,CuO难溶于水。
Ⅰ、将实验③反应后的剩余固体加足量的水溶解,过滤得到黑色粉末,洗涤干燥称得质量为0.3g。
Ⅱ、将过滤得到的黑色粉末按下面进行实验:
(3)写出玻璃管中发生的反应的化学方程式____________________ ;说明滤出的固体是________ ;
【实验结论】
(4)通过上述实验,得出的结论是____________________ ;
【实验反思】
(5)在实验Ⅱ的实验装置设计中存在一定的缺陷,改进的方法是____________________ 。
【实验一】氧化铜能否在氯酸钾制取氧气的实验中加快反应速率。
| 实验编号 | 氯酸钾(g) | 氧化物 | 产生气体(mL) | 耗时(s) |
| ① | 1.5 | —— | 50 | 1800 |
| ② | 1.5 | 0.3gMnO2 | 50 | 40 |
| ③ | 1.5 | XgCuO | 50 | 85 |
(1)实验③中加CuO的质量X应该为
(2)写出实验③反应的化学方程式
【实验二】为了证明CuO是KClO3的催化剂,同学们完成以下实验:
【资料】KClO3和KCl都溶于水,CuO难溶于水。
Ⅰ、将实验③反应后的剩余固体加足量的水溶解,过滤得到黑色粉末,洗涤干燥称得质量为0.3g。
Ⅱ、将过滤得到的黑色粉末按下面进行实验:
| 实验装置 | 实验现象 | 实验分析 |
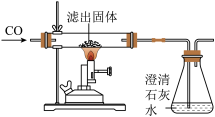 | 玻璃管中黑色粉末逐渐变红 | 有铜产生 |
| 锥形瓶中澄清的石灰水变浑浊 | 产生了CO2 |
(3)写出玻璃管中发生的反应的化学方程式
【实验结论】
(4)通过上述实验,得出的结论是
【实验反思】
(5)在实验Ⅱ的实验装置设计中存在一定的缺陷,改进的方法是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:
【实验一】实验目的:探究氧化铜是否能改变过氧化氢分解的速率.
结论:氧化铜能加快过氧化氢的分解速率。
【实验二】实验目的:______ 。
结论:氧化铜的化学性质在化学反应前后没有发生改变。
【实验三】实验目的:探究氧化铜的质量在化学反应前后有没有改变。
在实验后,该同学将反应剩余物过滤、洗涤、干燥,再称量,得到黑色固体质量为1g。
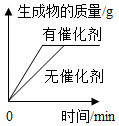
结论:氧化铜的____ 在化学反应前后没有发生改变。
【实验结论】
(1)综上所述,说明了氧化铜是过氧化氢溶液分解的催化剂.请写出该实验中过氧化氢溶液分解反应的化学方程式_____ 。
(2)某同学画出如图,表示有、无催化剂时,生成物质量与反应时间的关系图,你认为是否正确?______ 。
【实验一】实验目的:探究氧化铜是否能改变过氧化氢分解的速率.
| 1.在试管中加入2ml5%的过氧化氢溶液,将带火星的木条伸入试管中,观察现象 | 1.带火星的木条没有明显变化 |
| 2.取1gCuO粉末放在 | 2.带火星的木条复燃 |
【实验二】实验目的:
| 实验步骤 | 实验现象 |
| 待实验一第2步的试管中没有气泡时,重新加入2ml过氧化氢溶液,观察现象 |
【实验三】实验目的:探究氧化铜的质量在化学反应前后有没有改变。
在实验后,该同学将反应剩余物过滤、洗涤、干燥,再称量,得到黑色固体质量为1g。

结论:氧化铜的
【实验结论】
(1)综上所述,说明了氧化铜是过氧化氢溶液分解的催化剂.请写出该实验中过氧化氢溶液分解反应的化学方程式
(2)某同学画出如图,表示有、无催化剂时,生成物质量与反应时间的关系图,你认为是否正确?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某同学研究“影响过氧化氢生成氧气快慢的因素”,查阅资料,猜想如下:
【提出猜想】催化剂种类和反应物浓度都会影响过氧化氢生成氧气的快慢。
【实验操作】检查装置气密性良好,用排水法收集等体积的一瓶氧气,记录收集气体时间。
【实验记录】
(1)写出实验②中反应的文字表达式______________________________ 。
(2)实验②中加入过氧化氢的体积为__________ mL。
(3)实验③中加入的固体和用量为____________________ 。
【结论】
(4)该探究过程得出的结论______________________________ 。
【反思】
(5)过氧化氢溶液在常温下分解缓慢,加入二氧化锰后反应明显加快。小红提出,为了更好的证明二氧化锰和氯化钠是否对过氧化氢生成氧气快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为______________________________ 。
【拓展】
(6)若要测定相同时间内所产生氧气体积,如图装置应选__________ (填序号),测定气体前集气瓶内未装满水,对实验结果__________ (填“有”或“没有”)影响。

【提出猜想】催化剂种类和反应物浓度都会影响过氧化氢生成氧气的快慢。
【实验操作】检查装置气密性良好,用排水法收集等体积的一瓶氧气,记录收集气体时间。
【实验记录】
| 实验编号 | ① | ② | ③ |
| 反应物 | 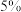 过氧化氢溶液 过氧化氢溶液 | 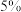 过氧化氢溶液_______ 过氧化氢溶液_______ | 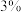 过氧化氢溶液100mL 过氧化氢溶液100mL |
| 加入固体 | 0.5g氯化钠固体 | 0.5g二氧化锰 | ____________ |
| 收集气体时间 |  | 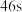 | 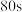 |
(1)写出实验②中反应的文字表达式
(2)实验②中加入过氧化氢的体积为
(3)实验③中加入的固体和用量为
【结论】
(4)该探究过程得出的结论
【反思】
(5)过氧化氢溶液在常温下分解缓慢,加入二氧化锰后反应明显加快。小红提出,为了更好的证明二氧化锰和氯化钠是否对过氧化氢生成氧气快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为
【拓展】
(6)若要测定相同时间内所产生氧气体积,如图装置应选

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】研究和控制化学反应条件有重要意义,同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
(1)小明在使用量筒量取40mL水时仰视刻度,则实际量取的水体积_____ (大于或者小于)40mL。
(2)实验3中,加入的二氧化锰质量M为_____ g;相同条件下,实验3产生氧气的速率最快,说明_____ 。
(3)同学通过查阅资料得知,双氧水加热时也会较快分解产生氧气,为了验证加热双氧水也可以产生氧气,同学们选择图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是_____ ,同学分析原因后,采用了_____ 法收集气体,再检验,证明加热双氧水也可产生氧气。

| 实验 | 双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 5 | 40 | 1 | 200 |
| 2 | 10 | 40 | 1 | 100 |
| 3 | 15 | 40 | M | 67 |
(2)实验3中,加入的二氧化锰质量M为
(3)同学通过查阅资料得知,双氧水加热时也会较快分解产生氧气,为了验证加热双氧水也可以产生氧气,同学们选择图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组用氯酸钾和二氧化锰混合加热制取氧气。
(1)反应中,二氧化锰加快了氯酸钾制氧气的反应速率。
①实验结束后,小利将二氧化锰分离出来并干燥,再与少量氯酸钾混合加热,伸入带火星的木条:小利的实验目的是_____ 。
②若要证明二氧化锰是氯酸钾分解制取氧气的催化剂,还需要补充实验,写出简单的实验步骤:_____ 。
③写出上述反应的文字表达式_____ 。
(2)小组同学发现上述制得的气体有刺激性气味,于是在老师的指导下对气体成分进行探究。
【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】
Ⅰ.氯酸钾与二氧化锰混合加热产生的气体可能含有两种成分;
Ⅱ.氯酸钾与二氧化锰混合加热产生的气体可能含有氯气;
Ⅲ.氯气是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
【猜想与假设】猜想一:该气体为氧气;
猜想二:该气体为氯气;
猜想三:该气体为_____ 。
【实验探究】
小涛认为小丽的结论不正确,原因是_____ 。
【实验结论】氯酸钾制取氧气得到的气体成分是氧气和氯气的混合物。
【反思与总结】某些反应可能会有副反应,生成少量其他物质。氯酸钾分解反应中有副反应,氯气就是副反应的生成物。
(3)二氧化锰不仅能作催化剂还可以作反应物,实验室常用二氧化锰与浓盐酸加热制取氯气,同时生成氯化锰和水。请完成该反应的文字表达式_____ 。
(1)反应中,二氧化锰加快了氯酸钾制氧气的反应速率。
①实验结束后,小利将二氧化锰分离出来并干燥,再与少量氯酸钾混合加热,伸入带火星的木条:小利的实验目的是
②若要证明二氧化锰是氯酸钾分解制取氧气的催化剂,还需要补充实验,写出简单的实验步骤:
③写出上述反应的文字表达式
(2)小组同学发现上述制得的气体有刺激性气味,于是在老师的指导下对气体成分进行探究。
【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】
Ⅰ.氯酸钾与二氧化锰混合加热产生的气体可能含有两种成分;
Ⅱ.氯酸钾与二氧化锰混合加热产生的气体可能含有氯气;
Ⅲ.氯气是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
【猜想与假设】猜想一:该气体为氧气;
猜想二:该气体为氯气;
猜想三:该气体为
【实验探究】
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 小丽用排水集气法收集A、B两瓶气体,将带火星木条伸入A中;湿润的淀粉碘化钾试纸伸入B中 | A中带火星木条复燃,B中淀粉碘化钾试纸不变色 | 猜想一成立 |
| 2 | 小岚用向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中 | C中带火星木条复燃,D中淀粉碘化钾试纸 | 猜想三成立 |
【实验结论】氯酸钾制取氧气得到的气体成分是氧气和氯气的混合物。
【反思与总结】某些反应可能会有副反应,生成少量其他物质。氯酸钾分解反应中有副反应,氯气就是副反应的生成物。
(3)二氧化锰不仅能作催化剂还可以作反应物,实验室常用二氧化锰与浓盐酸加热制取氯气,同时生成氯化锰和水。请完成该反应的文字表达式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】在“过氧化氢制取氧气的反应中二氧化锰的作用”的探究活动中老师和同学们一起进行了如下探究:
【活动与探究一】
实验(1):在试管中加入5mL5%过氧化氢溶液,把带火星的木条伸入试管,观察到木条不能复燃
实验(2):称量ag二氧化锰加入上述试管中,把带火星的木条伸入试管,观察到木条复燃了.

由此小何同学得出二氧化锰是这个化学变化中的催化剂.小苗同学认为小何同学的说法是错误的,小苗同学的理由是___ .
为了进一步探究二氧化锰是否是过氧化氢制氧气中的催化剂,小苗小组的同学进一步进行了如下探究.
查阅资料:过氧化氢溶液在常温下分解缓慢,放出的氧气很少.
设计实验方案:
由此得出利用过氧化氢和二氧化锰制氧气的化学反应式是___ .
【活动与探究二】
实验室中也可以利用分解氯酸钾来制取氧气,在实验中也用到了催化剂.下面两实验是为探究催化剂的种类对氯酸钾分解速度的影响.
甲:将3.0g 氯酸钾与1.0g 二氧化锰均匀混合加热
乙:将xg氯酸钾与1.0g氧化铜均匀混合加热
在相同温度下,比较两组实验产生氧气的快慢.
乙中的化学反应式是___ .
乙实验中x的值应为___ .
【活动与探究一】
实验(1):在试管中加入5mL5%过氧化氢溶液,把带火星的木条伸入试管,观察到木条不能复燃
实验(2):称量ag二氧化锰加入上述试管中,把带火星的木条伸入试管,观察到木条复燃了.

由此小何同学得出二氧化锰是这个化学变化中的催化剂.小苗同学认为小何同学的说法是错误的,小苗同学的理由是
为了进一步探究二氧化锰是否是过氧化氢制氧气中的催化剂,小苗小组的同学进一步进行了如下探究.
查阅资料:过氧化氢溶液在常温下分解缓慢,放出的氧气很少.
设计实验方案:
| 实验方案及现象 | 实验结论 |
| 实验(3):待实验(2)中试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,观察到木条又一次复燃了,重复上述实验多次,每次都出现相似的实验现象,二氧化锰好像永远用不完. | |
| 实验(4):待实验(3)结束后,将试管中的二氧化锰洗净、干燥,再称量,发现二氧化锰的质量约为ag |
由此得出利用过氧化氢和二氧化锰制氧气的化学反应式是
【活动与探究二】
实验室中也可以利用分解氯酸钾来制取氧气,在实验中也用到了催化剂.下面两实验是为探究催化剂的种类对氯酸钾分解速度的影响.
甲:将3.0g 氯酸钾与1.0g 二氧化锰均匀混合加热
乙:将xg氯酸钾与1.0g氧化铜均匀混合加热
在相同温度下,比较两组实验产生氧气的快慢.
乙中的化学反应式是
乙实验中x的值应为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是____ ;
Ⅱ中x的值应为____ 。
【反 思】
单独加热KClO3时反应缓慢,加入MnO2或CuO后反应明显加快,若要证明MnO2和CuO是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____ 和____ 是否改变。
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是
Ⅱ中x的值应为
【反 思】
单独加热KClO3时反应缓慢,加入MnO2或CuO后反应明显加快,若要证明MnO2和CuO是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
您最近一年使用:0次
【推荐1】中国是最早冶炼和使用金属铜的国家之一,古代炼铜有“湿法炼铜”和“火法炼铜”。
(1)①火法炼铜:古代人们就发现了在翠绿色的孔雀石(主要成分为 )上燃烧木炭会有红色的铜生成,该过程通过两步反应生成
)上燃烧木炭会有红色的铜生成,该过程通过两步反应生成 ,请写出第二步的化学方程式。
,请写出第二步的化学方程式。
第一步:
第二步:_______ (填化学方程式)。
②湿法炼铜:《梦溪笔谈》中记载“敖胆矾铁釜,久之亦化为铜”,胆矾化学式为 ,属于
,属于_______ (填“纯净物”或“混合物”),胆矾溶于水可得硫酸铜溶液,请写出“铁金化为铜”发生反应的化学方程式_______ (填化学方程式),观察到的现象是_______ 。
(2)铜在潮湿的空气中会生锈,产生铜锈(主要成分为: ),为探究铜生锈的条件,某实验小组设计了以下所示实验。
),为探究铜生锈的条件,某实验小组设计了以下所示实验。
【提出猜想】铜生锈可能与空气中的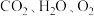 有关。
有关。
【进行实验】实验小组的同学取形状大小均相同的铜片,并打磨光亮.设计了如下图所示的4个实验并持续观察。
(注:所用蒸馏水都是经煮沸迅速冷却的;固体干燥剂只吸收水分,不吸收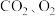 。)
。)
①为探究铜生锈是否与 有关,应选择实验
有关,应选择实验_______ (填编号)进行对照。
②为探究铜生锈是否与 有关,实验
有关,实验 试管中所加物质除了金属
试管中所加物质除了金属 和干燥剂外,还有
和干燥剂外,还有_______ (填化学式)。
【反思讨论】有同学认为无需上述的实验,依据_______ 定律也能推理出空气中的 和
和 肯定参加了铜生锈的反应。
肯定参加了铜生锈的反应。
(1)①火法炼铜:古代人们就发现了在翠绿色的孔雀石(主要成分为
 )上燃烧木炭会有红色的铜生成,该过程通过两步反应生成
)上燃烧木炭会有红色的铜生成,该过程通过两步反应生成 ,请写出第二步的化学方程式。
,请写出第二步的化学方程式。第一步:

第二步:
②湿法炼铜:《梦溪笔谈》中记载“敖胆矾铁釜,久之亦化为铜”,胆矾化学式为
 ,属于
,属于(2)铜在潮湿的空气中会生锈,产生铜锈(主要成分为:
 ),为探究铜生锈的条件,某实验小组设计了以下所示实验。
),为探究铜生锈的条件,某实验小组设计了以下所示实验。【提出猜想】铜生锈可能与空气中的
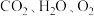 有关。
有关。【进行实验】实验小组的同学取形状大小均相同的铜片,并打磨光亮.设计了如下图所示的4个实验并持续观察。
| 编号 | A | B | C | D |
| 实验 | 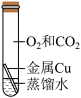 |  |  |  |
| 现象 | 铜丝表面出现铜锈 | 无明显现象 | 无明显现象 | 无明显现象 |
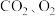 。)
。)①为探究铜生锈是否与
 有关,应选择实验
有关,应选择实验②为探究铜生锈是否与
 有关,实验
有关,实验 试管中所加物质除了金属
试管中所加物质除了金属 和干燥剂外,还有
和干燥剂外,还有【反思讨论】有同学认为无需上述的实验,依据
 和
和 肯定参加了铜生锈的反应。
肯定参加了铜生锈的反应。
您最近一年使用:0次
【推荐2】过氧化氢在二氧化锰的作用下可分解产生氧气。科学探究是一个奇妙的过程,请你一起参与实验探究,并填写下列空白。
(1)【提出问题】:小松同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现有大量气泡产生。小松想水泥块是否可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥。
(2)【猜想】:水泥块可以作过氧化氢分解的催化剂。
(3)【实验验证】:
(4)【结论】:水泥块能加快过氧化氢分解的速率,故水泥块可以作过氧化氢分解的催化剂。
(5)【讨论与反思】:小芳认为:仅凭上述两个实验还不能证明水泥块可以作过氧化氢分解反应的催化剂,她觉得需要增加一个探究实验:探究______ 。
【实验步骤】:①准确称量水泥块的质量;②完成实验二;③待反应结束,将实验二中试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后水泥块的质量。
【分析】:如果______ ,则说明水泥块可以作过氧化氢分解的催化剂。
(6)但小华认为,要证明小松的猜想,小芳的补充实验还是不够,还需要再补充一个实验:探究______ 。
(1)【提出问题】:小松同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现有大量气泡产生。小松想水泥块是否可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥。
(2)【猜想】:水泥块可以作过氧化氢分解的催化剂。
(3)【实验验证】:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 取5mL、5%的过氧化氢溶液于试管中,伸入带火星的木条 | 木条不复燃 | 过氧化氢分解产生氧气,但是反应速度 |
| 实验二 | 向盛水的试管中加入水泥块,伸入带火星的木条 | 没有明显现象 | |
| 实验三 | 水泥块能加快过氧化氢分解的速率 |
(5)【讨论与反思】:小芳认为:仅凭上述两个实验还不能证明水泥块可以作过氧化氢分解反应的催化剂,她觉得需要增加一个探究实验:探究
【实验步骤】:①准确称量水泥块的质量;②完成实验二;③待反应结束,将实验二中试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后水泥块的质量。
【分析】:如果
(6)但小华认为,要证明小松的猜想,小芳的补充实验还是不够,还需要再补充一个实验:探究
您最近一年使用:0次
【推荐3】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
【猜想】
Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后_____ 。
【实验】天平称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①③对比可以说明_____ 。
(3)步骤⑦的目的是_____ 。
(4)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为_____ 。
【猜想】
Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后
【实验】天平称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出,带火星的木条复燃 | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(3)步骤⑦的目的是
(4)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为
您最近一年使用:0次



