A~E为初中化学常见的物质。A为一种氧化物,B为目前世界上年产量最高的金属单质,C中含有两种元素,D在农业上常用来改良酸性土壤,E为石灰石的主要成分,其相互反应及转化关系如图所示,图中“——”表示两物质间能发生化学反应,“―→”表示两物质间存在转化关系。请回答:

(1)D物质的化学式为___________ 。
(2)A转变为B反应的化学方程式为___________ ,该反应在工业中的一种用途是___________ 。
(3)C与E反应的化学方程式为___________ ,该反应的基本反应类型为___________ 。
(4)B与C能发生反应的原因为___________ 。

(1)D物质的化学式为
(2)A转变为B反应的化学方程式为
(3)C与E反应的化学方程式为
(4)B与C能发生反应的原因为
2021·甘肃·模拟预测 查看更多[1]
更新时间:2021-12-10 22:53:46
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】“5G”改变生活,中国“芯”彰显中国“智”造。芯片的基材主要是高纯硅,硅(Si)常温下与稀盐酸不反应,加热条件下易与C12、O2等较活泼的非金属单质反应。如图是一种制备高纯硅的工艺流程图:

(1)操作Ⅰ的实验名称为______ 。
(2)该流程中可以循环利用的物质是______ 。(填化学式)
(3)反应Ⅱ必须在无氧环境下进行,理由是______ 。
(4)上述流程的反应中,没有涉及的基本反应类型是______ 反应(填“化合”、“分解”、“置换”或“复分解”)。

(1)操作Ⅰ的实验名称为
(2)该流程中可以循环利用的物质是
(3)反应Ⅱ必须在无氧环境下进行,理由是
(4)上述流程的反应中,没有涉及的基本反应类型是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】小组同学用化学试剂制作奥运五环。已知甲基橙是一种酸碱指示剂,其变色范围是pH≤3.1时呈红色,pH在3.1~4.4之间呈橙色,pH≥4.4时呈黄色。

(1)A环:NaOH溶液中加入______ 溶液。
(2)B环: 溶液中加入Na2S溶液,生成难溶于水的黑色物质CuS,写出该复分解反应的化学方程式:
溶液中加入Na2S溶液,生成难溶于水的黑色物质CuS,写出该复分解反应的化学方程式:______ 。
(3)依据下图,向D环中加入______ (选一种即可)后滴加甲基橙溶液,呈现黄色。


(1)A环:NaOH溶液中加入
(2)B环:
 溶液中加入Na2S溶液,生成难溶于水的黑色物质CuS,写出该复分解反应的化学方程式:
溶液中加入Na2S溶液,生成难溶于水的黑色物质CuS,写出该复分解反应的化学方程式:(3)依据下图,向D环中加入

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】习近平总书记指出:科技创新是核心。科技兴则民族兴,科技强则国家强。
(1)下图是明代宋应星所著《天工开物》中的我国古代炼铁、炼锌图。

①铁、锌及其合金均属于_____ (填字母)。
A 金属材料
B 复合材料
C 有机高分子材料
②结合所学知识推测,用于炼铁的装置必须具备的物理性质是_____ (填字母)。
A 密度小
B 熔点高
C 抗腐蚀性好
③炼锌的过程中有一个反应是木炭在高温条件下还原氧化锌(ZnO) ,生成单质锌和一种可用于灭火的气体。该反应的化学方程式为_____ ;此反应前后锌元素的化合价分别为_____ ;
(2)古往今来,正是一代代中华儿女的迸发出的创造伟力凝聚成了世界科技史长河中的璀璨明珠!下图科学家发明了“联合制碱法”,他的名字是_____ 他为纯碱和_____ 工业技术的发展做出了杰出的贡献。

(1)下图是明代宋应星所著《天工开物》中的我国古代炼铁、炼锌图。

①铁、锌及其合金均属于
A 金属材料
B 复合材料
C 有机高分子材料
②结合所学知识推测,用于炼铁的装置必须具备的物理性质是
A 密度小
B 熔点高
C 抗腐蚀性好
③炼锌的过程中有一个反应是木炭在高温条件下还原氧化锌(ZnO) ,生成单质锌和一种可用于灭火的气体。该反应的化学方程式为
(2)古往今来,正是一代代中华儿女的迸发出的创造伟力凝聚成了世界科技史长河中的璀璨明珠!下图科学家发明了“联合制碱法”,他的名字是

您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐2】多角度认识物质的变化,有助于我们更好地理解化学知识。
(1) 从微观角度(图1为某化学反应的微观示意图,据图回答下列问题)

① 微观上看,该化学变化中发生根本改变的微粒是____________ (填“原子”或“分子”)。
② 参加反应的A2与B2两种物质的分子个数比为_______ 。
(2) 从反应类型角度(一种物质可通过不同的反应类型生成,以二氧化碳为例。)
① 能与氧气化合生成二氧化碳的物质是_________ (填一种物质化学式)。
② 高温下,碳酸钙分解生成二氧化碳的化学方程式是_______________ 。
③ 在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和________ (填化学式,下同),该反应也属于氧化还原反应,其中__________ 是还原剂。
(3) 从能量变化角度(利用图2装置分别进行下列实验,认识物质变化中的能量变化)
① 往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_________ 。
② 将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷 燃烧的是_____________ (填标号)。
A. 氯化钠 B. 硝酸铵 C. 浓硫酸 D. 氢氧化钠
(1) 从微观角度(图1为某化学反应的微观示意图,据图回答下列问题)

① 微观上看,该化学变化中发生根本改变的微粒是
② 参加反应的A2与B2两种物质的分子个数比为
(2) 从反应类型角度(一种物质可通过不同的反应类型生成,以二氧化碳为例。)
① 能与氧气化合生成二氧化碳的物质是
② 高温下,碳酸钙分解生成二氧化碳的化学方程式是
③ 在一定条件下,碳与铁的氧化物能发生置换反应,生成二氧化碳和
(3) 从能量变化角度(利用图2装置分别进行下列实验,认识物质变化中的能量变化)
① 往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是
② 将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷 燃烧的是
A. 氯化钠 B. 硝酸铵 C. 浓硫酸 D. 氢氧化钠
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属及金属属材料广泛应用于生产、生活及科学实验中,金属材料的应用推动了社会的发展。
(1)在农业生产中(如图所示),大量使用合金,而不是纯金属,是因为合金硬度______ 纯金属(填“大于”或“小于”)。
(2)铁窗经过风雨后,会有铁锈附着在铁窗上,铁锈的产生实际上是铁窗与空气中的水蒸气和______ 等发生反应的过程,生活中可以通过刷油漆来防止铁窗生锈。
(3)铝在空气中能形成一层致密的氧化铝薄膜,因此具有很好的抗腐蚀性,该反应的化学方程式为:______ 。
(4)为了回收金属,在硝酸根和硝酸铜的混合溶液中加入一定量的铝粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。则滤渣中一定含有______ ;滤液中的溶质含有______ 。
(5)取碳和氧化铁的混合物ag在一定条件下恰好完全反应生成铁和二氧化碳,相关量的变化如下图,下列说法不正确的是______(填标号)。

(1)在农业生产中(如图所示),大量使用合金,而不是纯金属,是因为合金硬度
(2)铁窗经过风雨后,会有铁锈附着在铁窗上,铁锈的产生实际上是铁窗与空气中的水蒸气和
(3)铝在空气中能形成一层致密的氧化铝薄膜,因此具有很好的抗腐蚀性,该反应的化学方程式为:
(4)为了回收金属,在硝酸根和硝酸铜的混合溶液中加入一定量的铝粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。则滤渣中一定含有
(5)取碳和氧化铁的混合物ag在一定条件下恰好完全反应生成铁和二氧化碳,相关量的变化如下图,下列说法不正确的是______(填标号)。

| A.反应后产生气体的总质量为bg |
| B.B点对应的固体是黑色 |
| C.A点对应的固体物质有三种 |
| D.0~T2min内,固体的总质量逐渐减少 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】2018年阜新至沈阳,阜新至北京即将建成高速铁路,阜新将进入“高铁时代”。生铁和钢在钢轨铺设及高铁列车的制造中应用广泛,请根据所学化学知识回答下列相关问题:
(1)钢轨及高铁列车的许多部件其主要化学成分是铁,如遇到酸性物质会腐蚀。请写出铁与稀盐酸反应的化学方程式_______ ,其化学反应基本类型为_______ 。
(2)钢铁生锈是世界面临的难题,铁生锈实际上是铁与水、_______ 共同作用的结果。家庭中自行车链条也是钢铁制品,你经常采用的防锈方法是_______ 。
(3)在盛装铁锈(主要成分是Fe2O3)的试管内加入足量稀硫酸,可以观察到的实验现象是_______ ,该反应可以说明酸的一种化学性质——酸和某些金属氧化物反应生成_______ 。
(1)钢轨及高铁列车的许多部件其主要化学成分是铁,如遇到酸性物质会腐蚀。请写出铁与稀盐酸反应的化学方程式
(2)钢铁生锈是世界面临的难题,铁生锈实际上是铁与水、
(3)在盛装铁锈(主要成分是Fe2O3)的试管内加入足量稀硫酸,可以观察到的实验现象是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】工业上生产电路板及处理废液的工艺流程如下:

(1)操作a是________________ 。
(2)步骤②加入过量铁粉,除能与废液中的FeCl3反应外,还可发生反应的化学方程式为______ 。
(3)步骤③加入稀盐酸,充分搅拌,当观察到_________________________ 现象时,说明滤渣只剩铜。步骤③发生的化学方程式为 __________________________________ 。
(4)步骤②③所得FeCl2可与一种单质发生化合反应,生成可循环使用的FeCl3。请写出该反应的化学方程式________________ 。

(1)操作a是
(2)步骤②加入过量铁粉,除能与废液中的FeCl3反应外,还可发生反应的化学方程式为
(3)步骤③加入稀盐酸,充分搅拌,当观察到
(4)步骤②③所得FeCl2可与一种单质发生化合反应,生成可循环使用的FeCl3。请写出该反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】如图所示,A~G是初中化学常见的物质,图中“→”表示转化关系,“—”表示相互能反应(部分反应物、生成物及反应条件未列出)。已知A是人体胃液中含有的酸,G是最轻的气体,其余都是氧化物。请回答下列问题:
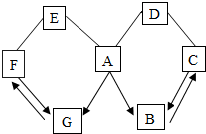
(1)F的化学式为_____ ;
(2)C与D发生反应的化学方程式为_____ (只写一个)。

(1)F的化学式为
(2)C与D发生反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】有一瓶无标签的无色液体,为了探究它是何种物质,做如下实验:把此液体编号为A,加热A液体,发现有气体B产生,在A中加入黑色粉末C,稍微振荡,在常温下就能迅速产生气体B,且产生了常温下为液体的纯净物D,而C的质量在反应前后没有改变。把B收集起来,用带火星的木条伸入盛B的集气瓶中,木条剧烈燃烧。如把黄色粉末E点燃后放入盛B的集气瓶中,能剧烈燃烧,生成一种无色有刺激性气味的气体F。
(1)根据实验,分析A、B、C、D、E、F分别是什么物质。写出各物质的化学式:A.______ ;B.______ ;C.______ ;D.______ ;E.______ ;F.______ 。
(2)E+B→F,写出该步骤的符号表达式________ 。
(1)根据实验,分析A、B、C、D、E、F分别是什么物质。写出各物质的化学式:A.
(2)E+B→F,写出该步骤的符号表达式
您最近一年使用:0次


 、
、 等有害气体。请回答下列问题:
等有害气体。请回答下列问题:
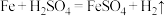

 选填“复分解”或“置换”
选填“复分解”或“置换” 反应,反应前后铁元素的化合价不变的反应是
反应,反应前后铁元素的化合价不变的反应是
 ,②
,②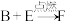 。
。

