实验小组同学在学习过氧化氢制氧气的实验后,决定研究“影响过氧化氢分解生成氧气快慢的因素”的课题。
【猜想假设】反应物的浓度和催化剂的用量会影响过氧化氢分解生成氧气的快慢。
【进行实验】实验装置图如下:
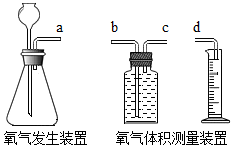
实验:探究过氧化氢溶液浓度对过氧化氢分解生成氧气快慢的影响。
实验数据记录如下(实验均在室温下进行):
实验2:探究催化剂用量对过氧化氢分解生成氧气快慢的影响。
实验数据记录如下(实验均在室温下进行):
【解释与结论】
(1)过氧化氢溶液属于___ (填“纯净物”或“混合物”)。
(2)过氧化氢在二氧化锰催化作用下反应的文字表达式为___ 。
(3)实验装置中各导管口的连接顺序为a→___ →d。
(4)由实验1可得到的结论是___ 。
(5)通过实验2得到“其他条件相同时,二氧化锰的质量越大,过氧化氢分解生成氧气 如越快”的结论,则x1 、x2 、x3数值大小关系为___ 。
【实验拓展】
(6)你还想研究的问题是___ 。
【猜想假设】反应物的浓度和催化剂的用量会影响过氧化氢分解生成氧气的快慢。
【进行实验】实验装置图如下:

实验:探究过氧化氢溶液浓度对过氧化氢分解生成氧气快慢的影响。
实验数据记录如下(实验均在室温下进行):
| 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | 二氧化锰的质量 | 相同时间内产生氧气的体积/mL | |
| 1-1 | 50.0g | 1% | 0.1g | 9 |
| 1-2 | 50.0g | 2% | 0.1g | 16 |
| 1-3 | 50.0g | 4% | 0.1g | 31 |
实验数据记录如下(实验均在室温下进行):
| 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | 二氧化锰的质量 | 相同时间内产生氧气的体积/mL | |
| 2-1 | 50.0 g | 4% | 0 | x1 |
| 2-2 | 50.0 g | 4% | 0.1g | x2 |
| 2-3 | 50.0 g | 4% | 0.2g | x3 |
(1)过氧化氢溶液属于
(2)过氧化氢在二氧化锰催化作用下反应的文字表达式为
(3)实验装置中各导管口的连接顺序为a→
(4)由实验1可得到的结论是
(5)通过实验2得到“其他条件相同时,二氧化锰的质量越大,过氧化氢分解生成氧气 如越快”的结论,则x1 、x2 、x3数值大小关系为
【实验拓展】
(6)你还想研究的问题是
更新时间:2022-01-22 16:09:32
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】氧气是一种化学性质比较活泼的气体,它可以与许多物质发生化学反应。兴趣小组对氧气的性质和影响制取氧气速率的因素进行了探究活动。
【活动一】探究氧气化学性质的实验
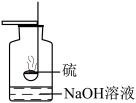
(1)兴趣小组的同学收集一瓶O2并进行性质检验。
【活动二】探究影响实验室制取氧气反应速率的因素
【实验I】为探究催化剂种类对过氧化氢分解速率的影响,兴趣小组的同学将不同催化剂分别加入30mL等浓度的过氧化氢溶液中,记录收集50mLO2所用的时间,数据如表。
(2)表格中a的值为______ 。
(3)实验②中制取氧气的化学方程式为_______ 。
(4)结论:通过上述实验对比,可得出的实验结论是_______ 。
【实验II】化学兴趣小组借助数字化实验手段,用装置A探究其他条件对过氧化氢分解速率的影响,选用0.2gMnO2粉末作催化剂分组进行实验,通过压强传感器测得的数据如图所示。_______ (选填“越快”或“越慢”)。
(6)分析图中实验②所示数据,可得出的结论是______ 。
【实验拓展】
(7)除上述影响过氧化氢分解速率的因素外,你认为过氧化氢分解的速率还可能与______ 有关。
【活动一】探究氧气化学性质的实验
(1)兴趣小组的同学收集一瓶O2并进行性质检验。
| 实验操作 | 实验现象 | 实验结论 |
| 硫燃烧时,观察到的现象是 | O2具有助燃性 |
| 集气瓶中NaOH溶液的作用是 | ||
【活动二】探究影响实验室制取氧气反应速率的因素
【实验I】为探究催化剂种类对过氧化氢分解速率的影响,兴趣小组的同学将不同催化剂分别加入30mL等浓度的过氧化氢溶液中,记录收集50mLO2所用的时间,数据如表。
| 实验序号 | 催化剂 | 收集50mLO2所用的时间/s |
| ① | 无 | >200 |
| ② | 0.2gMnO2粉末 | 15 |
| ③ | agCuO粉末 | 34 |
| ④ | 0.2gFeCl3粉末 | 27 |
(2)表格中a的值为
(3)实验②中制取氧气的化学方程式为
(4)结论:通过上述实验对比,可得出的实验结论是
【实验II】化学兴趣小组借助数字化实验手段,用装置A探究其他条件对过氧化氢分解速率的影响,选用0.2gMnO2粉末作催化剂分组进行实验,通过压强传感器测得的数据如图所示。
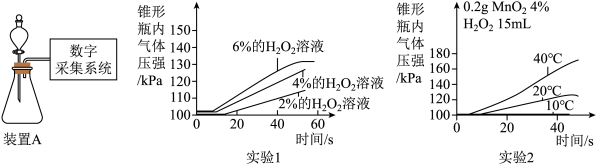
(6)分析图中实验②所示数据,可得出的结论是
【实验拓展】
(7)除上述影响过氧化氢分解速率的因素外,你认为过氧化氢分解的速率还可能与
您最近一年使用:0次
【推荐2】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后______
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
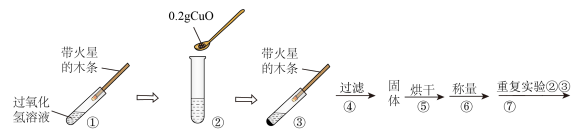
(1)填写下表:
(2)步骤①的目的是______ 。
(3)过氧化氢能被CuO催化分解放出O2的符号表达式为______ 。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 带火星的木条 | 步骤⑥结果为 固体质量 | 步骤⑦现象 溶液中有气泡产生 说明 | 结论 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立 |
(3)过氧化氢能被CuO催化分解放出O2的符号表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小林探究H2O2分解生成氧气速率的影响因素,借助如图1所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
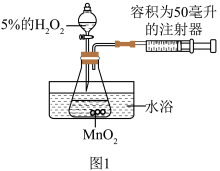
(1)写出此实验反应的文字表达式__________ 。
(2)此实验探究_________ 对过氧化氢制取氧气速率的影响。
(3)在两次实验中,可通过定量测定_________ 来比较H2O2分解反应速率的大小。
(4)实验2中反应过程中温度升高,但反应速率却越来越慢,你觉得原因应该是_______ 。
(5)水浴温度控制在80℃时,测定的反应速率比真实值偏大,其可能的原因是_______ (填字母序号)。
(6)小金通过实验发现,不同的金属氧化物对过氧化氢分解速率的影响。他在等体积的三个锥形瓶中加入40mL5%的H2O2溶液,分别加入MnO2、Fe2O3、CuO根据实验数据绘制了氧气体积和时间变化的曲线图(图2)。观察该图回答问题:
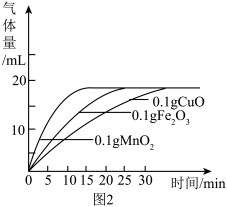
①通过该图可得出两条结论:________ 、________ 。
②兴趣小组做了另一组实验,向第四个锥形瓶中加入40mL约6~7%的H2O2溶液,并加入0.1gMnO2,请用虚线在图中补上实验所得曲线________ 。

| 实验1 | 实验2 | |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2的体积/毫升 | 40 | 40 |
| 水浴温度/℃ | 20 | 80 |
(1)写出此实验反应的文字表达式
(2)此实验探究
(3)在两次实验中,可通过定量测定
(4)实验2中反应过程中温度升高,但反应速率却越来越慢,你觉得原因应该是
(5)水浴温度控制在80℃时,测定的反应速率比真实值偏大,其可能的原因是
| A.发生装置内气体受热膨胀 |
| B.温度较高,水蒸发较快。导致氧气中含有较多水蒸气 |
| C.生成更多氧气 |
(6)小金通过实验发现,不同的金属氧化物对过氧化氢分解速率的影响。他在等体积的三个锥形瓶中加入40mL5%的H2O2溶液,分别加入MnO2、Fe2O3、CuO根据实验数据绘制了氧气体积和时间变化的曲线图(图2)。观察该图回答问题:

①通过该图可得出两条结论:
②兴趣小组做了另一组实验,向第四个锥形瓶中加入40mL约6~7%的H2O2溶液,并加入0.1gMnO2,请用虚线在图中补上实验所得曲线
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组在做完碳还原氧化铜实验后,进行了如下图所示的探究:
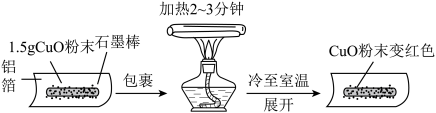
【猜想】把氧化铜还原成铜的物质是:Ⅰ. 石墨棒;Ⅱ. 铝箔。
【实验】用天平称量1.5g氧化铜粉末,直接用铝箔纸包裹。按上述操作步骤实验,黑色粉末__________ ,那么猜想Ⅱ不成立。
【结论】石墨棒能使氧化铜还原成铜,该反应的化学方程式为__________ 。
【改进】把石墨棒换成铝粉,重复上述操作,又获成功。那么,称取等量的铝粉并进行同样的操作,其目的是__________ 。该反应的化学方程式为__________ 。
【拓展】如果使用复印机的“碳粉”代替石墨棒还原氧化铜,效果更好。联想在空气中灼热的铁丝不能燃烧,而铁粉能燃烧,其原因是__________ 。

【猜想】把氧化铜还原成铜的物质是:Ⅰ. 石墨棒;Ⅱ. 铝箔。
【实验】用天平称量1.5g氧化铜粉末,直接用铝箔纸包裹。按上述操作步骤实验,黑色粉末
【结论】石墨棒能使氧化铜还原成铜,该反应的化学方程式为
【改进】把石墨棒换成铝粉,重复上述操作,又获成功。那么,称取等量的铝粉并进行同样的操作,其目的是
【拓展】如果使用复印机的“碳粉”代替石墨棒还原氧化铜,效果更好。联想在空气中灼热的铁丝不能燃烧,而铁粉能燃烧,其原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】金属锌在生产生活中有广泛应用。
Ⅰ、生活中人们常使用的“五号电池”属于锌锰电池,电池内部结构如图1所示。

[查阅资料]
①锌皮为金属锌(含有少量的铁)。
②黑色糊状填充物由炭黑、MnO2、ZnCl2、NH4Cl等组成
③NH4Cl和ZnCl2的溶解度数据见下表:
按照图2所示实验回收黑色糊状填充物中的部分物质。
(1)溶液A中溶质主要有______ (填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者的分离,得到的固体N是______ (填化学式)。
(2)欲从固体M中得到较纯的MnO2,操作Ⅲ可采用的方法是______ 。
Ⅱ、小明用纯锌粒和稀盐酸反应制取氢气时,发现加入CuSO4溶液后,反应速率明显变大,于是他对此反应速率变大的原因进行了实验探究。
【猜想】
①加入的CuSO4溶液中的 使反应速率变大
使反应速率变大
②加入的CuSO4溶液中的 使反应速率变大
使反应速率变大
③加入的CuSO4溶液中的Cu2+使反应速率变大
④加入CuSO4溶液后,______ 使反应速率变大。
小明经过思考,认为最不可能的原因是猜想②。
【实验验证】
用a、b、c、d四支试管取等质量且过量的纯锌粒,分别向试管中加入等体积等溶质质量分数的稀盐酸后,继续以下实验
【结论】在锌与稀盐酸反应时,加入铜粉或______ 可加快反应速率。
Ⅲ、尝试定量探究实验
(1)有一瓶未开封的浓盐酸,部分标签如图所示。从中取出100 mL,加400 mL水配制成体积比为1:4的稀盐酸(水的密度为1.00 g/mL)。计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)

(2)分别用5只烧杯各取该稀盐酸50.00 g,加入锌粒。反应4小时后,发现烧杯中锌粒仍在冒气泡。相关数据如下表:
根据以上数据计算参加反应的锌粒质量______ (写出计算过程,结果精确到0.01g)。
分析计算结果,发现有明显偏差,其可能原因是______ 。
Ⅰ、生活中人们常使用的“五号电池”属于锌锰电池,电池内部结构如图1所示。

[查阅资料]
①锌皮为金属锌(含有少量的铁)。
②黑色糊状填充物由炭黑、MnO2、ZnCl2、NH4Cl等组成
③NH4Cl和ZnCl2的溶解度数据见下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | l00 | |
| 溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
(1)溶液A中溶质主要有
(2)欲从固体M中得到较纯的MnO2,操作Ⅲ可采用的方法是
Ⅱ、小明用纯锌粒和稀盐酸反应制取氢气时,发现加入CuSO4溶液后,反应速率明显变大,于是他对此反应速率变大的原因进行了实验探究。
【猜想】
①加入的CuSO4溶液中的
 使反应速率变大
使反应速率变大②加入的CuSO4溶液中的
 使反应速率变大
使反应速率变大③加入的CuSO4溶液中的Cu2+使反应速率变大
④加入CuSO4溶液后,
小明经过思考,认为最不可能的原因是猜想②。
【实验验证】
用a、b、c、d四支试管取等质量且过量的纯锌粒,分别向试管中加入等体积等溶质质量分数的稀盐酸后,继续以下实验
| 实验 | 现象 | 结论 |
| (1)向a试管中加入少量NaCl晶体 | 产生气泡速率不变 | |
| (2)向b试管中加入少量 | 产生气泡速率不变 | 猜想①不成立 |
| (3)向c试管中加入少量Cu粉 | 产生气泡速率明显变大 | 猜想 |
| (4)向d试管中加入少量Cu粉,立即再加入CuSO4粉末 | 产生气泡速率与c试管的速率几乎一样大 | 猜想 |
Ⅲ、尝试定量探究实验
(1)有一瓶未开封的浓盐酸,部分标签如图所示。从中取出100 mL,加400 mL水配制成体积比为1:4的稀盐酸(水的密度为1.00 g/mL)。计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)

(2)分别用5只烧杯各取该稀盐酸50.00 g,加入锌粒。反应4小时后,发现烧杯中锌粒仍在冒气泡。相关数据如下表:
| 平行实验 | ① | ② | ③ | ④ | ⑤ | |
| 反应前质量/g | 锌粒 | 5.75 | 5.77 | 5.79 | 5.77 | 5.75 |
| 烧杯 | 75.17 | 76.36 | 70.16 | 74.73 | 70.14 | |
| 反应4h后质量/g | 烧杯及烧杯内所有物质 | 128.96 | 130.13 | 123.99 | 128.51 | 123.93 |
分析计算结果,发现有明显偏差,其可能原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】世界上每年都有将近总产量十分之一的钢铁锈蚀,造成了巨大的经济损失。为探究铁锈蚀的原因,某校学习小组以铁的腐蚀为项目进行拓展探究:
[知识回顾]铁制品锈蚀的条件及观察到出现锈蚀的现象是___________ ;
[实验活动]小明同学设计实验方案并按如图装置进行实验,当铁丝足量,时间足够长后,除观察到铁丝表面出现红棕色,还能观察到的实验现象是_____________ ,其原因是_____________ ;
[拓展探究]小强同学取铁钉用砂纸打磨,称其质量,按下图装置进行实验,放置3天,再取出铁钉称量。在不同温度下重复实验,得到铁钉质量增加情况如下表:
[提出质疑]有同学认为小强的实验未能真实反映50℃以后铁钉腐蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的原因是______________ ,请改进实验方案证明你的分析_____________ ;
[反思交流]请你写出一条生活中防止铁制品锈蚀的有效措施:___________ 。
[知识回顾]铁制品锈蚀的条件及观察到出现锈蚀的现象是
[实验活动]小明同学设计实验方案并按如图装置进行实验,当铁丝足量,时间足够长后,除观察到铁丝表面出现红棕色,还能观察到的实验现象是
[拓展探究]小强同学取铁钉用砂纸打磨,称其质量,按下图装置进行实验,放置3天,再取出铁钉称量。在不同温度下重复实验,得到铁钉质量增加情况如下表:
 | 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 铁钉质量增加/g | 0.02 | 0.04 | 0.08 | 0.16 | 0.18 | 0.18 | 0.18 | |
| 解释与结论:小强同学的实验是探究 | ||||||||
[反思交流]请你写出一条生活中防止铁制品锈蚀的有效措施:
您最近一年使用:0次