下图是氮气与氢气在高温、高压和催化剂的条件下反应生成的氨气(NH3),再与其他的原料合成硝酸铵(NH4NO3)的工业流程图。请按要求回答下列问题(提示:反应物与生成物在流程图中均已列出):
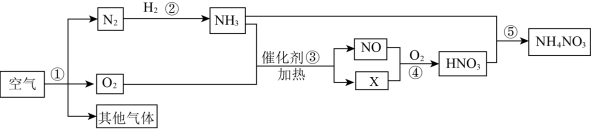
(1)步骤①发生的是________ 变化(填“物理”或“化学”)。
(2)请写出步骤②发生反应的化学方程式_______ 。
(3)步骤③发生反应的化学方程式为: ,则X的化学式为
,则X的化学式为_________ 。
(4)上述步骤中,发生的化学反应属于化合反应的是_______ (填步骤的序号)。
(5)80kg NH4NO3中含有氮元素的质量为________ kg。

(1)步骤①发生的是
(2)请写出步骤②发生反应的化学方程式
(3)步骤③发生反应的化学方程式为:
 ,则X的化学式为
,则X的化学式为(4)上述步骤中,发生的化学反应属于化合反应的是
(5)80kg NH4NO3中含有氮元素的质量为
更新时间:2022-01-24 17:22:44
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】空气是一种宝贵的自然资源
(1)通过实验测定了空气组成的科学家是_____ ;空气的成分按体积分数计算,稀有气体占__________ 。目前计入空气质量评价的主要污染物为:__________ 、二氧化硫、二氧化氮、臭氧、可吸入颗粒物和细颗粒物等。
(2)下列化学反应(部分反应的反应条件省略)中①氢气+氯气→氯化氢②甲烷+氧气→二氧化碳+ 水③氧化汞→汞+氧气④硫+氧气→二氧化硫,其中属于化合反应的是______ (填序号,下同); 属于氧化反应的是__________ ;属于分解反应的是_______ 。
(3)小明要量取 30mL 液体药品,应选量程为_____ (填“20mL”或“50mL”或“100mL”)的量筒, 除了用到量筒外,还需要__ (填仪器名称)。小明用量筒量取液体时,仰视读数为 36mL, 倒出部分液体后,俯视读数为 25mL,则他倒出液体的体积_________ (填“大于”、“小于”或“等于”)11mL。
(1)通过实验测定了空气组成的科学家是
(2)下列化学反应(部分反应的反应条件省略)中①氢气+氯气→氯化氢②甲烷+氧气→二氧化碳+ 水③氧化汞→汞+氧气④硫+氧气→二氧化硫,其中属于化合反应的是
(3)小明要量取 30mL 液体药品,应选量程为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F六种物质均为初中化学常见物质,且均含有同一种元素,其中只有A、D常温下为固体,B有毒性,B、C元素组成相同。如图是它们之间的相互转化关系。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系;部分反应物或生成物已略去。请回答:
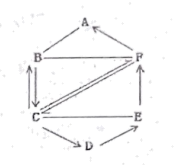
(1)写化学式:E______ 。
(2)C→F的转化在自然界广泛存在,这种转化叫做______ 。
(3)写出反应C→B的化学方程式______ ;该反应属于______ (填基本反应类型)。

(1)写化学式:E
(2)C→F的转化在自然界广泛存在,这种转化叫做
(3)写出反应C→B的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】氧气是生产生活中重要的物质。
(1)氧气有很多用途,下列属于氧气用途的是__________(填序号)。
(2)如图所示“氧气”要穿过迷宫,从进口顺利地走到出口,途中遇到不反应的物质才能通过(反应条件省略)。

①“箭头”画出了“氧气”应行走的路线,“氧气”不能从甲处通过,你认为甲处放的物质是______ (填字母)
A.硫 B. 水 C. 二氧化锰
②氧气在进迷宫过程中,碰到了三种能阻止它前进的物质,这三个反应的基本反应类型_______ (填“相同”或“不相同”)。
(1)氧气有很多用途,下列属于氧气用途的是__________(填序号)。
| A.医疗急救 | B.食品防腐 | C.航天火箭 | D.霓虹灯 |
(2)如图所示“氧气”要穿过迷宫,从进口顺利地走到出口,途中遇到不反应的物质才能通过(反应条件省略)。

①“箭头”画出了“氧气”应行走的路线,“氧气”不能从甲处通过,你认为甲处放的物质是
A.硫 B. 水 C. 二氧化锰
②氧气在进迷宫过程中,碰到了三种能阻止它前进的物质,这三个反应的基本反应类型
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】最近,三星锥考古又出土很多青铜器。青铜是铜锡或铜铅合金,它在空气久置后,表面会渐渐被氧化形成一层氧化铜(CuO)而发黑,也会被空气中水、二氧化碳和一种常见气体侵袭而变为铜绿(Cu2(OH)2CO3)。处理青铜发黑变绿的一种化学方法,一般用三酸(硝酸,盐酸,硫酸)抛光。如图1是铜在空气中发生化学变化和酸洗抛光等反应关系,回答下列问题:
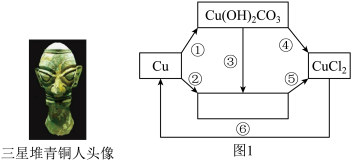
(1)写出 中物质的化学式
中物质的化学式_______ ;
(2)写出反应①的化学方程式_______ ;
(3)写出反应⑥的一个实验现象____ ;写出该化学反应的方程式____ 并指出反应类型___ 。

(1)写出
 中物质的化学式
中物质的化学式(2)写出反应①的化学方程式
(3)写出反应⑥的一个实验现象
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的化学方程式。
(1)铁丝燃烧________________ ;
(2)不能用铁桶配制波尔多液的原因________________ ;
(3)小苏打治疗胃酸过多________________ ;
(4)熟石灰和硝酸铵混合加热___________ 。
(1)铁丝燃烧
(2)不能用铁桶配制波尔多液的原因
(3)小苏打治疗胃酸过多
(4)熟石灰和硝酸铵混合加热
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】甲烷是最重要的基础有机物之一,不仅可做燃料,还能发生如下反应:
(1)①在隔绝空气和1000℃条件下,甲烷分解产生炭黑和氢气;
②在隔绝空气和1500℃条件下,甲烷分解产生乙炔(C2H2)和氢气;
③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳;
④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②、④两个反应的化学方程式:
②______ ;④______ 。
(2)在反应①~④中,属于置换反应的有______ 。在反应①和②中,反应物相同,而生成物不同,从微观的角度看,是因为反应条件不同导致______ 。③和④两个反应的反应物不同,但生成物相同,从物质组成的角度看,其原因是______ 。在实际生产中,反应③需要按比例控制氧气不能超量,从物质性质的角度看,原因是______ 。
(1)①在隔绝空气和1000℃条件下,甲烷分解产生炭黑和氢气;
②在隔绝空气和1500℃条件下,甲烷分解产生乙炔(C2H2)和氢气;
③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳;
④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②、④两个反应的化学方程式:
②
(2)在反应①~④中,属于置换反应的有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】工业制取硝酸的流程如下:

(1)步骤①反应属于分解反应,其微观实质是_____ ; 步骤②是利用液态氮与液态氧的_____ 不同。
(2)步骤③中催化剂所起的作用是_____ ,相应的化学方程式为_____ 。
(3)步骤④的化学方程式是 ,则X的化学式为
,则X的化学式为_____ 。
(4)流程中循环使用的物质是_____ (写化学式)。

(1)步骤①反应属于分解反应,其微观实质是
(2)步骤③中催化剂所起的作用是
(3)步骤④的化学方程式是
 ,则X的化学式为
,则X的化学式为(4)流程中循环使用的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】水产养殖中常用过氧化钙(CaO2)作供氧剂。CaO2•8H2O是一种白色固体,难溶于水和乙醇,且不与乙醇发生化学反应,加热至130℃时逐渐变为无水CaO2,实验室可用碳酸钙制取CaO2•8H2O,再经脱水制得CaO2,其制备流程如图所示。_______ ,该反应要在低温下进行的原因是_______ 。
(2)操作a的名称是_______ ,副产品的一种用途是_______ 。
(3)“水洗”的目的是_______ ,“乙醇洗”的目的是_______ ,烘烤过程中发生反应的化学方程式为_______ 。
(4)过氧化钙能作为水产养殖中的供氧剂,是因为过氧化钙在水中会缓慢放出氧气,该反应的化学方程式为_______ 。
(5)水产养殖中用的CaO2常含有杂质CaO,钙元素的质量分数会随CaO含量的增加而_______ (填“增大”、“减小”或“不变”)。
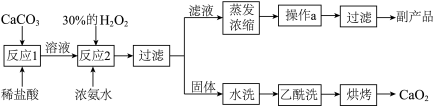
(2)操作a的名称是
(3)“水洗”的目的是
(4)过氧化钙能作为水产养殖中的供氧剂,是因为过氧化钙在水中会缓慢放出氧气,该反应的化学方程式为
(5)水产养殖中用的CaO2常含有杂质CaO,钙元素的质量分数会随CaO含量的增加而
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】根据下列材料回答下列问题。
材料一:反应前后,有元素化合价变化的化学反应是氧化还原反应。其中,有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂。
材料二:酸雨形成的原因主要有两种:
① ②2SO2+O2+2H2O
②2SO2+O2+2H2O 2H2SO4
2H2SO4
(1)材料二中反应①的 为
为_________________ (填化学式);
(2)材料二中反应②的基本反应类型为_________________________ ;
(3)结合材料一、二,下列说法正确的是 (填字母序号);
(4)为了减少城市酸雨的产生,下列措施正确的是 (填字母序号)。
材料一:反应前后,有元素化合价变化的化学反应是氧化还原反应。其中,有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂。
材料二:酸雨形成的原因主要有两种:
①
 ②2SO2+O2+2H2O
②2SO2+O2+2H2O 2H2SO4
2H2SO4(1)材料二中反应①的
 为
为(2)材料二中反应②的基本反应类型为
(3)结合材料一、二,下列说法正确的是 (填字母序号);
| A.反应①②都属于氧化还原反应 | B.反应①中  作还原剂 作还原剂 |
C.反应②中  作还原剂 作还原剂 | D.反应②中  发生氧化反应 发生氧化反应 |
| A.使用低硫煤、节约用煤 | B.大力发展公共交通 |
| C.安装尾气净化器及节能装置 | D.努力开发新能源 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】回答问题
(1)按照要求从铁、氧气、二氧化硫、碳酸钠、氢氧化镁中选择合适的物质,将其化学式填入空格中。
①能供给呼吸的气体_______ ;
②一种金属单质_______ ;
③一种非金属氧化物_______ ;
④一种难溶的碱_______ ;
⑤一种可溶的盐_______ 。
(2)济南市花是荷花和玫瑰,水生、陆生兼具,草本、木本共娇,一城“荷谐玫好”。
①人与自然和谐共生,保护自然环境,人人有责。现有下列四种生活垃圾,不能投放到可回收物垃圾桶内的是_______ (填下列选项序号之一)。

A.包装纸箱 B.废弃果皮 C.金属易拉罐 D.塑料饮料瓶
②中国科学院将“碳中和北方中心”落地济南,打造碳中和示范城市。只有逐步减少二氧化碳的排放,才能达到碳中和。下列不利于这一做法的是_______ (填下列选项序号之一)。

A.太阳能发电代替火力发电 B.少开私家车,绿色出行
C.夏天空调应不低于26℃ D.就地焚烧农作物的秸秆
③“赠人玫瑰,手留余香”。玫瑰花中含有的香茅醇(化学式为C10H20O)成分具有芬芳的气味,香茅醇属于_______ (选填“有机物” “无机物”之一);香茅醇中碳、氢元素的质量比是_______ (填最简整数比)。

④金代词人元好问在《临江仙—忆大明湖》中写到:“荷叶荷花何处好,大明湖上新秋。”荷叶中的荷叶碱(化学式C19H21NO2)有降血压、降血脂、降胆固醇的作用,荷叶碱中质量分数最大的元素是_______ (填元素符号)

(1)按照要求从铁、氧气、二氧化硫、碳酸钠、氢氧化镁中选择合适的物质,将其化学式填入空格中。
①能供给呼吸的气体
②一种金属单质
③一种非金属氧化物
④一种难溶的碱
⑤一种可溶的盐
(2)济南市花是荷花和玫瑰,水生、陆生兼具,草本、木本共娇,一城“荷谐玫好”。
①人与自然和谐共生,保护自然环境,人人有责。现有下列四种生活垃圾,不能投放到可回收物垃圾桶内的是

A.包装纸箱 B.废弃果皮 C.金属易拉罐 D.塑料饮料瓶
②中国科学院将“碳中和北方中心”落地济南,打造碳中和示范城市。只有逐步减少二氧化碳的排放,才能达到碳中和。下列不利于这一做法的是

A.太阳能发电代替火力发电 B.少开私家车,绿色出行
C.夏天空调应不低于26℃ D.就地焚烧农作物的秸秆
③“赠人玫瑰,手留余香”。玫瑰花中含有的香茅醇(化学式为C10H20O)成分具有芬芳的气味,香茅醇属于

④金代词人元好问在《临江仙—忆大明湖》中写到:“荷叶荷花何处好,大明湖上新秋。”荷叶中的荷叶碱(化学式C19H21NO2)有降血压、降血脂、降胆固醇的作用,荷叶碱中质量分数最大的元素是

您最近一年使用:0次
【推荐2】温室效应加剧引起的气候异常变化是人类面临的全球性问题之一、
(1)“碳中和”中的“碳”是指___________ (选填“CO”或“CO2”)。
(2)煤、___________ 、天然气被称作三大化石能源。天然气的主要成分为___________ (填名称或化学式)。
(3)第19届杭州亚运会“薪火”火炬塔首次使用废碳再生的“绿色甲醇(CH3O)”作为燃料,实现了循环内的零碳排放。甲醇燃烧反应的微观示意图如图所示:___________ (选填“发生”或“不发生”)改变。
②写出反应方程式:___________ 。
(4)氨气(NH3)作为一种零碳能源具有广泛应用前景。
①氨气易液化、方便储存和运输,含氢质量分数为___________ (精确到0.1%)。
②氨气在氧气中燃烧生成氮气和水,采用氨气作为零碳能源可行性的理由:___________ 。
(5)缓解温室效应的途径有自然界转化和人为转化。下列属于自然界转化的是___________(选填字母)。
(1)“碳中和”中的“碳”是指
(2)煤、
(3)第19届杭州亚运会“薪火”火炬塔首次使用废碳再生的“绿色甲醇(CH3O)”作为燃料,实现了循环内的零碳排放。甲醇燃烧反应的微观示意图如图所示:
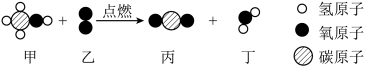
②写出反应方程式:
(4)氨气(NH3)作为一种零碳能源具有广泛应用前景。
①氨气易液化、方便储存和运输,含氢质量分数为
②氨气在氧气中燃烧生成氮气和水,采用氨气作为零碳能源可行性的理由:
(5)缓解温室效应的途径有自然界转化和人为转化。下列属于自然界转化的是___________(选填字母)。
| A.光合作用 | B.海洋吸收 | C.工业利用 |
您最近一年使用:0次
【推荐3】阅读下面的科普短文,回答相关问题。
氨是一种重要的化学物质。可用于制作硝酸和氮肥。氨主要来自于人工合成。1909年,佛里茨·哈伯成功地利用氮气和氢气合成出氨,工业合成氨的流程如图1所示。
为了找到合成氨反应合适的催化剂。人们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨。当容器中氨的含量不在发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图2所示。
1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨。其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。

(1)工业上可用_______ 方法获得合成氨的原料N2。
(2)从“合成塔”中出来的气体是_______ (填“纯净物”或“混合物”)。
(3)铁触媒催化剂在合成氨反应中的作用是_____ 。该反应的符号表达式为_____ 。该反应所属的基本反应类型是____ 。在铁触媒作用下,氮气和氢气合成氨气,请将该反应的微观过程按顺序排列:_____ 。(用序号表示)
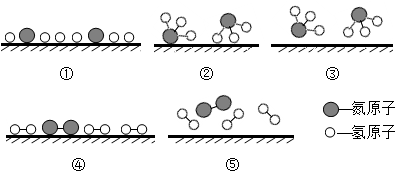
(4)按下列条件进行合成氨反应,平衡时氨的含量最高的是_______ 。(填字母编号)
A 200大气压、300℃ B 200大气压、500℃
C 400大气压、300℃ D 400大气压、500℃
(5)NH3可以进一步制得尿素和碳酸氢铵等化肥。下图是某商店内的两种化肥的标签。

①从标签上看,碳酸氢铵不同于尿素的化学性质是_______ 。
②上述100kg的碳酸氢铵化肥中至少含有纯净的NH4HCO3的质量为多少?_______ 。(最终结果保留一位小数)
氨是一种重要的化学物质。可用于制作硝酸和氮肥。氨主要来自于人工合成。1909年,佛里茨·哈伯成功地利用氮气和氢气合成出氨,工业合成氨的流程如图1所示。
为了找到合成氨反应合适的催化剂。人们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨。当容器中氨的含量不在发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图2所示。
1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨。其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。

(1)工业上可用
(2)从“合成塔”中出来的气体是
(3)铁触媒催化剂在合成氨反应中的作用是

(4)按下列条件进行合成氨反应,平衡时氨的含量最高的是
A 200大气压、300℃ B 200大气压、500℃
C 400大气压、300℃ D 400大气压、500℃
(5)NH3可以进一步制得尿素和碳酸氢铵等化肥。下图是某商店内的两种化肥的标签。

①从标签上看,碳酸氢铵不同于尿素的化学性质是
②上述100kg的碳酸氢铵化肥中至少含有纯净的NH4HCO3的质量为多少?
您最近一年使用:0次



