氯化铁溶液能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程。请回答下列问题:
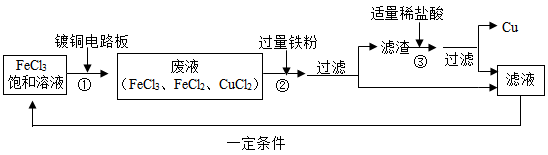
(1)根据图示,可以推测出步骤①中铜和FeCl3反应的化学方程式是___________ 。
(2)步骤②中发生了两个反应:2FeCl3+Fe═3FeCl2和___________ 。
(3)滤渣的成份有___________ 。
(4)步骤②③所得的滤液中的溶质可与一种气体单质发生化合反应转化为FeCl3,从而实现循环使用。该气体单质是___________ 。

(1)根据图示,可以推测出步骤①中铜和FeCl3反应的化学方程式是
(2)步骤②中发生了两个反应:2FeCl3+Fe═3FeCl2和
(3)滤渣的成份有
(4)步骤②③所得的滤液中的溶质可与一种气体单质发生化合反应转化为FeCl3,从而实现循环使用。该气体单质是
更新时间:2022-02-10 08:57:32
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】辉铜矿的主要成分为硫化亚铜(Cu2S),工业上用辉铜矿冶炼铜的一种工艺流程图如下。回答下列问题:
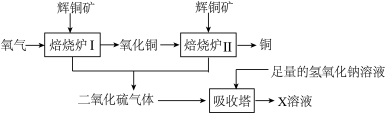
(1)硫化亚铜(Cu2S)中,铜元素和硫元素的质量比为______________ .在焙烧炉Ⅰ和Ⅱ中,将辉铜矿研碎的目的是_________________ 。
(2)焙烧炉Ⅱ中所发生反应的化学方程式为_______________ 。
(3)吸收塔中所发生反应为SO2+2NaOH=X+H2O,则X的组成元素为_____________ 。

(1)硫化亚铜(Cu2S)中,铜元素和硫元素的质量比为
(2)焙烧炉Ⅱ中所发生反应的化学方程式为
(3)吸收塔中所发生反应为SO2+2NaOH=X+H2O,则X的组成元素为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】用下图实验测定物质的组成。

(1)实验 1:能证明空气中 O2 含量的现象是______ 。化学反应方程式为______ 。
(2)实验 2:①的实验目的是______ 。
②向外拉注射器活塞,观察到______ ,证明蜡烛中一定含有碳元素。集气瓶中发生反应的化学方程式为______ 。

(1)实验 1:能证明空气中 O2 含量的现象是
(2)实验 2:①的实验目的是
②向外拉注射器活塞,观察到
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】证据推理是实验探究的重要环节。请回答下列探究石蜡性质的相关实验问题。
(1)取一小块石蜡放入水中,石蜡浮在水面上,可得到的结论是_______ 。(写2点)
(2)下列是探究蜡烛燃烧的三个实验。
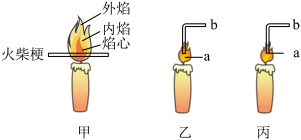
①实验甲进行大约1s钟左右,可观察到的现象是_______ ,据此可得到的结论是_______ 。
②实验乙中,玻璃管a端置于焰心处,则b端可观察的的现象是_______ ,用燃着的火柴靠近b端,b口立即产生火焰,由此可得到的结论是_______ (写1点)。
③实验丙中,玻璃管a端移置外焰处,b端接导管井通入澄清石灰水中,澄清石灰水变浑浊。由此可推知石蜡的组成元素中一定含有_______ 元素。
进一步的实验证明石蜡由碳、氢两种元素组成,若以CxHy表示石蜡的组成,则石蜡燃烧的化学方程式为_______ 。
(1)取一小块石蜡放入水中,石蜡浮在水面上,可得到的结论是
(2)下列是探究蜡烛燃烧的三个实验。

①实验甲进行大约1s钟左右,可观察到的现象是
②实验乙中,玻璃管a端置于焰心处,则b端可观察的的现象是
③实验丙中,玻璃管a端移置外焰处,b端接导管井通入澄清石灰水中,澄清石灰水变浑浊。由此可推知石蜡的组成元素中一定含有
进一步的实验证明石蜡由碳、氢两种元素组成,若以CxHy表示石蜡的组成,则石蜡燃烧的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】当朋友请你吃火锅时,你是否知道下列问题:
(1)在朋友已选择的点菜单中(√),朋友让你继续选菜,考虑到朋友龋齿,你应选择_______ ;
(2)香菜叶色浓绿枝干挺直,种植这种农作物施加的一种化肥是___________ ;
(3)喝啤酒若吃海鲜火锅,能导致人体中含氮的尿酸增加,引发痛风,这说明尿酸与海鲜中的__________ 营养素有关,因此,别造成“贪得一口福,吞下难忍苦”的后果。
(4)在火锅中加入盐,汤的沸点升高,反复加热,会造成汤中部分硝酸根离子转化为亚硝酸根离子(NO2—)使亚硝酸盐增多,如:硝酸钙在132℃时转化成可溶于水的亚硝酸钙,同时产生一种气体单质,该反应方程式为__________________________ ;氮元素的化合价变化是_____________ 。
火锅菜单 | 选择 | 价钱(盘) |
小肥羊肉卷 | √ | 15元 |
香菜 | √ | 5元 |
海带根 |
| 6元 |
豆腐 | √ | 5元 |
金针菇 |
| 10元 |
地瓜片 |
| 5元 |
鸭血块 |
| 5元 |
(2)香菜叶色浓绿枝干挺直,种植这种农作物施加的一种化肥是
(3)喝啤酒若吃海鲜火锅,能导致人体中含氮的尿酸增加,引发痛风,这说明尿酸与海鲜中的
(4)在火锅中加入盐,汤的沸点升高,反复加热,会造成汤中部分硝酸根离子转化为亚硝酸根离子(NO2—)使亚硝酸盐增多,如:硝酸钙在132℃时转化成可溶于水的亚硝酸钙,同时产生一种气体单质,该反应方程式为
您最近一年使用:0次
【推荐2】元素及其化合物是初中化学的基础知识。
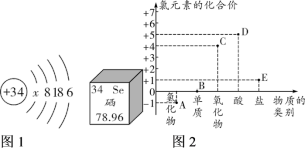
(1)图1是硒元素的原子结构示意图及该元素在周期表中的部分信息,硒元素的原子序数是________ ,x的数值是________ 。
(2)图2是以化合价为纵坐标、物质的类别为横坐标所绘制的“价类图”。图中A~E是含氯元素的物质,每种物质中氯元素的化合价与纵坐标的数值对应。
盐酸是将上述物质________ (填字母, 从A~E中选填)溶于水得到的溶液; D物质的化学式是________ ;E 是“84”消毒液的主要成分,也可由HClO与NaOH反应生成,该反应的化学方程式是____________________________ 。
(3)ClO2和Cl2都可以用作自来水的杀菌消毒剂,它们的消毒原理是在高价态的氯元素变成Cl-的过程中杀死细菌。氯元素化合价变化数与杀菌消毒能力成正比,计算相同质量的ClO2杀菌消毒能力是Cl2的________ 倍。(精确到小数点后2位)

(1)图1是硒元素的原子结构示意图及该元素在周期表中的部分信息,硒元素的原子序数是
(2)图2是以化合价为纵坐标、物质的类别为横坐标所绘制的“价类图”。图中A~E是含氯元素的物质,每种物质中氯元素的化合价与纵坐标的数值对应。
盐酸是将上述物质
(3)ClO2和Cl2都可以用作自来水的杀菌消毒剂,它们的消毒原理是在高价态的氯元素变成Cl-的过程中杀死细菌。氯元素化合价变化数与杀菌消毒能力成正比,计算相同质量的ClO2杀菌消毒能力是Cl2的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐3】“碳循环”是自然界中重要的一类物质转化,CO2在转化中起着非常重要的作用,如图是这种作用的具体体现之一
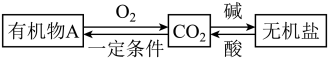
(1)如果A是葡萄糖(C6H12O6),它的分子中碳、氢、氧原子个数比为_________ ;
(2)自然界中“碳循环”的“碳”是指________ (选填“单质”“元素”“原子”) 。
(3)某有机物R在空气中完全燃烧的化学方程式:R+3O2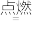 2CO2+3H2O,R的化学式为
2CO2+3H2O,R的化学式为_______ 。
(4)碳酸钾是无机盐,写出碳酸钾与盐酸反应的化学方程式_________________ 。
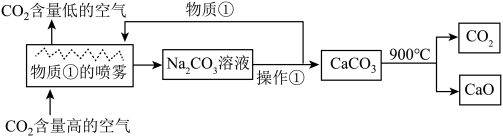
(5)科学家用NaOH溶液喷淋吸收CO2(如图)。对该方法的叙述正确的是____ 。

(1)如果A是葡萄糖(C6H12O6),它的分子中碳、氢、氧原子个数比为
(2)自然界中“碳循环”的“碳”是指
(3)某有机物R在空气中完全燃烧的化学方程式:R+3O2
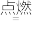 2CO2+3H2O,R的化学式为
2CO2+3H2O,R的化学式为(4)碳酸钾是无机盐,写出碳酸钾与盐酸反应的化学方程式
(5)科学家用NaOH溶液喷淋吸收CO2(如图)。对该方法的叙述正确的是

| A.该方法中包含分解反应,置换反应等 |
| B.物质是①是Na2CO3溶液 |
| C.操作①是蒸发浓缩,降温结晶 |
| D.整个过程至少有两种物质可以循环利用 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】应用所学知识,回答下列有关金属的问题:
(1)地壳中含量最多的金属元素是_______ (用元素符号回答).
(2)下列金属制品中,利用金属导电性的是_______ (填字母序号).

(3)将锌、铜、铁三种金属分别投入到足量的稀硫酸中,呈现不同现象的原因是______ 。
(4)将一定量的铁粉投入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,向滤渣中加入少量稀盐酸,无气体产生,则滤渣的成分可能是_________ 或_________ 。
(1)地壳中含量最多的金属元素是
(2)下列金属制品中,利用金属导电性的是

(3)将锌、铜、铁三种金属分别投入到足量的稀硫酸中,呈现不同现象的原因是
(4)将一定量的铁粉投入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,向滤渣中加入少量稀盐酸,无气体产生,则滤渣的成分可能是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】我国西汉时期就有用胆矾湿法炼铜的记载。现阶段,这种方法在生产有色金属方面的作用越来越大。为了验证铁和硫酸铜溶液的反应,认识其反应原因,同学们设计了如下实验方案,请根据下列提示,补全实验内容:
【实验方案】
实验方法:将洁净的铁丝伸入盛有硫酸铜溶液的试管中。
(1)实验原理:___________ (用化学方程式表示)。
(2)实验现象:___________ 。
(3)实验结论:___________ 。
【问题与交流】
(4)①该实验成功的关键是什么?(写1点)___________
②反应后溶液质量将如何变化?___________
【实验方案】
实验方法:将洁净的铁丝伸入盛有硫酸铜溶液的试管中。
(1)实验原理:
(2)实验现象:
(3)实验结论:
【问题与交流】
(4)①该实验成功的关键是什么?(写1点)
②反应后溶液质量将如何变化?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图为干电池的结构示意图。请利用所学知识完成下列问题。
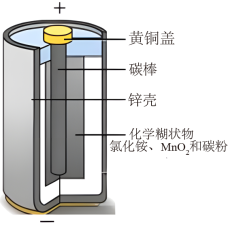
(1)碳棒(主要成分是石墨)用作干电池的正极是利用了石墨的___________ 性。
(2)干电池的材料很多可以回收利用。例如双氧水与回收的二氧化锰可用于实验室制取氧气,请写出反应的化学方程式______________ 。
(3)黄铜是铜与锌的合金。黄铜的硬度___________ (填“大于”或“小于”)纯铜。将锌放入硫酸铜溶液中,观察到___________ 现象,说明锌比铜活泼。

(1)碳棒(主要成分是石墨)用作干电池的正极是利用了石墨的
(2)干电池的材料很多可以回收利用。例如双氧水与回收的二氧化锰可用于实验室制取氧气,请写出反应的化学方程式
(3)黄铜是铜与锌的合金。黄铜的硬度
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】磷酸铁锂是目前最常用的一种锂离子电池正极材料,磷酸铁锂主流生产工艺是以磷酸铁为原料。近年来,新能源汽车行业高速发展,带动上游磷酸铁锂及磷酸铁(化学式为 )产能快速增加。采用硫酸亚铁及磷铵盐为原料制备的磷酸铁生产工艺称为“氨法磷酸铁”。“氨法磷酸铁”主要生产工艺流程如下图所示,请回答下列问题:
)产能快速增加。采用硫酸亚铁及磷铵盐为原料制备的磷酸铁生产工艺称为“氨法磷酸铁”。“氨法磷酸铁”主要生产工艺流程如下图所示,请回答下列问题:
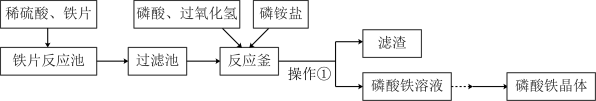
(1)操作①的名称是__________ 。
(2)铁片反应池中发生的反应方程式为: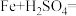
_______ 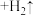 。
。
(3)该生产工艺中制备的 克磷酸铁中铁元素的质量是
克磷酸铁中铁元素的质量是_________ 克。
 )产能快速增加。采用硫酸亚铁及磷铵盐为原料制备的磷酸铁生产工艺称为“氨法磷酸铁”。“氨法磷酸铁”主要生产工艺流程如下图所示,请回答下列问题:
)产能快速增加。采用硫酸亚铁及磷铵盐为原料制备的磷酸铁生产工艺称为“氨法磷酸铁”。“氨法磷酸铁”主要生产工艺流程如下图所示,请回答下列问题:
(1)操作①的名称是
(2)铁片反应池中发生的反应方程式为:
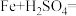
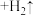 。
。(3)该生产工艺中制备的
 克磷酸铁中铁元素的质量是
克磷酸铁中铁元素的质量是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】化学实验室要从含少量铜粉的银、锰混合金属粉末中分离出贵金属,并获得一种盐的晶体,将有关金属随意编号A、B、C,并设计了如下流程:

(1)无色气体为________ 。
(2)用A、B、C表示三种金属的活动性由强到弱的顺序是________ 。
(3)步骤②的反应方程式是________ 。

(1)无色气体为
(2)用A、B、C表示三种金属的活动性由强到弱的顺序是
(3)步骤②的反应方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
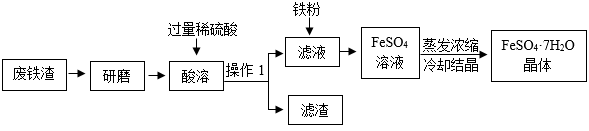
【推荐3】FeSO4·7H2O是一种重要的补铁剂。实验室以生锈的工业废铁渣(含Fe、C、Fe2O3)为原料制备硫酸亚铁晶体的流程如图所示:
资料卡片:铁与硫酸铁溶液反应的化学方程式为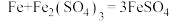 。
。
(1)铁和稀硫酸反应的化学方程式______ 。
(2)滤渣的成分______ ,操作1中玻璃棒的作用是______ 。
(3)废铁渣中的少量Fe2O3是如何除去的______ 。
(4)蒸发浓缩的目的是______ 。
(5)已知硫酸亚铁的溶解度和析出晶体的组成如下表:根据信息,FeSO4·7H2O晶体冷却结晶温度最高不超过______ 。
(6)补铁剂可以用于治疗的疾病是______ 。

资料卡片:铁与硫酸铁溶液反应的化学方程式为
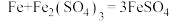 。
。(1)铁和稀硫酸反应的化学方程式
(2)滤渣的成分
(3)废铁渣中的少量Fe2O3是如何除去的
(4)蒸发浓缩的目的是
(5)已知硫酸亚铁的溶解度和析出晶体的组成如下表:根据信息,FeSO4·7H2O晶体冷却结晶温度最高不超过
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||
您最近一年使用:0次



