工业纯碱中含少量氯化钠。兴趣小组分别采用不同的方法测定工业纯碱样品中碳酸钠的质量分数。
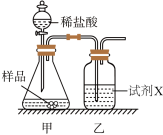
(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用____ 。
(2)方法二:沉淀法。称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。计算样品中碳酸钠的质量分数______ 。(Na2CO3+CaCl2=CaCO3↓+2NaCl)
(3)请写出提高方法一测量精确度的操作建议(写出2条)_____ 。
(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用

(2)方法二:沉淀法。称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。计算样品中碳酸钠的质量分数
| 烧杯1 | 烧杯2 | 烧杯3 | |
| 样品溶液(克) | 10 | 20 | 30 |
| 氯化钙溶液(克) | 30 | 30 | 30 |
| 沉淀质量(克) | 2 | 4 | 5 |
(3)请写出提高方法一测量精确度的操作建议(写出2条)
更新时间:2022-03-03 22:15:36
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】为测定氢氧化钠和硫酸钠混合物的组成情况,某研究小组进行了如下实验。
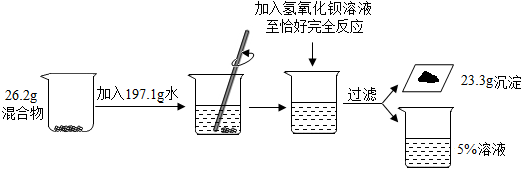
请回答下列问题:
(1)实验中发生反应的化学方程式为_________。
(2)求解混合物中发生反应物质的质量(x)的比例式为_________。
(3)混合物中氢氧化钠和硫酸钠质量的最简整数比为__________。
(4)在滴加氢氧化钡溶液的过程中,烧杯中各溶质质量的变化情况为_________。
(5)所用氢氧化钡溶液中溶质质量分数为__________。

请回答下列问题:
(1)实验中发生反应的化学方程式为_________。
(2)求解混合物中发生反应物质的质量(x)的比例式为_________。
(3)混合物中氢氧化钠和硫酸钠质量的最简整数比为__________。
(4)在滴加氢氧化钡溶液的过程中,烧杯中各溶质质量的变化情况为_________。
(5)所用氢氧化钡溶液中溶质质量分数为__________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】现有NaOH、NaCl和Na2CO3固体混合物109.1g。在烧杯中加入水溶解,向烧杯中加入稀盐酸,加入稀盐酸的质量与产生气体的关系如图:
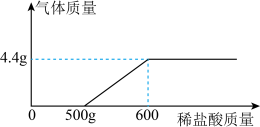
求:
(1)完全反应后,产生二氧化碳气体的体积是多少L?,保留一位小数。(已知二氧化碳气体密度为1.9g/L)
(2)加入稀盐酸的的质量分数?
(3)计算原混合物中NaCl的质量分数,保留一位小数。

求:
(1)完全反应后,产生二氧化碳气体的体积是多少L?,保留一位小数。(已知二氧化碳气体密度为1.9g/L)
(2)加入稀盐酸的的质量分数?
(3)计算原混合物中NaCl的质量分数,保留一位小数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】小丽同学在某化工厂参加社会实践,与技术员一起分析由Na2CO3和NaCl组成的样品中NaCl的质量分数。现取15g该固体样品,全部溶于200mL水中,向所得到的混合溶液中逐滴滴入溶质质量分数为7.3%的稀盐酸,记录了如下图所示的曲线关系。(水的密度为1g/mL,计算结果精确到0.1%)
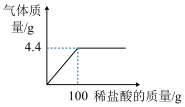
(1)当Na2CO3与稀盐酸恰好完全反应时,消耗7.3%的稀盐酸的质量是_____g;
(2)样品中NaCl的质量分数是多少?
(3)计算Na2CO3与稀盐酸恰好完全反应时,所得溶液的溶质质量分数。
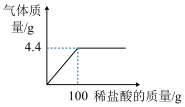
(1)当Na2CO3与稀盐酸恰好完全反应时,消耗7.3%的稀盐酸的质量是_____g;
(2)样品中NaCl的质量分数是多少?
(3)计算Na2CO3与稀盐酸恰好完全反应时,所得溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
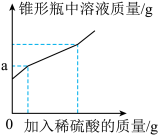
【推荐1】为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品6.5g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,现部分数据如图表:
(1)6.5g样品与稀硫酸完全反应产生气体的质量是____ g。
(2)求6.5g样品中碳酸钠的质量____ (写出具体计算过程)。
(3)分析图像:加入稀硫酸时中间有一段锥形瓶内溶液质量增加的幅度比两侧小,原因是___ 。
(4)以上三次实验数据只有一次表示反应恰好完全,则图象中a的数值是_____ 。
| 加入稀硫酸的质量/g | 40 | 65 | 75 |
| 产生气体的质量/g | 1.1 | 2.2 | 2.2 |
(2)求6.5g样品中碳酸钠的质量
(3)分析图像:加入稀硫酸时中间有一段锥形瓶内溶液质量增加的幅度比两侧小,原因是
(4)以上三次实验数据只有一次表示反应恰好完全,则图象中a的数值是

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某氯化钠样品中含有少量的氯化钙,样品中钠元素和钙元素的质量比为23:20。取一定量的该样品,向其中加入适量的碳酸钠溶液(密度为1.1g/cm3)恰好完全反应,过滤,得到10g沉淀和112.8g滤液。请计算:
(1)原样品中氯化钙的质量
(2)所加入碳酸钠溶液的溶质质量分数。
(3)所加入碳酸钠溶液的体积。(计算结果精确到0.1)
(1)原样品中氯化钙的质量
(2)所加入碳酸钠溶液的溶质质量分数。
(3)所加入碳酸钠溶液的体积。(计算结果精确到0.1)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】(1)某小苏打溶液中含16.8gNaHCO3,加入一定量的单质或化合物X,恰好使溶液中溶质只有Na2CO3,请你填写出X的化学式和质量.
例如:X为_____时,质量为_____;
①X为_____时,质量为_____;
②X为_____时,质量为_____;
③X为_____时,质量为_____.
(2)现有质量为18.4g的NaOH和NaHCO3的混合物.装入一密闭容器中,在120℃的温度下进行加热,经充分反应后,排出剩余气体,此时容器内固体物质的质量为16.6g.试计算原混合物中NaOH和NaHCO3的质量各为多少?(提示: )
)
例如:X为_____时,质量为_____;
①X为_____时,质量为_____;
②X为_____时,质量为_____;
③X为_____时,质量为_____.
(2)现有质量为18.4g的NaOH和NaHCO3的混合物.装入一密闭容器中,在120℃的温度下进行加热,经充分反应后,排出剩余气体,此时容器内固体物质的质量为16.6g.试计算原混合物中NaOH和NaHCO3的质量各为多少?(提示:
 )
)
您最近一年使用:0次



