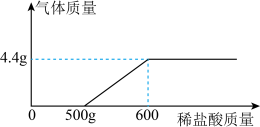
现有NaOH、NaCl和Na2CO3固体混合物109.1g。在烧杯中加入水溶解,向烧杯中加入稀盐酸,加入稀盐酸的质量与产生气体的关系如图:
求:
(1)完全反应后,产生二氧化碳气体的体积是多少L?,保留一位小数。(已知二氧化碳气体密度为1.9g/L)
(2)加入稀盐酸的的质量分数?
(3)计算原混合物中NaCl的质量分数,保留一位小数。

求:
(1)完全反应后,产生二氧化碳气体的体积是多少L?,保留一位小数。(已知二氧化碳气体密度为1.9g/L)
(2)加入稀盐酸的的质量分数?
(3)计算原混合物中NaCl的质量分数,保留一位小数。
更新时间:2018-02-01 20:57:02
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】为测定某敞口放置的氢氧化钠溶液的变质情况,某同学实验并记录如图:

(1)D烧杯溶液中溶质的化学式为_____;
(2)求100g样品溶液中碳酸钠的质量?(简要写出计算过程)

(1)D烧杯溶液中溶质的化学式为_____;
(2)求100g样品溶液中碳酸钠的质量?(简要写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】实验室里用过氧化氢溶液与二氧化锰制取氧气,相关数据如下:
请计算:
(1)制得氧气的物质的量为_________。
(2)该实验中反应的过氧化氢的物质的量(根据化学方程式计算)。
______________
(3)理论上该实验所用过氧化氢溶液的溶质质量分数为___________________。
| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
| 136.0 | 0.2 | 133.0 |
请计算:
(1)制得氧气的物质的量为_________。
(2)该实验中反应的过氧化氢的物质的量(根据化学方程式计算)。
______________
(3)理论上该实验所用过氧化氢溶液的溶质质量分数为___________________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】制碱工业在实际生产的产品碳酸钠中会混有少量的氯化钠,现有纯碱样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体全部逸出,得到不饱和氯化钠溶液。反应过程中测得烧杯内溶液的质量(m)与反应时间(t)关系如图所示。

试回答:
(1)生成CO2的质量为______ g。
(2)26.5g样品中碳酸钠的质量分数为多小?(写出计算过程,结果精确到0.1%下同。)
(3)请计算所得溶液中溶质的质量分数。

试回答:
(1)生成CO2的质量为
(2)26.5g样品中碳酸钠的质量分数为多小?(写出计算过程,结果精确到0.1%下同。)
(3)请计算所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应。有关实验数据如下表:( 假设石灰石样品中杂质不与稀盐酸反应也不溶于水 , 且不考虑反应过程中水分和 HCl 气体的挥发 )
(1)反应中生成二氧化碳的质量为_______g。
(2)该石灰石样品中碳酸钙的质量分数为_______(结果精确到0.1%)。
(3)反应后所得溶液中溶质质量分数是多少?(请写出计算过程)
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 157.6 g | |
(1)反应中生成二氧化碳的质量为_______g。
(2)该石灰石样品中碳酸钙的质量分数为_______(结果精确到0.1%)。
(3)反应后所得溶液中溶质质量分数是多少?(请写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】我国是世界湿法炼铜与火法炼铜的先驱。
(1)火法炼铜的原理是: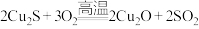
 ,某冶炼厂用含Cu2S10%的铜矿石160t冶炼铜,假设Cu2S全部转化为Cu2O,则生产的Cu2O质量是多少?(写出计算过程)
,某冶炼厂用含Cu2S10%的铜矿石160t冶炼铜,假设Cu2S全部转化为Cu2O,则生产的Cu2O质量是多少?(写出计算过程)
(2)火法炼铜产生的SO2会污染环境,可用NaOH溶液吸收。某实验小组将(1)中产生的64gSO2通入足量的NaOH溶液中,请在题图坐标中画出相应的曲线图______ (纵坐标为反应物或生成物的质量,请设定具体物质,并标出曲线中必要的数据)。

(3)火法炼铜第一步生成Cu2O后,可改为湿法炼铜,即: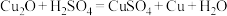
 。试通过原理比较湿法炼铜比火法炼铜的优点是
。试通过原理比较湿法炼铜比火法炼铜的优点是______ ;实验室佩好同学模仿湿法炼铜,将5.6g铁加入到一定量的硫酸铜溶液中,最终得到6g固体,6g固体中铜单质的质量为______ 。
(1)火法炼铜的原理是:
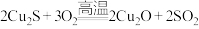
 ,某冶炼厂用含Cu2S10%的铜矿石160t冶炼铜,假设Cu2S全部转化为Cu2O,则生产的Cu2O质量是多少?(写出计算过程)
,某冶炼厂用含Cu2S10%的铜矿石160t冶炼铜,假设Cu2S全部转化为Cu2O,则生产的Cu2O质量是多少?(写出计算过程)(2)火法炼铜产生的SO2会污染环境,可用NaOH溶液吸收。某实验小组将(1)中产生的64gSO2通入足量的NaOH溶液中,请在题图坐标中画出相应的曲线图

(3)火法炼铜第一步生成Cu2O后,可改为湿法炼铜,即:
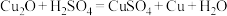
 。试通过原理比较湿法炼铜比火法炼铜的优点是
。试通过原理比较湿法炼铜比火法炼铜的优点是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】小江同学为了寻找含碳酸钙质量分数超过85%的石灰石,对一样品进行了如下定量实验(石灰石样品中的杂质不与盐酸反应).
试通过计算,分析该石灰石样品中碳酸钙的质量分数是否符合要求?_____
| 实验步骤 | 将适量盐酸加入烧杯中并称重 | 称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | 待反应完全后,称重 |
| 实验数据 | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】小丽同学家里有一只破损的手镯(银锌合金),她想探究此手镯中银的含量。首先称得手镯质量为12g。在用足量的稀硫酸分多次与此手镯充分反应,实验结果如表:
根据上表中的数据分析,完成下列问题:
(1)从第______ 次实验开始,稀硫酸有剩余:表格中m=_________ 。
(2)该手镯中银的质量分数是____________ 。
(3)所用稀硫酸的溶质质量分数是多少?(写出计算过程)
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
| 充分反应后剩余固体的质量/g | 11.35 | 10.7 | 10.05 | 9.6 | m |
根据上表中的数据分析,完成下列问题:
(1)从第
(2)该手镯中银的质量分数是
(3)所用稀硫酸的溶质质量分数是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】某学生在学习盐的性质时做了氯化铝溶液和氢氧化钠溶液反应的实验。该学生向氯化铝溶液中逐滴滴加氢氧化钠溶液时,发现溶液中有沉淀生成,且沉淀量先增多后减少直至消失。经查阅资料获知:Al(OH)3是一种两性氢氧化物,它既可以与酸反应又可以与碱反应都生成盐和水。它与碱反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O,NaAlO2可溶于水。现该学生将ag硬铝(Mg、Al、Cu、Si合金)溶于200.0g盐酸中,充分反应后过滤,然后向滤液X中逐滴滴加20.0%的NaOH溶液至过量,产生的沉淀与加入NaOH溶液的质量关系如图所示。已知Mg(OH)2不溶于NaOH溶液,请分析回答下列问题:

(1)滤液X的pH______7(选填“大于”、“等于”或“小于”)。
(2)图中D点处溶液中含有的溶质是______。
(3)盐酸的质量分数是______。
(4)当滴加NaOH溶液至260g时,沉淀的质量m2的值是多少?(写出计算过程)

(1)滤液X的pH______7(选填“大于”、“等于”或“小于”)。
(2)图中D点处溶液中含有的溶质是______。
(3)盐酸的质量分数是______。
(4)当滴加NaOH溶液至260g时,沉淀的质量m2的值是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】现有一瓶敞口放置在空气中的氢氧化钠样品,为了探究样品变质的情况,某兴趣小组进行了如图1所示实验,加入稀盐酸的质量与产生气体质量的关系如图2所示。请结合图1、2中的实验数据,完成以下计算:

(1)图2中b的数值是____________ 。
(2)完全反应时产生气体的质量是____________ g。
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果精确到0.01%)。

(1)图2中b的数值是
(2)完全反应时产生气体的质量是
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果精确到0.01%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】在一烧杯中盛有l00gBaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示:
请根据题意回答问题:
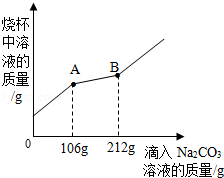
(1)在实验过程中,有气体放出,还可以看到的明显实验现象是 .
(2)在实验过程中放出气体的总质量为 g.
(3)当滴入Na2CO3溶液至图中B点时,计算此时所得不饱和溶液中溶质质量分数是多少?(计算结果精确到0.1%) .
请根据题意回答问题:

(1)在实验过程中,有气体放出,还可以看到的明显实验现象是 .
(2)在实验过程中放出气体的总质量为 g.
(3)当滴入Na2CO3溶液至图中B点时,计算此时所得不饱和溶液中溶质质量分数是多少?(计算结果精确到0.1%) .
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入溶质质量分数为26.5%的碳酸钠溶液,测得溶液pH随加入碳酸钠溶液质量的变化曲线如下图所示。

回答下列问题:
⑴A点处溶液中溶质的化学式是CaCl2和______________;
⑵计算原滤液中氯化钙的质量分数为_____________(写出计算过程,结果精确到0.1%)。
⑶根据计算所得数据在下图中画出产生沉淀的曲线。
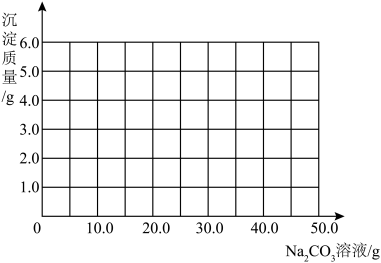 _______________
_______________
⑷CD段pH上升的原因是________________________________。

回答下列问题:
⑴A点处溶液中溶质的化学式是CaCl2和______________;
⑵计算原滤液中氯化钙的质量分数为_____________(写出计算过程,结果精确到0.1%)。
⑶根据计算所得数据在下图中画出产生沉淀的曲线。
 _______________
_______________⑷CD段pH上升的原因是________________________________。
您最近一年使用:0次



