小丽同学家里有一只破损的手镯(银锌合金),她想探究此手镯中银的含量。首先称得手镯质量为12g。在用足量的稀硫酸分多次与此手镯充分反应,实验结果如表:
根据上表中的数据分析,完成下列问题:
(1)从第______ 次实验开始,稀硫酸有剩余:表格中m=_________ 。
(2)该手镯中银的质量分数是____________ 。
(3)所用稀硫酸的溶质质量分数是多少?(写出计算过程)
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
| 充分反应后剩余固体的质量/g | 11.35 | 10.7 | 10.05 | 9.6 | m |
根据上表中的数据分析,完成下列问题:
(1)从第
(2)该手镯中银的质量分数是
(3)所用稀硫酸的溶质质量分数是多少?(写出计算过程)
更新时间:2021-09-25 13:22:34
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】小江同学为了寻找含碳酸钙质量分数超过85%的石灰石,对一样品进行了如下定量实验(石灰石样品中的杂质不与盐酸反应).
试通过计算,分析该石灰石样品中碳酸钙的质量分数是否符合要求?_____
| 实验步骤 | 将适量盐酸加入烧杯中并称重 | 称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | 待反应完全后,称重 |
| 实验数据 | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。小柯利用如图装置测定疏通剂中铝的质量分数。

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O=_____NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。_____

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
| 反应前总质量m1 | 反应后总质量m2 |
| 371.84g | 371.24g |
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O=_____NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。_____
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】“黄铜”是铜、锌合金。“黄铜”中的铜可用由黄铜矿(主要成分是CuFeS2)炼制而成。为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56g)
请回答:
(1)CuFeS2中铜、铁、硫元素的质量比为_____。若CuFeS2中含硫的质量为128g,则CuFeS2的质量为_____g;
(2)_____同学取用的稀盐酸过量;
(3)_____同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是_____g。
(4)求样品中锌的质量分数?(写出计算过程,精确到0.1%)
| 甲 | 乙 | 丙 | |
| 烧杯+稀盐酸质量 | 139g | 129g | 129g |
| 加入黄铜样品质量 | 20g | 24g | 20g |
| 充分反应后,烧杯+剩余物质质量 | 158.8g | 152.8g | 148.8g |
请回答:
(1)CuFeS2中铜、铁、硫元素的质量比为_____。若CuFeS2中含硫的质量为128g,则CuFeS2的质量为_____g;
(2)_____同学取用的稀盐酸过量;
(3)_____同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是_____g。
(4)求样品中锌的质量分数?(写出计算过程,精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某种铁合金中含有不溶于酸的杂质。取该合金样品粉末11.4g,分四次向其中加入稀盐酸共100g。反应过程的有关数据记录如下表。
(1)a=________。
(2)所得溶液溶质的质量分数(请写出计算过程)。
| 次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 8.6 | a | 3 | 0.2 |
(1)a=________。
(2)所得溶液溶质的质量分数(请写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】黄铜是铜锌合金。取10g黄铜于烧杯中,将120g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
(1)该合金属于___________ 。(填物质类别)
(2)表中m=___________ 。
(3)所用稀硫酸的溶质质量分数(请根据化学方程式写出规范的计算步骤)
(4)请在下图画出:往10g黄铜加入稀硫酸,生成氢气质量的图像。
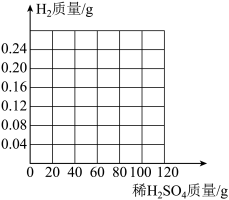
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 |
| 加入硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 剩余物的质量/g | 129.96 | 149.92 | m | 189.84 | 209.80 | 229.80 |
(2)表中m=
(3)所用稀硫酸的溶质质量分数(请根据化学方程式写出规范的计算步骤)
(4)请在下图画出:往10g黄铜加入稀硫酸,生成氢气质量的图像。

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:

(1)实验过程中产生的CO2气体的质量为___ g
(2)计算CaCO3中各元素的质量比___ .
(3)计算反应后的CaCl2 不饱和溶液中溶质的质量分数____ (写出计算过程,结果精确到0.1%).

(1)实验过程中产生的CO2气体的质量为
(2)计算CaCO3中各元素的质量比
(3)计算反应后的CaCl2 不饱和溶液中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】现有FeCl3和CuCl2的混合溶液195.2g,向其中加入铁粉反应的先后顺序为:2FeCl3+Fe=3FeCl2,CuCl2+Fe=FeCl2+Cu。加入铁粉质量与反应后溶液中剩余固体质量的关系如图所示。

(1)m(剩余固体)>6.4g时,剩余固体的成分是_____ (填化学式)。
(2)求当加入11.2g铁粉时,反应后所得溶液中FeCl2的质量分数(写出计算过程)。

(1)m(剩余固体)>6.4g时,剩余固体的成分是
(2)求当加入11.2g铁粉时,反应后所得溶液中FeCl2的质量分数(写出计算过程)。
您最近一年使用:0次




