现有一瓶敞口放置在空气中的氢氧化钠样品,为了探究样品变质的情况,某兴趣小组进行了如图1所示实验,加入稀盐酸的质量与产生气体质量的关系如图2所示。请结合图1、2中的实验数据,完成以下计算:

(1)图2中b的数值是____________ 。
(2)完全反应时产生气体的质量是____________ g。
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果精确到0.01%)。

(1)图2中b的数值是
(2)完全反应时产生气体的质量是
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果精确到0.01%)。
更新时间:2021-08-28 16:04:23
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】南岸区文峰水泥厂新进了一批石灰石原料,为了测定石灰石在碳酸钙的质量分数,该厂化验室取一定量的石灰石样品与100g过量的稀盐酸在烧杯中反应(样品中杂质不溶于水,也不与稀盐酸反应),有关实验数据如下表:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为___________g;
(2)该石灰石中碳酸钙的质量分数为___________;
(3)将烧杯中的混合物过滤,向滤液中加入过量的硝酸银溶液,充分反应生成57.4g白色沉淀。假定实验过程中无损耗,则稀盐酸中溶质的质量分数为多少?(结果保留一位小数)
| 反应前 | 反应后 | |
| 烧杯和稀盐酸的总重量 | 石灰石样品的质量 | 烧杯和其中混合物的总质量 |
| 200.0g | 12.5g | 208.1g |
(2)该石灰石中碳酸钙的质量分数为___________;
(3)将烧杯中的混合物过滤,向滤液中加入过量的硝酸银溶液,充分反应生成57.4g白色沉淀。假定实验过程中无损耗,则稀盐酸中溶质的质量分数为多少?(结果保留一位小数)
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】为了测定某含杂质7%的黄铜样品中铜的质量分数(主要成分是铜和锌,杂质不溶于水,不与其他物质反应,受热也不分解),某化学小组进行了如下实验:
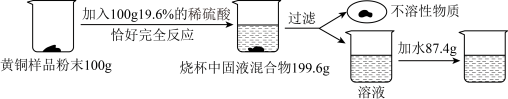
(1)该黄铜样品中铜的质量分数为?
(2)向过滤后所得滤液中加入87.4g水,计算最终所得溶液中溶质的质量分数。

(1)该黄铜样品中铜的质量分数为?
(2)向过滤后所得滤液中加入87.4g水,计算最终所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】向由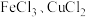 和
和 组成的
组成的 混合溶液中,慢慢滴加一定质量分数的
混合溶液中,慢慢滴加一定质量分数的 溶液,其反应过程如图所示。当反应进行至B点时,溶液完全变成蓝色;
溶液,其反应过程如图所示。当反应进行至B点时,溶液完全变成蓝色; 段共消耗
段共消耗 溶液
溶液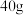 。请完成下列问题:
。请完成下列问题:

(1) 溶液中溶质的质量分数为多少?
溶液中溶质的质量分数为多少?
(2)原溶液中 与
与 的质量比为多少?
的质量比为多少?
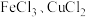 和
和 组成的
组成的 混合溶液中,慢慢滴加一定质量分数的
混合溶液中,慢慢滴加一定质量分数的 溶液,其反应过程如图所示。当反应进行至B点时,溶液完全变成蓝色;
溶液,其反应过程如图所示。当反应进行至B点时,溶液完全变成蓝色; 段共消耗
段共消耗 溶液
溶液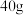 。请完成下列问题:
。请完成下列问题:
(1)
 溶液中溶质的质量分数为多少?
溶液中溶质的质量分数为多少?(2)原溶液中
 与
与 的质量比为多少?
的质量比为多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为测定某纯碱样品(含氢氧化钠杂质)中碳酸钠的含量,进行如下实验:取65g纯碱样品平均分为5份,分别加入相同质量分数的稀盐酸溶液,获得如下实验数据:
(1)13g样品完全反应时放出气体的质量是_____ g。
(2)纯碱样品中Na2CO3的质量分数是_____ 。(结果保留小数点后一位)
(3)盐酸中溶质的质量分数是多少?(写出计算过程)
(4)若向13g样品中持续不断的加入稀盐酸,请你画出加入稀盐酸与生成气体的质量关系图。(在答题卡的坐标中作图)

| 实验 | 1 | 2 | 3 | 4 | 5 |
| 样品质量/g | 13 | 13 | 13 | 13 | 13 |
| 加入盐酸质量/g | 15 | 30 | 80 | 130 | 150 |
| 反应后物质质量/g | 28 | 43 | 90.8 | 138.6 | 158.6 |
(1)13g样品完全反应时放出气体的质量是
(2)纯碱样品中Na2CO3的质量分数是
(3)盐酸中溶质的质量分数是多少?(写出计算过程)
(4)若向13g样品中持续不断的加入稀盐酸,请你画出加入稀盐酸与生成气体的质量关系图。(在答题卡的坐标中作图)

您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】某化学兴趣小组取9.87g部分变质的熟石灰样品放入大烧杯中,加入255.51g水,充分搅拌至熟石灰全部溶解后,通入足量的CO2,溶质质量与反应的CO2质量的关系如图所示,

求通入m2gCO2时所得溶液的溶质质量分数。【提示:CaCO3+H2O+CO2=Ca(HCO3)2】

求通入m2gCO2时所得溶液的溶质质量分数。【提示:CaCO3+H2O+CO2=Ca(HCO3)2】
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究。
【提出问题】这瓶NaOH溶液变质程度如何呢?
【提出猜想】小明的猜想:NaOH溶液部分变质。
【实验探究】小明设计如下实验来验证自己的猜想,请根据表中内容填写 小明实验时的现象:
【深入研究】通过实际实验,确认这瓶放置已久的NaOH溶液部分变质。现从该瓶中取了100g 溶液,向其中逐滴加入稀盐酸,至恰好不再产生气泡时共消耗稀盐酸73g,同时产生CO2气体2.2g,此时测得溶液的pH=7。
(2)恰好反应时所得溶液的质量是_______________ g。
(3)求这瓶溶液中Na2CO3的质量分数为_________ 。( 写出计算过程)
【提出问题】这瓶NaOH溶液变质程度如何呢?
【提出猜想】小明的猜想:NaOH溶液部分变质。
【实验探究】小明设计如下实验来验证自己的猜想,请根据表中内容
| 实验步骤 | 实验现象 | 结论 |
| ①取样,滴加足量的CaCl2溶液。 | 产生白色沉淀。 | NaOH溶液部分变质。 |
| ②过滤,用pH试纸测溶液的pH。 | (1)pH |
【深入研究】通过实际实验,确认这瓶放置已久的NaOH溶液部分变质。现从该瓶中取了100g 溶液,向其中逐滴加入稀盐酸,至恰好不再产生气泡时共消耗稀盐酸73g,同时产生CO2气体2.2g,此时测得溶液的pH=7。
(2)恰好反应时所得溶液的质量是
(3)求这瓶溶液中Na2CO3的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】为得到高纯度碳酸钙,实验室用Na2CO3溶液与CaCl2溶液反应制取。现将150gCaCl2溶液分四次加入盛有100gNa2CO3溶液的烧杯中,充分反应,四次测量所得数据见下表:
(1)第___________次恰好完全反应,此时生成沉淀的总质量为___________g。
(2)第四次测量时,所得溶液中的溶质有___________(填化学式)。
(3)CaCl2溶液的溶质的质量分数为___________。(写出计算过程)
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 累计加入CaCl2溶液的质量/g | 40 | 80 | 120 | 150 |
| 烧杯中溶液的总质量/g | 134 | 168 | 202 | 232 |
(1)第___________次恰好完全反应,此时生成沉淀的总质量为___________g。
(2)第四次测量时,所得溶液中的溶质有___________(填化学式)。
(3)CaCl2溶液的溶质的质量分数为___________。(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】现有碳酸钠和氯化钠的混合物15g,将其放入烧杯中加入100g水,使其完全溶解。向所得溶液中加入溶质质量分数为9.8%的稀硫酸,烧杯中溶液的质量与加入稀硫酸的质量关系如图所示,请回答下列问题。

(1)B点时烧杯中溶液含有的溶质是______ 。(填化学式)
(2)恰好完全反应时加入稀硫酸的质量为多少克?(写出计算过程)
(3)混合物中氯化钠的质量是多少克?(写出计算过程)

(1)B点时烧杯中溶液含有的溶质是
(2)恰好完全反应时加入稀硫酸的质量为多少克?(写出计算过程)
(3)混合物中氯化钠的质量是多少克?(写出计算过程)
您最近一年使用:0次



