制碱工业在实际生产的产品碳酸钠中会混有少量的氯化钠,现有纯碱样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体全部逸出,得到不饱和氯化钠溶液。反应过程中测得烧杯内溶液的质量(m)与反应时间(t)关系如图所示。

试回答:
(1)生成CO2的质量为______ g。
(2)26.5g样品中碳酸钠的质量分数为多小?(写出计算过程,结果精确到0.1%下同。)
(3)请计算所得溶液中溶质的质量分数。

试回答:
(1)生成CO2的质量为
(2)26.5g样品中碳酸钠的质量分数为多小?(写出计算过程,结果精确到0.1%下同。)
(3)请计算所得溶液中溶质的质量分数。
更新时间:2021-11-07 16:55:05
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】2022年成都世界乒乓球团体锦标赛于10月9日在中国四川成都落下帷幕,中国队再次蝉联男女团冠军。制作乒乓球材料“聚酯纤维”常用对苯二甲酸(化学式为C8H6O4)和乙二醇为原料制的。
(1)对苯二甲酸中的碳、氢元素的质量比为______ 。
(2)对苯二甲酸中氧元素的质量分数为______ 。(精确到0.1%)【写出计算过程】
(3)3.1g乙二醇在空气中完全燃烧,产生4.4gCO2和2.7gH2O,则乙二醇中一定含有______ (填元素符号)元素。
(1)对苯二甲酸中的碳、氢元素的质量比为
(2)对苯二甲酸中氧元素的质量分数为
(3)3.1g乙二醇在空气中完全燃烧,产生4.4gCO2和2.7gH2O,则乙二醇中一定含有
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小王同学取22g固体混合物置于烧杯中,将100 g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
回答下列问题:
(1)原固体混合物中氧化铜的质量为________ 。
(2)计算该实验所用稀硫酸中溶质的质量分数。(写出计算过程.结果精确到0.1%)
| 次序 | ① | ② | ③ | ④ |
| 加入稀硫酸的质量/g | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 16 | a | 12 | 12 |
(1)原固体混合物中氧化铜的质量为
(2)计算该实验所用稀硫酸中溶质的质量分数。(写出计算过程.结果精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:

按要求回答下列问题:
(1)根据实验数据分析,从第________ 份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数________________ 。(要求写出计算过程)
(3)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线____________ 。
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量(g) | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |

按要求回答下列问题:
(1)根据实验数据分析,从第
(2)列式计算该黄铜样品中金属锌的质量分数
(3)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】为测定某硫酸溶液中溶质的质量分数,化学小组同学取 10g 该硫酸溶液,向其中加入21.2g BaCl2 溶液,二者恰好完全反应,过滤后称得滤液的质量为28.87g。请计算:(温馨提示: )
)
(l)反应后生成沉淀的质量是______g。
(2)该硫酸溶液中溶质的质量分数。(计算结果精确到 0.1%)。
 )
)(l)反应后生成沉淀的质量是______g。
(2)该硫酸溶液中溶质的质量分数。(计算结果精确到 0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】过氧化氢溶液俗称双氧水,是一种常见消毒剂,实验员用以下方法制取了少量过氧化氢溶液,在低温下,向119.2g某浓度的稀硫酸中逐渐加入一定量的过氧化钡(BaO2),发生的化学反应BaO2+H2SO4=BaSO4↓+H2O2,当恰好完全反应时,生成69.9g沉淀。计算:
(1)加入BaO2的质量为______ g。
(2)反应后所得溶液中溶质质量分数。
(3)医用双氧水常为溶质质量分数为3%的过氧化氢溶液,如果将(2)中所得溶液稀释到医用双氧水浓度,计算需加入水的质量。
(1)加入BaO2的质量为
(2)反应后所得溶液中溶质质量分数。
(3)医用双氧水常为溶质质量分数为3%的过氧化氢溶液,如果将(2)中所得溶液稀释到医用双氧水浓度,计算需加入水的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】现有一份部分变质的氢氧化钠固体,为了除去其中的杂质,进行了如下操作,请回答问题:
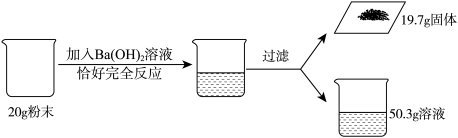
(1)写出发生反应的化学方程式为__________。
(2)根据已知条件列出所加溶液溶质质量(x)的比例式为__________。
(3)求已变质与未变质氢氧化钠的质量最简整数比为__________。
(4)计算所加溶液的溶质质量分数为__________。
(5)若要把除杂后的溶液配制成10%的溶液,需要__________(填“蒸发”或“加入”)水__________g。

(1)写出发生反应的化学方程式为__________。
(2)根据已知条件列出所加溶液溶质质量(x)的比例式为__________。
(3)求已变质与未变质氢氧化钠的质量最简整数比为__________。
(4)计算所加溶液的溶质质量分数为__________。
(5)若要把除杂后的溶液配制成10%的溶液,需要__________(填“蒸发”或“加入”)水__________g。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐1】某氢氧化钠样品中混有少量氯化钠,为测定样品中氢氧化钠的质量分数,称取5g样品,加入27g水完全溶解后,缓慢加入稀盐酸,同时测定溶液的pH=7时,刚好用去10%的稀盐酸36.5g,试计算:
(1)将100g质量分数为38%的浓盐酸稀释成10%的稀盐酸,需加水的质量为________g。
(2)样品中氢氧化钠的质量分数为___________。
(3)反应后所得溶液中溶质的质量分数为________。
(1)将100g质量分数为38%的浓盐酸稀释成10%的稀盐酸,需加水的质量为________g。
(2)样品中氢氧化钠的质量分数为___________。
(3)反应后所得溶液中溶质的质量分数为________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,环保小组的同学进行了以下实验。取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液。测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图。根据所得数据计算:

①500g废水中加入氢氧化钠溶液充分反应后,得到沉淀的物质的量是_____ mol。
②该废水中硫酸铜的溶质质量分数。(写出计算过程)_______________
③该废水中硫酸的物质的量是___________ 。

①500g废水中加入氢氧化钠溶液充分反应后,得到沉淀的物质的量是
②该废水中硫酸铜的溶质质量分数。(写出计算过程)
③该废水中硫酸的物质的量是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如表实验数据:
请通过计算回答:
(1)表中m的值为______;
(2)原固体混合物中的MgCl2质量分数是多少_____?(要求写出计算过程)
(3)加入氢氧化钠溶液的溶质质量分数是多少_____?
实验次数 | 一 | 二 | 三 | 四 |
固体混合物的质量(g) | 20 | 20 | 20 | 20 |
加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
(1)表中m的值为______;
(2)原固体混合物中的MgCl2质量分数是多少_____?(要求写出计算过程)
(3)加入氢氧化钠溶液的溶质质量分数是多少_____?
您最近一年使用:0次




