1 . 某兴趣小组在完成镁与稀盐酸反应的实验时,观察到有灰白色沉淀生成的“异常”现象,他们对此进行了以下探究。
【猜想假设】猜想1:Mg猜想2:MgCl2
【交流讨论】
(1)小张认为沉淀还可能是MgCO3,小王认为这一猜想是错误的,理由是______ 。
【实验I】
(2)为验证猜想2是否正确,同学们取1g样品并加入足量蒸馏水振荡,沉淀未溶解。同学们又取_______ 于试管中,也加足量蒸馏水振荡,固体全部溶解,证实猜想2错误。
【深入探究】该沉淀的物质组成
【查阅资料】灰白色沉淀的成分为碱式氯化镁。它存在多种组成,化学式可表示为Mgx(OH)yClz·nH2O;它受热分解可产生氧化镁、氯化氢和水。
【实验Ⅱ】
(3)为确定分解后的产物,同学们分别取样于试管中加热,将产物通过硫酸铜固体,看到______ ,证明有水产生,将产物通入______ 中,看到溶液呈红色,证明有氯化氢产生。
【实验III】
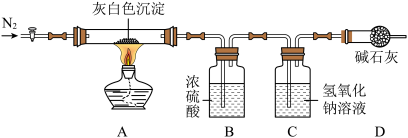
洗去沉淀表面杂质并室温晾干。取其7.07g,用如图装置(夹持仪器未画出)按照正确的操作步骤进行实验。待反应停止后,测得硬质玻璃管中剩余固体质量为4.00g,装置B的质量增加了2.34g。
(4)按图连接好装置,实验前要先_______ 。
(5)反应停止后,应继续通入N2一段时间,目的是______ ;该沉淀中,镁、氯的离子个数比n(Mg2+):n(Cl-)=______ 。
(6)若该沉淀Mgx(OH)yClz•nH2O中,n=5,则x、y、z的数值为_______ 。
【反思与评价】
(7)装置B、C顺序是否可以调换?请判断并叙述理由______ 。
(8)若无装置D,则测得的y数值会_______ (填偏大、偏小、不变)。
【猜想假设】猜想1:Mg猜想2:MgCl2
【交流讨论】
(1)小张认为沉淀还可能是MgCO3,小王认为这一猜想是错误的,理由是
【实验I】
(2)为验证猜想2是否正确,同学们取1g样品并加入足量蒸馏水振荡,沉淀未溶解。同学们又取
【深入探究】该沉淀的物质组成
【查阅资料】灰白色沉淀的成分为碱式氯化镁。它存在多种组成,化学式可表示为Mgx(OH)yClz·nH2O;它受热分解可产生氧化镁、氯化氢和水。
【实验Ⅱ】
(3)为确定分解后的产物,同学们分别取样于试管中加热,将产物通过硫酸铜固体,看到
【实验III】
洗去沉淀表面杂质并室温晾干。取其7.07g,用如图装置(夹持仪器未画出)按照正确的操作步骤进行实验。待反应停止后,测得硬质玻璃管中剩余固体质量为4.00g,装置B的质量增加了2.34g。
(4)按图连接好装置,实验前要先
(5)反应停止后,应继续通入N2一段时间,目的是
(6)若该沉淀Mgx(OH)yClz•nH2O中,n=5,则x、y、z的数值为
【反思与评价】
(7)装置B、C顺序是否可以调换?请判断并叙述理由
(8)若无装置D,则测得的y数值会
您最近一年使用:0次
2 . CuSO4溶液是初中化学常见的一种试剂。
(1)农业上常用它配置波尔多液杀菌剂
①写出配置波尔多液过程中的化学方程式:______ 。
②在烧杯中放入20mL某硫酸铜溶液,逐滴加入某浓度的澄清石灰水,测定混合液pH随滴入Ca(OH)2溶液体积的变化,结果如图。下列说法正确的是______ (填字母)(已知:溶液中自由移动离子的浓度越小,溶液的导电性越差)。
C.ab段烧杯内溶液的导电性逐渐降低 D.bc段烧杯内沉淀质量不断增加
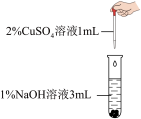
(2)兴趣小组同学在做硫酸铜和氢氧化钠反应的实验时,发现滴加试剂的顺序不同会产生不同的现象。
【提出问题】乙组产生的蓝绿色沉淀的成分是什么呢?
【查阅资料】Ⅰ、NaOH和CuSO4溶液混合可生成Cu(OH)2、Cux(OH)y(SO4)z等多种产物。
Ⅱ、68℃时,Cu(OH)2发生分解,生成两种氧化物;300℃左右Cux(OH)y(SO4)z发生分解。
【实验探究】将乙组反应后的物质过滤、洗涤、低温干燥得蓝绿色固体样品。小组同学称取27.6g样品,在老师的指导下进行实验。
②控制温度为68℃,对样品进行热分解,至固体质量不再减少,再通一段时间N2。冷却后测得装置B增重1.8g。
A.样品中Cu(OH)2的质量为______ 。
B、若实验后没有继续通一段时间N2导致计算Cu(OH)2的质量结果______ (填“偏大/偏小/不变”)
③为了进一步确定装置A中加热后的剩余固体组成,小组同学又进行了以下步骤:______ 。
(1)农业上常用它配置波尔多液杀菌剂
①写出配置波尔多液过程中的化学方程式:
②在烧杯中放入20mL某硫酸铜溶液,逐滴加入某浓度的澄清石灰水,测定混合液pH随滴入Ca(OH)2溶液体积的变化,结果如图。下列说法正确的是
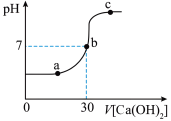
C.ab段烧杯内溶液的导电性逐渐降低 D.bc段烧杯内沉淀质量不断增加
(2)兴趣小组同学在做硫酸铜和氢氧化钠反应的实验时,发现滴加试剂的顺序不同会产生不同的现象。
| 实验组 | 甲组 | 乙组 |
| 实验操作 |
|
|
| 实验现象 | 产生蓝色沉淀 | 产生蓝绿色沉淀 |
【查阅资料】Ⅰ、NaOH和CuSO4溶液混合可生成Cu(OH)2、Cux(OH)y(SO4)z等多种产物。
Ⅱ、68℃时,Cu(OH)2发生分解,生成两种氧化物;300℃左右Cux(OH)y(SO4)z发生分解。
【实验探究】将乙组反应后的物质过滤、洗涤、低温干燥得蓝绿色固体样品。小组同学称取27.6g样品,在老师的指导下进行实验。
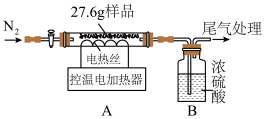
②控制温度为68℃,对样品进行热分解,至固体质量不再减少,再通一段时间N2。冷却后测得装置B增重1.8g。
A.样品中Cu(OH)2的质量为
B、若实验后没有继续通一段时间N2导致计算Cu(OH)2的质量结果
③为了进一步确定装置A中加热后的剩余固体组成,小组同学又进行了以下步骤:

您最近一年使用:0次
3 . 将一定质量铁的氧化物FexOy和mgCO置于密闭容器中、高温下使其充分反应。反应过程中,容器内部分物质的质量变化如图所示。下列说法错误的是

| A.反应结束后,剩余CO的质量为5.6g |
| B.FexOy完全反应生成CO2的质量为17.6g |
| C.实际参加反应的CO质量为11.2g |
| D.铁的氧化物FexOy中x:y=2:3 |
您最近一年使用:0次
4 . 实验室常用燃烧法测定有机物的组成。某有机物2.6g在一定量的氧气中完全燃烧,生成4.4g二氧化碳、2.8g一氧化碳和1.8g水,此过程中消耗氧气的质量为________ ;若进一步测定该有机物的相对分子质量为26,则该有机物的化学式为________ 。
您最近一年使用:0次
5 . 一种只含碳、氢元素的有机化合物中,碳元素和氢元素的质量比为24:5,则该化合物的化学式可能是
| A.CH4 | B.C2H2 | C.C3H8 | D.C4H10 |
您最近一年使用:0次
6 . 发射通讯卫星的火箭用联氨( )做燃料,用四氧化二氮(
)做燃料,用四氧化二氮( )助燃,反应的化学方程式如下:
)助燃,反应的化学方程式如下: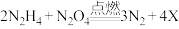 ,生成物不会对大气造成污染。
,生成物不会对大气造成污染。
(1)X的化学式是______ 。
(2)求用12.8 kg联氨做燃料需要助燃物 的质量。
的质量。
 )做燃料,用四氧化二氮(
)做燃料,用四氧化二氮( )助燃,反应的化学方程式如下:
)助燃,反应的化学方程式如下: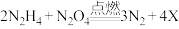 ,生成物不会对大气造成污染。
,生成物不会对大气造成污染。(1)X的化学式是
(2)求用12.8 kg联氨做燃料需要助燃物
 的质量。
的质量。
您最近一年使用:0次
7 . 工业上是用甲基丙烯酸甲酯来合成有机玻璃。已知甲基丙烯酸甲酯由碳、氢、氧三种元素组成,其中碳元素的质量分数为60%,氢元素的质量分数为8%;该物质的一个分子中含有2个氧原子。请回答:
(1)甲基丙烯酸甲酯的化学式量为_______ 。
(2)该物质的化学式为_______ 。
(1)甲基丙烯酸甲酯的化学式量为
(2)该物质的化学式为
您最近一年使用:0次
8 . 某化合物由碳、氢两种元素组成,其中碳、氢元素的质量比为4:1.若该化合物的相对分子质量为30,则该化合物的化学式为
| A.CH3 | B.C2H6 | C.CH18 | D.C4H |
您最近一年使用:0次
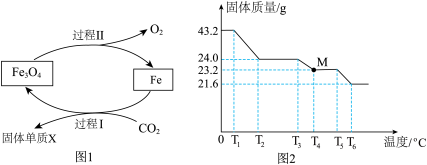
9 . CO2作为最主要的温室气体,其低能耗捕集、转化和利用正受到世界的关注。科学家研究发现,在一定条件下可以将CO2转化为某固体单质X,反应原理如图1所示。_______ (填化学式)。
(2)过程Ⅱ的化学方程式为 ,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)
,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)
(3)杭州亚运会生产电动车锂电池所用到的草酸亚铁(FeC2O4)在不同温度下分解能得到不同的铁的氧化物,同时放出气体。
i.FeC2O4中碳元素的化合价为_______ 。
ii.43.2gFeC2O4受热分解所得固体质量随温度的变化如图2所示。_______ °C时,固体M开始分解;请通过计算分析固体M的化学式_______ 。
(2)过程Ⅱ的化学方程式为
 ,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)
,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)(3)杭州亚运会生产电动车锂电池所用到的草酸亚铁(FeC2O4)在不同温度下分解能得到不同的铁的氧化物,同时放出气体。
i.FeC2O4中碳元素的化合价为
ii.43.2gFeC2O4受热分解所得固体质量随温度的变化如图2所示。
您最近一年使用:0次
2024-01-17更新
|
207次组卷
|
2卷引用:广东省佛山市禅城区2023-2024学年九年级上学期期末考试化学试题
名校
10 . 人体缺乏维生素C会引起坏血病,下图是维生素C的说明书部分信息。计算:
(1)维生素C的化学式为_____ 。
(2)维生素C中碳、氢、氧元素的质量比为_____ (写最简比)。
(3)维生素C中碳元素的质量分数是_____ (结果精确到 )。
)。
(4)若成人按说明书用量服用,则每日从该片剂中摄入的维生素C的质量为_____  。
。
| 某品牌维生素C(片剂) 化学式: 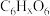 相对分子质量:176 规格:每片含维生素C  用法与用量:一日3次,成人每次2片…… |
(2)维生素C中碳、氢、氧元素的质量比为
(3)维生素C中碳元素的质量分数是
 )。
)。(4)若成人按说明书用量服用,则每日从该片剂中摄入的维生素C的质量为
 。
。
您最近一年使用:0次