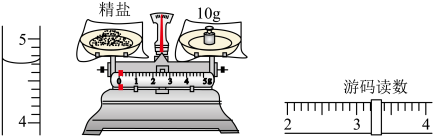
一定质量分数溶液的配制是初中化学重要的探究实验。某化学兴趣小组用氯化钠配制50g溶质质量分数为6%的氯化钠溶液。
(1)现有以下操作:①溶解、②称取氯化钠、③过滤、④量取水、⑤计算。请从以上操作中选出正确的操作顺序是______ 。
(2)若其它操作正确,量取水时仰视量筒读数,对结果会造成什么影响?
(3)用已配好的50g溶质质量分数为6%的氯化钠溶液,配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为______ g。
(1)现有以下操作:①溶解、②称取氯化钠、③过滤、④量取水、⑤计算。请从以上操作中选出正确的操作顺序是
(2)若其它操作正确,量取水时仰视量筒读数,对结果会造成什么影响?
(3)用已配好的50g溶质质量分数为6%的氯化钠溶液,配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为
更新时间:2022-03-05 19:37:17
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
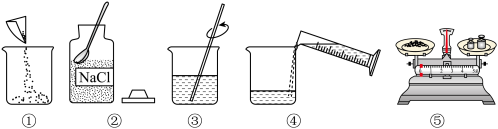
(1)用图表示的序号表示配制溶液的正确操作顺序:_______ 。
(2)图②中,有一种塑料仪器,其名称是______ 。
(3)配置50g质量分数为10%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠___ g,水____ g。
(4)称量氯化钠时,如发现指针向左偏转,则应该进行的操作是:_______ 。
(5)下列操作会导致实验结果偏小的是 。
①称量的氯化钠固体中含有不溶性杂质
②用量筒量取水时仰视读数
③往烧杯中加水有液体溅出
④将配制好的溶液装入试剂瓶中有少量溅出

(1)用图表示的序号表示配制溶液的正确操作顺序:
(2)图②中,有一种塑料仪器,其名称是
(3)配置50g质量分数为10%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠
(4)称量氯化钠时,如发现指针向左偏转,则应该进行的操作是:
(5)下列操作会导致实验结果偏小的是 。
①称量的氯化钠固体中含有不溶性杂质
②用量筒量取水时仰视读数
③往烧杯中加水有液体溅出
④将配制好的溶液装入试剂瓶中有少量溅出
| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
【推荐2】某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只有含少量NaCl的KNO3固体药品。如图所示,回答下列问题。
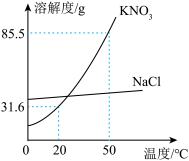
(1)如图所示50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的______ 溶液(填“饱和”或“不饱和”)。
(2)提纯KNO3的方法是______ 。
(3)小明用提纯后的KNO3固体配制100g溶质质量分数为5%的KNO3溶液,经检测,所配溶液中KNO3溶质质量分数偏大,其原因可能是______ 。
①KNO3固体仍然不纯;
②溶解前,烧杯中有水;
③量取水时,俯视读数;
④装瓶时,有少量溶液洒出。

(1)如图所示50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的
(2)提纯KNO3的方法是
(3)小明用提纯后的KNO3固体配制100g溶质质量分数为5%的KNO3溶液,经检测,所配溶液中KNO3溶质质量分数偏大,其原因可能是
①KNO3固体仍然不纯;
②溶解前,烧杯中有水;
③量取水时,俯视读数;
④装瓶时,有少量溶液洒出。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】食盐是生活必需品,是重要的化工原料,也是同学们实验时常用的药品。
(1)食盐中含有各种添加剂,如添加碘酸钾(KIO3)补充碘元素、添加亚铁氰化钾(K4[Fe(CN)6]3H2O)作为抗结剂防止食盐结块。
①食盐中至少含有_____________ 种金属元素(填数字)。
②亚铁氰化钾中的金属离子是 K+和____________ (填微粒符号)。
(2)电解饱和食盐水可以得到多种化工产品,主要过程如下:

①若气体A 是一种单质,则该气体为__________ ,你猜想的依据是 _____________ 。
②电解生成氢氧化钠的化学方程式为_____________ 。
③酸D溶液中溶质的化学式为_________________ 。
(3)如图是实验室配制一定溶质质量分数的氯化钠溶液的流程图。
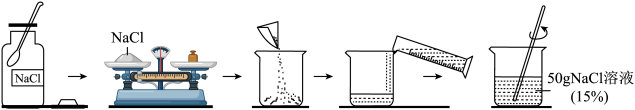
请回答:
①应称量____________ g氯化钠固体,需加水 _____________ mL。
②若称量氯化钠固体时指针向右偏转,则应______________ 直到天平平衡。
③实验中发现氯化钠固体已结块,为了较快地溶解,合理的方法有_____________ (填序号)。
A.用玻璃棒将氯化钠固体捣碎 B.用热水溶解
C.加入更多的水 D.用玻璃棒搅拌
④下列操作中可能导致配制氯化钠溶液的溶质质量分数偏小的是___________ (填序号)。
A.氯化钠中含有杂质 B.量取水时仰视
C.用已有少量水的烧杯溶解氯化钠 D.转移时,有少量溶液溅出
⑤取上述溶液10g,需加______________ g水稀释,可得到5%的氯化钠溶液。

(1)食盐中含有各种添加剂,如添加碘酸钾(KIO3)补充碘元素、添加亚铁氰化钾(K4[Fe(CN)6]3H2O)作为抗结剂防止食盐结块。
①食盐中至少含有
②亚铁氰化钾中的金属离子是 K+和
(2)电解饱和食盐水可以得到多种化工产品,主要过程如下:

①若气体A 是一种单质,则该气体为
②电解生成氢氧化钠的化学方程式为
③酸D溶液中溶质的化学式为
(3)如图是实验室配制一定溶质质量分数的氯化钠溶液的流程图。

请回答:
①应称量
②若称量氯化钠固体时指针向右偏转,则应
③实验中发现氯化钠固体已结块,为了较快地溶解,合理的方法有
A.用玻璃棒将氯化钠固体捣碎 B.用热水溶解
C.加入更多的水 D.用玻璃棒搅拌
④下列操作中可能导致配制氯化钠溶液的溶质质量分数偏小的是
A.氯化钠中含有杂质 B.量取水时仰视
C.用已有少量水的烧杯溶解氯化钠 D.转移时,有少量溶液溅出
⑤取上述溶液10g,需加

您最近一年使用:0次
【推荐1】水是一种重要的资源,人类生活、生产活动中处处离不开水及水溶液.
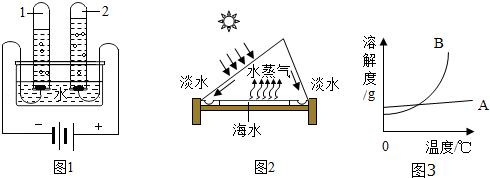
(1)电解水实验揭示了水的组成,图1实验中得到氧气的试管是__________ (填“1”或“2”).
(2)自来水厂净水过程中用到活性炭,其作用是___________ .
(3)消防队员常用高压水枪灭火,其灭火的原理是_________ ;
(4)将下列物质分别加入水中,不能形成溶液的是_________ (填序号)
A.冰块 B.二氧化碳 C.食盐 D.酒精
(5)海水淡化可缓解淡水资源匮乏的问题,图2为太阳能海水淡化装置示意图.
①水变成水蒸气的过程中,不发生变化的是_________ (填字母序号)
A、分子质量 B.分子种类 C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会________ (填“变大”、“变小”或“不变”)
(6)配制75g6%的氯化钠溶液时,涉及以下实验步骤:
A.称量及量取 B.计算 C.溶解 D.装瓶贴标签.
其正确的实验步骤是__________ (填字母),若用量筒量取水时俯视读数,其它操作正确,则所得溶液的质量分数____________ 6%(填“>”、“<”或“=”),小明用pH试纸检测所配溶液,得到氯化钠溶液的pH_________ 7(填“>”、“<”或“=”),氯化钠溶液能导电是因为含有自由移动的________ (填微粒符号),若将该氯化钠溶液全部稀释成浓度为0.9%的生理盐水,则需再加水________ g.
(7)如表是氯化钠和硝酸钾在不同温度下的溶解度,运用溶解度表与溶解度曲线回答下列问题:
①图3中能表示氯化钠的溶解度曲线是_________ (填“A”或“B”).
②60℃时,100g水中加入90g硝酸钾,充分溶解,所得溶液是__________ (填“饱和”或“不饱和”)溶液.将该溶液降温到10℃时,析出晶体的质量为__________ g.
③根据表格可知,氯化钠和硝酸钾两物质溶解度过相等的温度范围在_________ ℃之间.
④60℃时,用等质量的氯化钠、硝酸钾分别配制两种饱和溶液,测得其质量依次为m1g和m2g,则m1_____ m2.(填“>”、“<”或“=”)
⑤现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若某硝酸钾固体中含有少量氯化钠,则提纯硝酸钾的操作步骤是__________ (填序号).

(1)电解水实验揭示了水的组成,图1实验中得到氧气的试管是
(2)自来水厂净水过程中用到活性炭,其作用是
(3)消防队员常用高压水枪灭火,其灭火的原理是
(4)将下列物质分别加入水中,不能形成溶液的是
A.冰块 B.二氧化碳 C.食盐 D.酒精
(5)海水淡化可缓解淡水资源匮乏的问题,图2为太阳能海水淡化装置示意图.
①水变成水蒸气的过程中,不发生变化的是
A、分子质量 B.分子种类 C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会
(6)配制75g6%的氯化钠溶液时,涉及以下实验步骤:
A.称量及量取 B.计算 C.溶解 D.装瓶贴标签.
其正确的实验步骤是
(7)如表是氯化钠和硝酸钾在不同温度下的溶解度,运用溶解度表与溶解度曲线回答下列问题:
| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 |
②60℃时,100g水中加入90g硝酸钾,充分溶解,所得溶液是
③根据表格可知,氯化钠和硝酸钾两物质溶解度过相等的温度范围在
④60℃时,用等质量的氯化钠、硝酸钾分别配制两种饱和溶液,测得其质量依次为m1g和m2g,则m1
⑤现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若某硝酸钾固体中含有少量氯化钠,则提纯硝酸钾的操作步骤是
您最近一年使用:0次
【推荐2】硝酸钾固体的溶解度曲线如图所示。_____ (填“饱和”或“不饱和”)溶液。
(2)将40℃时的硝酸钾饱和溶液降温到20℃,所得溶液的溶质质量分数______ (填“变大”或“变小”)。
(3)现有60℃的硝酸钾饱和溶液42g,将其稀释至22%,需加入水的质量为______ g。

(2)将40℃时的硝酸钾饱和溶液降温到20℃,所得溶液的溶质质量分数
(3)现有60℃的硝酸钾饱和溶液42g,将其稀释至22%,需加入水的质量为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某化工厂为了综合利用生产过程中的副产品CaSO4 ,与相邻的化肥厂联合设计了以下制备(NH4)2SO4的工艺流程。在如图流程中,沉淀池里物质发生的主要化学反应为:
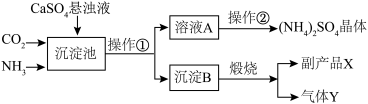
(1)沉淀B高温煅烧反应的化学方程式______ ,反应的基本类型:______ ,该工艺中可循环使用的物质为______ (填化学式)。
(2)实验室里操作①称为______ ,实验室进行此操作时,用到的玻璃仪器有玻璃棒、______ 、______ 。
(3)①同学们在实验室用硫酸铵晶体配制硫酸铵溶液,,除用到胶头滴管、量筒、烧杯外,还需要用到玻璃棒,玻璃棒的作用是______ 。
②实验室用200克40%的硫酸铵溶液加水稀释成10%的硫酸铵溶液。需要加水的质量为______ 克
(4)从绿色化学和资源综合利用的角度说明上述流程的主要优点是______ 。


(1)沉淀B高温煅烧反应的化学方程式
(2)实验室里操作①称为
(3)①同学们在实验室用硫酸铵晶体配制硫酸铵溶液,,除用到胶头滴管、量筒、烧杯外,还需要用到玻璃棒,玻璃棒的作用是
②实验室用200克40%的硫酸铵溶液加水稀释成10%的硫酸铵溶液。需要加水的质量为
(4)从绿色化学和资源综合利用的角度说明上述流程的主要优点是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】掌握化学实验中常用仪器的特征和用途,有利于开展化学学习和研究。
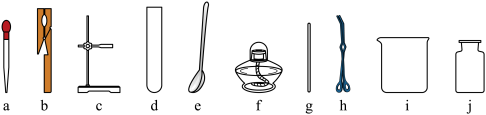
(1)写出下列仪器的名称:d______ ;f______ ;h______ ;e______ 。
(2)从上述常见仪器图示中,选择恰当的字母序号填空:
①可以用来夹持试管的仪器是______ ;
②用酒精灯加热时需要垫上陶土网的仪器是______ ;
③吸取和滴加少量液体试剂的仪器是______ ;
④加热少量水需要用______ ;
⑤口部或内壁经过了磨砂处理的仪器是______ 。
(3)某同学用量筒量取一定体积的液体。
①量液时,量筒必须放在水平桌面,当液体接近刻度时,应改用______ (填仪器名称)滴加。
②读数时,视线应与量筒内液体的______ 保持水平。
③用量筒量取溶液,俯视读数为15mL;倒出部分溶液后,平视读数为9mL。则该学生实际倒出的溶液体积______ (填“大于”或“小于”)6mL。

(1)写出下列仪器的名称:d
(2)从上述常见仪器图示中,选择恰当的字母序号填空:
①可以用来夹持试管的仪器是
②用酒精灯加热时需要垫上陶土网的仪器是
③吸取和滴加少量液体试剂的仪器是
④加热少量水需要用
⑤口部或内壁经过了磨砂处理的仪器是
(3)某同学用量筒量取一定体积的液体。
①量液时,量筒必须放在水平桌面,当液体接近刻度时,应改用
②读数时,视线应与量筒内液体的
③用量筒量取溶液,俯视读数为15mL;倒出部分溶液后,平视读数为9mL。则该学生实际倒出的溶液体积
您最近一年使用:0次
【推荐2】按要求回答问题
(1)二氧化硫由______ 构成;铁由______ 构成。
(2)______ 决定原子种类。
(3)量筒读数时,视线应:______ 。
(4)铁丝在空气中灼热发红,但不能燃烧,这一事实与下列哪一因素关系最密切______。
(5)给试管内的液体加热时,试管破裂的原因______ (填一条)。
(1)二氧化硫由
(2)
(3)量筒读数时,视线应:
(4)铁丝在空气中灼热发红,但不能燃烧,这一事实与下列哪一因素关系最密切______。
| A.铁丝的表面积 | B.氧气的浓度 |
| C.燃烧区的温度 | D.铁丝的粗细 |
您最近一年使用:0次