黄铜(铜、锌合金)是重要的金属材料,有优良的导热性和耐腐蚀性,可用作各种仪器零件。为了测定黄铜样品中铜的质量分数,某研究小组进行了如图实验,请计算:

(1)生成氢气的质量为______ g。
(2)黄铜样品中铜的质量分数。

(1)生成氢气的质量为
(2)黄铜样品中铜的质量分数。
更新时间:2022-03-09 14:41:22
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】为测定某纯碱样品(含少量杂质)中碳酸钠的含量。取12g样品放入烧杯中,加入100g氯化钙溶液恰好完全反应(杂质不参与反应)。过滤后,所得溶液质量为102g。试计算:
(1)生成碳酸钙的质量为____ g。
(2)纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)(已知: )
)
(1)生成碳酸钙的质量为
(2)纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)(已知:
 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】胆矾(CuCO4·5H2O,相对分子质量为250)广泛应用于生产生活中。(将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图。)

(1)加热至__________ ℃时,CuSO4开始分解。
(2)加热至1000℃时,CuO开始分解,生成Cu2O与一种能使带火星的木条复燃的气体,该气体为_______ 。CuO完全分解时产生该气体的质量为________ g。
(3)根据胆矾分解的化学方程式 ,计算“上图”中x的值
,计算“上图”中x的值_______ (写出计算过程)。
(4)下列物质均可作为炼铜的原料。理论上,冶炼等质量的下列物质得到铜最多的是_______(填字母序号)。

(1)加热至
(2)加热至1000℃时,CuO开始分解,生成Cu2O与一种能使带火星的木条复燃的气体,该气体为
(3)根据胆矾分解的化学方程式
 ,计算“上图”中x的值
,计算“上图”中x的值(4)下列物质均可作为炼铜的原料。理论上,冶炼等质量的下列物质得到铜最多的是_______(填字母序号)。
| A.CuSO4·5H2O | B.CuSO4 | C.CuO | D.Cu2O |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】超市出售的纯碱产品中往往含有少量的氯化钠,为测定某品牌纯碱样品中碳酸钠的质量分数,小明将60g稀盐酸分三次加到盛有12g纯碱样品的烧杯中,实验数据记录如表。请计算:
(1)共生成二氧化碳_______ g。
(2)纯碱样品中碳酸钠的质量分数。(结果保留到小数点后一位)
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸质量/g | 20 | 20 | 20 |
| 烧杯中物质总质量/g | 29.8 | 47.6 | 67.6 |
(1)共生成二氧化碳
(2)纯碱样品中碳酸钠的质量分数。(结果保留到小数点后一位)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。(铁和硫酸反应方程式为: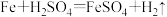 )请根据关系图分析并计算:
)请根据关系图分析并计算:

(1)铁粉全部反应完时,产生氢气的质量为______ g。
(2)求参加反应的稀硫酸中溶质的质量(写出计算过程)。
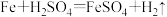 )请根据关系图分析并计算:
)请根据关系图分析并计算:
(1)铁粉全部反应完时,产生氢气的质量为
(2)求参加反应的稀硫酸中溶质的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐3】小卫同学生活在农村,家里使用的是井水,烧开水的炊壶有一层很厚的水垢。查阅资料后得知:水垢的主要成分是CaCO3和Mg(OH)2,他为了弄清水垢中碳酸钙的质量分数,取经干燥后的水垢样品带到实验室用稀盐酸与其反应并进行分析。
(1)实验室的稀盐酸是用质量分数为38%的浓盐酸配制的,配制1000g质量分数为10%的稀盐酸需要该浓盐酸的质量为________ g(保留一位小数)。
(2)小卫取10g水垢样品,与足量稀盐酸充分反应后,得到3.3g二氧化碳。该水垢中碳酸钙的质量分数为多少?
(1)实验室的稀盐酸是用质量分数为38%的浓盐酸配制的,配制1000g质量分数为10%的稀盐酸需要该浓盐酸的质量为
(2)小卫取10g水垢样品,与足量稀盐酸充分反应后,得到3.3g二氧化碳。该水垢中碳酸钙的质量分数为多少?
您最近一年使用:0次



