某研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:

【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】如图1是他们进行实验的装置图,
①此实验中B处宜采用的气体收集方法是______ 。
②有同学认为也可以用如图2装置。当向里推活塞时,如果装置气密性良好,可能观察到现象是______ 。
【实验记录】
【结论】根据上述实验探究过程得出的结论是______ 。
【反思】H2O2在加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在该反应前后的______ 和______ 是否改变。
【拓展应用】已知所有化学反应遵循如下规律:参加化学反应前各物质的质量总和等于反应后各生成物的质量总和。如果实验室用一定质量分数的过氧化氢溶液50.0克和2.0克二氧化锰混合反应,完全反应后称得剩余物的总质量为48.8克,试求反应中放出氧气的质量为______ 克。

【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】如图1是他们进行实验的装置图,
①此实验中B处宜采用的气体收集方法是
②有同学认为也可以用如图2装置。当向里推活塞时,如果装置气密性良好,可能观察到现象是
【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2 | 5%H2O2 |
| 催化剂 | 1gMnO2 | |
| 时间 | 165秒 | 46秒 |
【反思】H2O2在加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在该反应前后的
【拓展应用】已知所有化学反应遵循如下规律:参加化学反应前各物质的质量总和等于反应后各生成物的质量总和。如果实验室用一定质量分数的过氧化氢溶液50.0克和2.0克二氧化锰混合反应,完全反应后称得剩余物的总质量为48.8克,试求反应中放出氧气的质量为
更新时间:2022-03-15 22:56:52
|
相似题推荐
科学探究题
|
较易
(0.85)
解题方法
【推荐1】走进实验室,寻找新的催化剂
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
【实验结论】红砖粉末能作为过氧化氢溶液分解的催化剂。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
| 实验步骤 | 实验现象 | 实验结论及解释 | |
| Ⅰ | 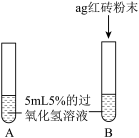 | A中无明显现象;B中产生大量能使带火星木条 | 红磷粉末能改变过氧化氢分解速率 |
| Ⅱ | 向B试管中重新加入5%的过氧化氢溶液,反应停止后,过滤分离出红砖粉,洗涤、干燥、称量 | B试管又产生大量能使带火星的木条复燃的气体,滤渣的质量等于 | 红砖粉末的 |
| Ⅲ | 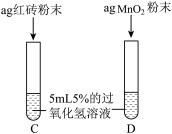 | 两支试管中均产生气泡且 | 红砖粉末的催化剂效果没有二氧化锰粉末好 |
您最近一年使用:0次
【推荐2】某化学兴趣小组的同学知道二氧化锰能作过氧化氢分解的催化剂后,想再探究四氧化三铁是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程。
【查阅资料】四氧化三铁能和稀硫酸反应,产生黄色溶液。
【提出问题】四氧化三铁能不能作过氧化氢分解的催化剂呢?
【猜想假设】猜想Ⅰ:四氧化三铁能作过氧化氢分解的催化剂。
猜想Ⅱ:_______
【实验过程】
【得出结论】实验三、四证明:四氧化三铁的______________ 在反应前后均没有发生任何变化,可以作为过氧化氢分解的催化剂。猜想_____________ 正确。
【反思评价】写出四氧化三铁催化过氧化氢分解的文字表达式:_______ 。
【查阅资料】四氧化三铁能和稀硫酸反应,产生黄色溶液。
【提出问题】四氧化三铁能不能作过氧化氢分解的催化剂呢?
【猜想假设】猜想Ⅰ:四氧化三铁能作过氧化氢分解的催化剂。
猜想Ⅱ:
【实验过程】
| 实验编号 | 实验操作 | 实验现象 |
| 实验一 | 在试管中加入过氧化氢溶液,然后将带火星的木条伸入试管中 | 有少量气泡,木条不复燃 |
| 实验二 | 在装有过氧化氢的试管中加入1g四氧化三铁,然后将带火星的木条伸入试管中 | 产生大量气泡,木条复燃 |
| 实验三 | 待2中反应结束,将试管内的剩余物进行过滤、洗涤、干燥、称量 | 称得固体质量为1g |
| 实验四 | 将实验三中所得固体放入试管中,滴入足量的稀硫酸,充分振荡 |
【得出结论】实验三、四证明:四氧化三铁的
【反思评价】写出四氧化三铁催化过氧化氢分解的文字表达式:
您最近一年使用:0次
科学探究题
|
较易
(0.85)
【推荐3】下表是某化学兴趣小组探究影响化学反应速率的因素的实验数据。
(1)通过实验①和②对比可知,化学反应速率与___ 有关;
(2)从实验___ 和___ 对比可知,化学反应速率与温度的关系是:___ ;
(3)该实验可得出的结论是___ ;
(4)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应的速率与微观粒子的碰撞概率有关。 从微观角度来看,“反应物浓度越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积内粒子 数越___ ,粒子间碰撞的概率越大,化学反应速率越快。
实验序号 | H2O2溶液浓度% | H2O2溶液浓度/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
④ | 30 | 5 | 35 | 0 | 2 | 10.76 |
(2)从实验
(3)该实验可得出的结论是
(4)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应的速率与微观粒子的碰撞概率有关。 从微观角度来看,“反应物浓度越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积内粒子 数越
您最近一年使用:0次
科学探究题
|
较易
(0.85)
名校
解题方法
【推荐1】Fenton法常用于处理含难降解有机物的工业废水。其原理是利用Fe2+和H2O2的反应产生能降解污染物的活性成分。现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响。
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。

实验测得p-CP的浓度随时间变化的关系如图。
(2)实验发现,温度过高时,降解反应较难发生。请从Fenton法所用试剂的角度分析原因:__________ 。
(3)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:____________________ 。
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。
| 实验编号 | 实验目的 | 温度/℃ | pH | 浓度/(mg·L-1) | |
| H2O2 | Fe2+ | ||||
| ① | 为②③提供参照 | 25 | 3 | 204 | 16.8 |
| ② | 探究温度对降解反应速率的影响 | 204 | 16.8 | ||
| ③ | 25 | 10 | 204 | 16.8 | |

实验测得p-CP的浓度随时间变化的关系如图。
(2)实验发现,温度过高时,降解反应较难发生。请从Fenton法所用试剂的角度分析原因:
(3)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】学习了“过氧化氢制氧气使用二氧化锰作催化剂”,化学社团在“寻找新的催化剂”的活动中,对“硫酸铜能否作过氧化氢分解的催化剂”进行了以下探究。
(1)【实验探究】甲同学按如下方案进行实验。
(2)【评价改进】大家认为甲同学的实验结论不严谨。若要确定该实验结论正确,还需证明硫酸铜的___ 在反应前后都没有发生改变。
(3)【讨论交流】大家认为:在甲同学实验的基础上,乙同学将甲同学实验时试管中的溶液蒸发、干燥得到白色固体,再称其质量为_______ g,然后将固体加入5%的过氧化氢溶液中,仍然可以加速过氧化氢分解。由此可以得出甲同学的实验结论。
(4)【拓展延伸】比较硫酸铜和二氧化锰对过氧化氢制氧气的催化效果,实验过程中不需要控制的条件是_______ (填序号)。
A.溶液的起始温度 B.催化剂的质量 C.溶液的浓度 D.过氧化氢完全分解的时间
(1)【实验探究】甲同学按如下方案进行实验。
| 实验步骤 | 实验现象 | 实验结论 |
 | 步骤①木条不复燃; 步骤②产生气泡,溶液变蓝色; 步骤③ | 硫酸铜能作过氧化氢分解的催化剂,反应的化学方程式为 |
(3)【讨论交流】大家认为:在甲同学实验的基础上,乙同学将甲同学实验时试管中的溶液蒸发、干燥得到白色固体,再称其质量为
(4)【拓展延伸】比较硫酸铜和二氧化锰对过氧化氢制氧气的催化效果,实验过程中不需要控制的条件是
A.溶液的起始温度 B.催化剂的质量 C.溶液的浓度 D.过氧化氢完全分解的时间
您最近一年使用:0次
【推荐3】小明将家中清洗伤口用的消毒液 “双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验。
【第一组实验】检验该双氧水是否失效。
(1)实验过程
①在试管中加入5mL 的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③用如图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是______ ;
(2)实验结论:______ 。

【第二组实验探究】:氧化铜(CuO)能否催化“双氧水”分解
[猜想]Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后______ 和______ 不变。
[实验]用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验:

(3)完成下表:
(4)步骤⑦的目的______ 。
(5)过氧化氢能被CuO催化分解放出O2的符号表达式为:______ 。
【第一组实验】检验该双氧水是否失效。
(1)实验过程
①在试管中加入5mL 的“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③用如图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是
(2)实验结论:

【第二组实验探究】:氧化铜(CuO)能否催化“双氧水”分解
[猜想]Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后
[实验]用天平称量0.2gCuO,取5mL的过氧化氢溶液于试管中,进行如下实验:

(3)完成下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中 | 所得固体质量为 | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立。 |
(4)步骤⑦的目的
(5)过氧化氢能被CuO催化分解放出O2的符号表达式为:
您最近一年使用:0次



