氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性。实验室里加热氯化铵(NH4CI)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水。
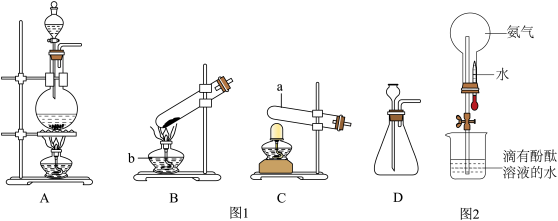
(1)如图1装置是实验室制取气体的一些发生装置,a仪器名称___________ 。实验室用D装置制取二氧化碳,其反应的原理为(用化学方程式表示)___________ ,制取氨气的发生装置___________ (填序号),收集一瓶氨气的方法是___________ 。___________ 色的喷泉。
(3)当喷泉实验结束后,测烧瓶内溶液的pH。步骤如下:
步骤一:用镊子撕一小段pH试纸,放到干净的玻璃片上:
步骤二:用蒸馏水润湿pH试纸;
步骤三:用玻璃棒蘸取待测液滴到pH试纸上;
步骤四:把试纸显示的颜色与比色卡对比,读取pH。
该实验步骤___________ 错误,造成的后果是使测定结果___________ (填“偏小”“偏大”或“无影响”)。
(1)如图1装置是实验室制取气体的一些发生装置,a仪器名称
(3)当喷泉实验结束后,测烧瓶内溶液的pH。步骤如下:
步骤一:用镊子撕一小段pH试纸,放到干净的玻璃片上:
步骤二:用蒸馏水润湿pH试纸;
步骤三:用玻璃棒蘸取待测液滴到pH试纸上;
步骤四:把试纸显示的颜色与比色卡对比,读取pH。
该实验步骤
更新时间:2022-03-28 22:34:48
|
相似题推荐
实验题
|
适中
(0.65)
【推荐1】根据下列装置图回答问题:
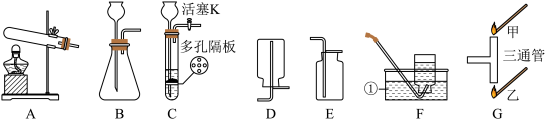
(1)写出标号①仪器的名称:①___________ 。
(2)实验室制取CO2的反应方程式为___________ ,常选用___________ (填装置序号)收集CO2。小明用装置C制取CO2,C作为发生装置的优点___________ 连接装置C、G(竖直放置),当试管中发生反应一段时间后观察到___________ (填“甲”或“乙”)处燃着的火柴先熄灭;若要停止产生CO2,进行的操作是___________ 。
(3)如图是以H2O2溶液为原料制备O2的改进装置,用铂丝(可上下抽动)作催化剂,安全管下端浸没于H2O2溶液中,完成相应的探究实验。将铂丝插入溶液,立即产生O2。

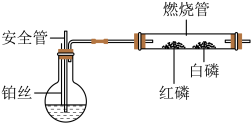
①若烧瓶内压强过大,安全管中出现的现象是_______ 。写出圆底烧瓶中的化学方程式_______ 。
②均匀微热燃烧管,观察白磷燃烧而红磷不燃烧,白磷燃烧的现象是_______ 。小明认为该装置有个不足______ 。

(1)写出标号①仪器的名称:①
(2)实验室制取CO2的反应方程式为
(3)如图是以H2O2溶液为原料制备O2的改进装置,用铂丝(可上下抽动)作催化剂,安全管下端浸没于H2O2溶液中,完成相应的探究实验。将铂丝插入溶液,立即产生O2。


①若烧瓶内压强过大,安全管中出现的现象是
②均匀微热燃烧管,观察白磷燃烧而红磷不燃烧,白磷燃烧的现象是
您最近一年使用:0次
【推荐2】实验是化学学习的必要途径,请根据图1和图2回答下列问题:

(1)请写出编号①的仪器名称:________ 。
(2)小东想要用碳酸钠粉末和稀盐酸制取一瓶二氧化碳,你建议他最好使用的制取装置组合_____ (请在装置A-F中选择),发生反应的化学方程式为_________ 。
(3)图2是小燕配制100g13.5%氯化钠溶液的操作示意图,其中有一个装置存在错误,该装置的字母编号是________ ,改正操作后,用图2所示的字母编号来表示配制溶液的正确操作顺序是:________ 。
(4)小燕所得溶液的溶质质量分数小于13.5%,可能的原因是______ (填序号)。
①氯化钠固体不纯;②用生锈的砝码称量;③装瓶时有少量液体洒出;④用量筒量取水时,仰视读数;⑤所用烧杯不干燥

(1)请写出编号①的仪器名称:
(2)小东想要用碳酸钠粉末和稀盐酸制取一瓶二氧化碳,你建议他最好使用的制取装置组合
(3)图2是小燕配制100g13.5%氯化钠溶液的操作示意图,其中有一个装置存在错误,该装置的字母编号是
(4)小燕所得溶液的溶质质量分数小于13.5%,可能的原因是
①氯化钠固体不纯;②用生锈的砝码称量;③装瓶时有少量液体洒出;④用量筒量取水时,仰视读数;⑤所用烧杯不干燥
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】结合如图回答问题。
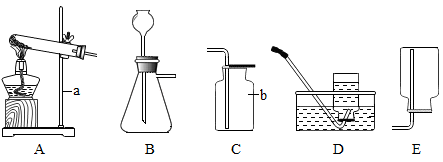
(1)仪器名称:a______ 。
(2)氯酸钾和二氧化锰制氧气,可选装置______ (填序号)和D组合,反应的化学方程式为______ ,收集完气体后,应先______ 避免水槽内的水倒吸使试管受热不均而炸裂。
(3)用如图装置制取CO2并验证相关性质。
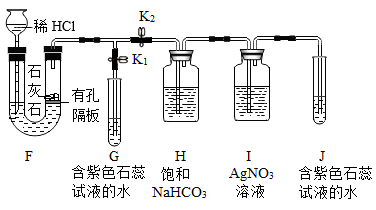
①上述实验中,能验证二氧化碳的性质有______ (填序号)。
A.二氧化碳密度比空气大 B.二氧化碳能溶于水
C.二氧化碳能与水反应生成一种酸 D.二氧化碳能与澄清石灰水反应
②生成的CO2气体中常混有HCl,原因是盐酸具有______ 性。
③CO2气体中常混有HCl常用饱和碳酸氢钠溶液除去,那装置I的作用是______ 。

(1)仪器名称:a
(2)氯酸钾和二氧化锰制氧气,可选装置
(3)用如图装置制取CO2并验证相关性质。

①上述实验中,能验证二氧化碳的性质有
A.二氧化碳密度比空气大 B.二氧化碳能溶于水
C.二氧化碳能与水反应生成一种酸 D.二氧化碳能与澄清石灰水反应
②生成的CO2气体中常混有HCl,原因是盐酸具有
③CO2气体中常混有HCl常用饱和碳酸氢钠溶液除去,那装置I的作用是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】已知:钠在常温下与水剧烈反应生成氢气和氢氧化钠。小明结合已有知识设计如图装置进行验证,操作如下:
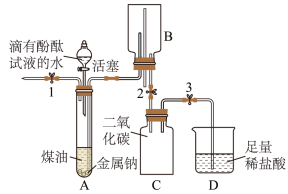
步骤一:打开止水夹1及分液漏斗活塞,待液体充满大试管后,关闭止水夹1及分液漏斗活塞观察到液体分层,钠熔成银白色小球,……
步骤二:打开止水夹2,待B中部分溶液进入C中,迅速关闭止水夹2。
步骤三:打开止水夹3,D中溶液进入C中,刚开始没有气泡产生,过一会儿产生气泡,溶液红色消失。
步骤四:将燃着的木条伸到导管尖嘴处,打开止水夹1,气体燃烧,产生淡蓝色火焰。
分析:
(1)补充完整步骤一的实验现象;_____
(2)写出步骤三中装置C里发生的化学反应方程式;_____
(3)设计实验探究:步骤三反应结束后,C中溶液的溶质成分(酚酞除外),写出实验操作、现象和结论。_____

步骤一:打开止水夹1及分液漏斗活塞,待液体充满大试管后,关闭止水夹1及分液漏斗活塞观察到液体分层,钠熔成银白色小球,……
步骤二:打开止水夹2,待B中部分溶液进入C中,迅速关闭止水夹2。
步骤三:打开止水夹3,D中溶液进入C中,刚开始没有气泡产生,过一会儿产生气泡,溶液红色消失。
步骤四:将燃着的木条伸到导管尖嘴处,打开止水夹1,气体燃烧,产生淡蓝色火焰。
分析:
(1)补充完整步骤一的实验现象;
(2)写出步骤三中装置C里发生的化学反应方程式;
(3)设计实验探究:步骤三反应结束后,C中溶液的溶质成分(酚酞除外),写出实验操作、现象和结论。
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】某校同学开展了如图所示的“溶液酸碱性的检验”的实验活动.
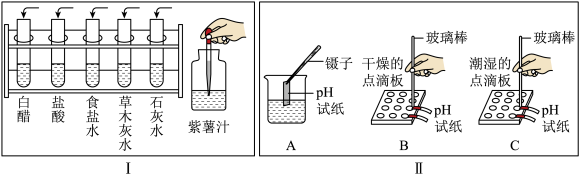
(1)把自制的紫色紫薯汁按图 所示分别滴加到试管中,观察到的现象如下表所示:
所示分别滴加到试管中,观察到的现象如下表所示:
①图 中存放紫薯汁的仪器名称为
中存放紫薯汁的仪器名称为________ .
②根据上表推测,紫薯汁能作酸碱指示剂,遇到稀硫酸可能显示的颜色是________ .
(2)用pH试纸测定图 中部分溶液的酸碱度:草木灰水
中部分溶液的酸碱度:草木灰水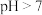 ,属于
,属于________  填“酸性”“中性”或“碱性”
填“酸性”“中性”或“碱性” 溶液;白醋pH
溶液;白醋pH________  填“
填“ ”“
”“ ”或“
”或“ ”
”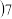 .
.
(3)图 是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是
是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是________  填“A”“B”或“C”,下同
填“A”“B”或“C”,下同 ,可能导致所测溶液pH发生改变的错误操作是
,可能导致所测溶液pH发生改变的错误操作是________ ,如果测定的是石灰水,测得的pH将________  填“偏大”“不变”或“偏小”
填“偏大”“不变”或“偏小” 简述正确测定溶液PH的操作步骤:
简述正确测定溶液PH的操作步骤:________ .

(1)把自制的紫色紫薯汁按图
 所示分别滴加到试管中,观察到的现象如下表所示:
所示分别滴加到试管中,观察到的现象如下表所示:| 溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
| 加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
 中存放紫薯汁的仪器名称为
中存放紫薯汁的仪器名称为②根据上表推测,紫薯汁能作酸碱指示剂,遇到稀硫酸可能显示的颜色是
(2)用pH试纸测定图
 中部分溶液的酸碱度:草木灰水
中部分溶液的酸碱度:草木灰水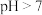 ,属于
,属于 填“酸性”“中性”或“碱性”
填“酸性”“中性”或“碱性” 溶液;白醋pH
溶液;白醋pH 填“
填“ ”“
”“ ”或“
”或“ ”
”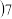 .
.(3)图
 是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是
是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 填“A”“B”或“C”,下同
填“A”“B”或“C”,下同 ,可能导致所测溶液pH发生改变的错误操作是
,可能导致所测溶液pH发生改变的错误操作是 填“偏大”“不变”或“偏小”
填“偏大”“不变”或“偏小” 简述正确测定溶液PH的操作步骤:
简述正确测定溶液PH的操作步骤:
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】实验是学习化学的重要方法。
【实验一】“吹气球实验”(如图)
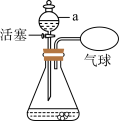
(1)打开活塞,通过仪器a向锥形瓶中加水,观察到气球胀大;关闭活塞,一段时间内气球大小没有变化,说明该装置气密性___________ 。
(2)若生成氧气使气球胀大,则反应的化学方程式为___________ 。
(3)若锥形瓶中装有氢氧化钠固体,通过仪器a加少量水,气球也能胀大,主要原因是___________ 。
【实验二】探究酸和碱的性质
(4)电解水时常加入NaOH增强水的导电性,是由于NaOH在水中能解离出___________ (写粒子符号)。
(5)下图为稀硫酸与氢氧化钠溶液反应过程中溶液pH随加入液体体积变化曲线。
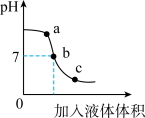
①测定溶液pH的方法是:用玻璃棒蘸取溶液,滴到pH试纸上,把试纸显示的颜色与___________ 对照,读取pH。图中a点对应的溶液呈___________ 性,若向溶液中加入___________ ,溶液变为红色,也能得出此结论。
②曲线上的b点说明两溶液恰好完全反应,反应的化学方程式为___________ 。
【实验一】“吹气球实验”(如图)

(1)打开活塞,通过仪器a向锥形瓶中加水,观察到气球胀大;关闭活塞,一段时间内气球大小没有变化,说明该装置气密性
(2)若生成氧气使气球胀大,则反应的化学方程式为
(3)若锥形瓶中装有氢氧化钠固体,通过仪器a加少量水,气球也能胀大,主要原因是
【实验二】探究酸和碱的性质
(4)电解水时常加入NaOH增强水的导电性,是由于NaOH在水中能解离出
(5)下图为稀硫酸与氢氧化钠溶液反应过程中溶液pH随加入液体体积变化曲线。

①测定溶液pH的方法是:用玻璃棒蘸取溶液,滴到pH试纸上,把试纸显示的颜色与
②曲线上的b点说明两溶液恰好完全反应,反应的化学方程式为
您最近一年使用:0次
实验题
|
适中
(0.65)
真题
解题方法
【推荐2】化学小组同学为鉴定某工厂排出的无色污水成分,他们查阅工厂的有关资料后,推测出污水中可能含有HCl、Na2SO4、NaOH、Na2CO3中的一种或几种物质,同学们取污水进行了探究:(已知Na2SO4溶液呈中性)
(1)测污水的pH:取一张pH试纸,放在玻璃片上________________________ ,读数为pH=2,由此可知:污水中一定有_____________ ,可能有Na2SO4。
(2)检验Na2SO4是否存在:甲同学在一支试管中取少量污水,向试管中滴加少量的_______________ 溶液,振荡,产生了白色沉淀,反应的化学方程式为____________________ ,证明污水中有Na2SO4存在。乙同学用物理方法也得到了同样的结论,他的实验操作及实验现象是_____________________________ 。
通过探究,同学们确定了污水的成分。
为使排放的污水中不含酸,可向污水中加过量的________________________ 。
(1)测污水的pH:取一张pH试纸,放在玻璃片上
(2)检验Na2SO4是否存在:甲同学在一支试管中取少量污水,向试管中滴加少量的
通过探究,同学们确定了污水的成分。
为使排放的污水中不含酸,可向污水中加过量的
您最近一年使用:0次





