碳酸锂(Li2CO3)是制备锂电池的重要原料。工业上以锂辉石精矿(主要成分为Li2O)为原料制取碳酸锂的主要工艺流程及碳酸锂的溶解度表如下:
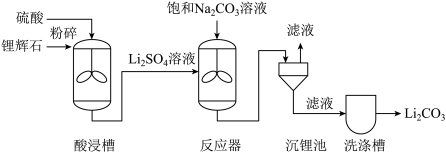
请回答下列问题:
(1)将锂辉石粉碎的目的是_______________ 。
(2)沉锂池中,分离固体和液体的操作是____ ,所需的玻璃仪器有____ 、烧杯、玻璃棒。
(3)酸浸槽中,发生反应的化学方程式为____ 。结合碳酸锂的溶解度表,洗涤槽中应用_____ (填“冷水”或“热水”)洗涤。

| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 碳酸锂的溶解度/g | 1.55 | 1.33 | 1.18 | 1.00 | 0.82 |
(1)将锂辉石粉碎的目的是
(2)沉锂池中,分离固体和液体的操作是
(3)酸浸槽中,发生反应的化学方程式为
更新时间:2022-04-09 11:37:40
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】t2℃时,将甲、乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一所示,甲和乙的溶解度曲线如图二、请结合图示回答下列问题:
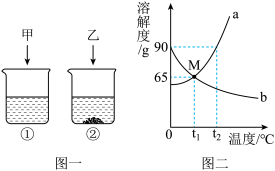
(1)固体甲对应的溶解度曲线是___________ (选填“a”或“b”);
(2)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出,你认为“全部溶解”的原因是___________ ;
(3)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是___________ (填字母)。
a、甲溶液仍为饱和溶液 b、两溶液质量:甲<乙
c、两溶液中溶剂质量:甲=乙 d、两溶液溶质质量分数:甲>乙

(1)固体甲对应的溶解度曲线是
(2)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出,你认为“全部溶解”的原因是
(3)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是
a、甲溶液仍为饱和溶液 b、两溶液质量:甲<乙
c、两溶液中溶剂质量:甲=乙 d、两溶液溶质质量分数:甲>乙
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下列是KNO3和NaCl在不同温度时的溶解度表及溶解度曲线。

(1)上图中表示NaCl溶解度曲线的是___ (填“A”或“B”)。
(2)20℃时,向盛有40gNaCl的烧杯中加入100g水,搅拌,充分溶解后,溶液的溶质质量分数为___ (只列出计算表达式)。
(3)30℃时,向各盛有100g水的两个烧杯中,分别加入50g 和50g NaCl,所得
和50g NaCl,所得 溶液的质量
溶液的质量___ (填“>”、“<”或“=”)NaCl溶液的质量。
(4)由表中数据分析可知,在某一温度时NaCl和 具有相同的溶解度mg,则m的取值范围是
具有相同的溶解度mg,则m的取值范围是___ 。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |

(1)上图中表示NaCl溶解度曲线的是
(2)20℃时,向盛有40gNaCl的烧杯中加入100g水,搅拌,充分溶解后,溶液的溶质质量分数为
(3)30℃时,向各盛有100g水的两个烧杯中,分别加入50g
 和50g NaCl,所得
和50g NaCl,所得 溶液的质量
溶液的质量(4)由表中数据分析可知,在某一温度时NaCl和
 具有相同的溶解度mg,则m的取值范围是
具有相同的溶解度mg,则m的取值范围是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐3】硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
(1)60℃时硝酸钾的溶解度是_____ g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是_____ 。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
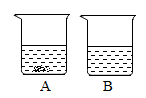
①烧杯A中溶解的物质是_____ 。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数_____ (填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量_____ (填“一定”或“不一定”)相等。
| 温度/℃ | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | 硝酸钾 | 31.6 | 63.9 | 110 | 169 | 246 |
| 氯化钠 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(1)60℃时硝酸钾的溶解度是
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。

①烧杯A中溶解的物质是
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】某同学发现物质之间的转化有规律可循,画出了如图所示思维导图,其中A~E是初中化学常见的五种物质。物质A和B属于同种类别,B、C、D、E分别属于四种不同类别的化合物,B常用于灭火,D是大理石的主要成分。则物质A的化学式为_________ ;A和B反应的基本反应类型为_______ ;C→D反应的化学方程式为________ ;D和E反应的化学方程式为________ 。


您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某无色水溶液中可能含有以下离子中的几种:H+、Mg2+、Cu2+、 、
、 为确定其成分,进行如下实验:
为确定其成分,进行如下实验:
①经测定,溶液 pH=1;
②取未知溶液适量,加入过量的NaOH溶液,有白色沉淀产生,过滤;
③取②的部分滤液,加入适量的BaCl2溶液,有白色沉淀生成。
分析上述实验,回答下列问题:
(1)原溶液中一定含有的离子是:_____ ;一定不含 的原因是
的原因是_____ 。
(2)步骤②中发生的复分解反应共有_____ 种。
(3)步骤③中产生白色沉淀的化学方程式:_____ 。
 、
、 为确定其成分,进行如下实验:
为确定其成分,进行如下实验:①经测定,溶液 pH=1;
②取未知溶液适量,加入过量的NaOH溶液,有白色沉淀产生,过滤;
③取②的部分滤液,加入适量的BaCl2溶液,有白色沉淀生成。
分析上述实验,回答下列问题:
(1)原溶液中一定含有的离子是:
 的原因是
的原因是(2)步骤②中发生的复分解反应共有
(3)步骤③中产生白色沉淀的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】无水氯化钙在工业上有广泛的用途。以石灰石矿粉(主要成分为 ,含有
,含有 杂质)为原料,生产无水氯化钙的流程如下:
杂质)为原料,生产无水氯化钙的流程如下:
___________ (选填“能”或“不能”)和盐酸反应。
(2)石灰石矿粉中的杂质氧化铁与盐酸反应的化学方程式为___________ 。
(3)滤渣3中除有少量 外,还含有的物质是
外,还含有的物质是___________ (填化学式)。
(4)中性滤液蒸发得到产品的过程中需要用玻璃棒不断搅拌的目的是___________ 。
 ,含有
,含有 杂质)为原料,生产无水氯化钙的流程如下:
杂质)为原料,生产无水氯化钙的流程如下:

(2)石灰石矿粉中的杂质氧化铁与盐酸反应的化学方程式为
(3)滤渣3中除有少量
 外,还含有的物质是
外,还含有的物质是(4)中性滤液蒸发得到产品的过程中需要用玻璃棒不断搅拌的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】民用客机 是中国首款完全自主知识产权飞机,中后机身由江西制造,整机钛合金应用比例达
是中国首款完全自主知识产权飞机,中后机身由江西制造,整机钛合金应用比例达 。工业上利用钛铁矿[主要成分为钛酸亚铁(
。工业上利用钛铁矿[主要成分为钛酸亚铁( )]制备金属钛的工业流程如下图。
)]制备金属钛的工业流程如下图。
(1)操作1的名称为______ 。
(2)流程中“熔融氧化”发生反应的化学方程式为______ 。
(3)流程中氯化镁熔融电解反应的基本类型为______ 。
(4)流程中能循环利用的物质为______ 和______ 。
 是中国首款完全自主知识产权飞机,中后机身由江西制造,整机钛合金应用比例达
是中国首款完全自主知识产权飞机,中后机身由江西制造,整机钛合金应用比例达 。工业上利用钛铁矿[主要成分为钛酸亚铁(
。工业上利用钛铁矿[主要成分为钛酸亚铁( )]制备金属钛的工业流程如下图。
)]制备金属钛的工业流程如下图。
(1)操作1的名称为
(2)流程中“熔融氧化”发生反应的化学方程式为
(3)流程中氯化镁熔融电解反应的基本类型为
(4)流程中能循环利用的物质为
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐2】下图是初中化学实验的几种常用仪器,请按要求填空。
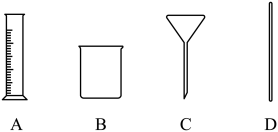
(1)在读取A中液体体积时,视线应与____________ 保持水平;
(2)进行过滤操作,除铁架台,C和D外,还需要用到上述仪器中的________ (填序号),仪器D在过滤操作中的用途是 ____________ 。

(1)在读取A中液体体积时,视线应与
(2)进行过滤操作,除铁架台,C和D外,还需要用到上述仪器中的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海南在我国海洋强国战略中具有特殊地位,肩负重要职责。利用海洋资源是海洋科技创新的新引擎。


(1)盐化工是我国重要海洋产业,盐卤中主要盐类物质及其含量如图甲,利用盐卤生产金属镁的流程如图乙,由图甲可知,盐卤中含量最多的盐是_______ ,该物质由______ 构成(填“分子”、“原子”或“离子”);
(2)流程图中操作A的名称是_______ ;若生产过程中镁元素没有损失,且其他盐类中的镁元素质量可略不计,则1000g盐卤可制备金属镁_____ g。


(1)盐化工是我国重要海洋产业,盐卤中主要盐类物质及其含量如图甲,利用盐卤生产金属镁的流程如图乙,由图甲可知,盐卤中含量最多的盐是
(2)流程图中操作A的名称是
您最近一年使用:0次



