生活在盐湖地区的人们“冬天捞碱,夏天晒盐”,所得纯碱中含少量食盐。为测定某纯碱样品中碳酸钠的质量分数,进行如下图所示操作。
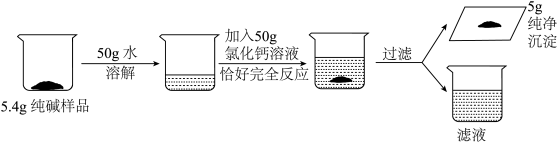
(1)由质量守恒定律可知,所得滤液质量是____________ g。
(2)计算纯碱样品中碳酸钠的质量分数_____ (写出计算过程,结果保留到0.1%)。

(1)由质量守恒定律可知,所得滤液质量是
(2)计算纯碱样品中碳酸钠的质量分数
2022·陕西西安·三模 查看更多[2]
更新时间:2022-04-12 18:12:43
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定实验室某瓶盐酸的溶质质量分数是否与标签相符,小雷取大理石样品于烧杯中,向其中加入盐酸,数据记录如表。(大理石中的杂质不参加反应)

请分析计算:
(1)反应生成CO2的质量为______ g;
(2)判断该瓶盐酸的溶质质量分数是否与标签相符?(结果精确到0.1%)

反应前烧杯内物质的质量/ g | 恰好完全反应后烧杯内物质的总质量/g | |
盐酸样品 | 大理石 | 113.6 |
106.0 | 12.0 | |
(1)反应生成CO2的质量为
(2)判断该瓶盐酸的溶质质量分数是否与标签相符?(结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】小明用如图1所示装置进行实验,他将碳粉和过量氧化铜混合充分加热,试管中固体总质量与加热时间的变化关系如图2所示。
(1)该反应中氧化铜发生了___________ (填“氧化”或“还原”)反应。
(2)根据化学方程式计算实验前混合物中碳粉的质量________ (结果精确到0.1g)。

(1)该反应中氧化铜发生了
(2)根据化学方程式计算实验前混合物中碳粉的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】化学兴趣小组欲测出某黄铜(含 Cu、Zn)中铜的质量分数。实验室现有98%的浓硫酸和10%的稀盐酸。

(1)若用10%的盐酸溶液制取 H2,则制得的H2可能混有水蒸气和_______ 等杂质。
(2)配制100g9.8%的硫酸溶液 ,需______ g98%的浓硫酸。
(3)现取10g 黄铜样品与足量的9.8%的硫酸溶液充分反应,产生氢气的质量如图所示,计算黄铜样品中铜的质量分数(写出计算过程) 。
(4)下列因素会使计算出的铜的质量分数结果偏大的是______。

(1)若用10%的盐酸溶液制取 H2,则制得的H2可能混有水蒸气和
(2)配制100g9.8%的硫酸溶液 ,需
(3)现取10g 黄铜样品与足量的9.8%的硫酸溶液充分反应,产生氢气的质量如图所示,计算黄铜样品中铜的质量分数(写出计算过程) 。
(4)下列因素会使计算出的铜的质量分数结果偏大的是______。
| A.氢气中混有水蒸气 | B.装置漏气 |
| C.加入的酸过量 | |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】加热14.8g氯酸钾和二氧化锰的混合物制取氧气,至完全反应后称量试管中固体的质量为10.0g。
(1)生成氧气的质量为______ g。
(2)计算完全反应后固体中二氧化锰的质量分数______ 。(写出计算过程)
(1)生成氧气的质量为
(2)计算完全反应后固体中二氧化锰的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某研究性学习小组为了测定黄铜(铜、锌合金)的组成。在化学老师的帮助下,选用98%的浓硫酸、黄铜样品进行下列实验和计算。
实验Ⅰ:配制150g9.8%的稀硫酸。
(1)计算:需要浓硫酸的质量___________g,约8.2mL;需要水的体积为__________mL。
(2)量取浓硫酸和水:量取液体时要准确量取。如果量取98%的浓硫酸时俯视读数,会导致所配溶液溶质质量分数_________9.8%。(填“大于”、“小于”或“等于”)。
(3)稀释
(4)装瓶贴标签:请填写下面的标签。_________

实验Ⅱ:测定黄铜样品中铜的质量分数。称取黄铜样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。试计算:

(5)产生氢气的质量为___________g;
(6)样品中铜的质量分数_______;
(7)反应后所得溶液中溶质的质量分数_______(计算结果精确到0.1%)。
实验Ⅰ:配制150g9.8%的稀硫酸。
(1)计算:需要浓硫酸的质量___________g,约8.2mL;需要水的体积为__________mL。
(2)量取浓硫酸和水:量取液体时要准确量取。如果量取98%的浓硫酸时俯视读数,会导致所配溶液溶质质量分数_________9.8%。(填“大于”、“小于”或“等于”)。
(3)稀释
(4)装瓶贴标签:

实验Ⅱ:测定黄铜样品中铜的质量分数。称取黄铜样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。试计算:

(5)产生氢气的质量为___________g;
(6)样品中铜的质量分数_______;
(7)反应后所得溶液中溶质的质量分数_______(计算结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】超市售卖的纯碱产品中往往会含有少量的氯化钠,某同学想通过实验来测定某品牌的纯碱样品中 的质量分数。他取了6g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸61.7g,烧杯中没有残留不溶物,称得反应后溶液的质量为65.5g。计算样品中
的质量分数。他取了6g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸61.7g,烧杯中没有残留不溶物,称得反应后溶液的质量为65.5g。计算样品中 的质量分数。(结果保留到0.1%)
的质量分数。(结果保留到0.1%)
 的质量分数。他取了6g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸61.7g,烧杯中没有残留不溶物,称得反应后溶液的质量为65.5g。计算样品中
的质量分数。他取了6g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸61.7g,烧杯中没有残留不溶物,称得反应后溶液的质量为65.5g。计算样品中 的质量分数。(结果保留到0.1%)
的质量分数。(结果保留到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】小明同学欲测定某纯碱样品(含少量氯化钠)中碳酸钠的质量分数,取26.5g该纯碱样品加入到100g水中,使其完全溶解,再加入169.3g稀盐酸,恰好完全反应,得到287g不饱和溶液。请计算:
(1)生成二氧化碳的质量为______ g。
(2)该纯碱样品中碳酸钠的质量分数。
(1)生成二氧化碳的质量为
(2)该纯碱样品中碳酸钠的质量分数。
您最近一年使用:0次



