在学习“空气”这一节时,我们知道了氮气可以用来制作氮肥。以下便是利用空气制取氮肥的流程。
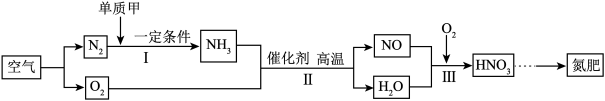
(1)将液态空气汽化,利用沸点不同将氮气和氧气分离,此过程是____ 变化(选填“物理”或“化学”)。
(2)I中反应的化学方程式为_____ 。
(3)学习氧气的性质时,我们知道了氧化反应的定义,整个流程中共有______ 个氧化反应。事实上,凡是物质所含元素化合价发生变化的反应都能称为氧化还原反应,那么反应Ⅱ______ (填"“属于”或“不属于”)氧化还原反应。
(4)HNO3和H2CO3一样,在物质分类上都属于“酸”,是我们将在下学期学习的一类新的物质。请列出HNO3中氮元素质量分数的计算式_______ 。(只列式,不计算)

(1)将液态空气汽化,利用沸点不同将氮气和氧气分离,此过程是
(2)I中反应的化学方程式为
(3)学习氧气的性质时,我们知道了氧化反应的定义,整个流程中共有
(4)HNO3和H2CO3一样,在物质分类上都属于“酸”,是我们将在下学期学习的一类新的物质。请列出HNO3中氮元素质量分数的计算式
更新时间:2022-04-15 11:13:11
|
相似题推荐
【推荐1】2022年9月27日,我国发射成功试验卫星。发射卫星使用了无毒无污染的液氢、液氧和煤油。请回答下列问题:
(1)煤油是一种无色透明的液体,易挥发和易燃,煤油完全燃烧生成水和二氧化碳。煤油具有的物理性质为_______ (写一点即可),该反应的文字表达式为_______ ;
(2)液氧是通过分离液态空气获得,该过程属于_______ (“物理”或“化学”)变化,液氧是长征五号火箭的_______ (填序号)
A.助燃剂 B.燃料 C.冷却剂 D.催化剂
(1)煤油是一种无色透明的液体,易挥发和易燃,煤油完全燃烧生成水和二氧化碳。煤油具有的物理性质为
(2)液氧是通过分离液态空气获得,该过程属于
A.助燃剂 B.燃料 C.冷却剂 D.催化剂
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下列科技短文并回答问题。
过氧化氢可用于消毒杀菌,具有不稳定性。将水蒸气冷凝在硅、玻璃、塑料、金属等材料表面,均发现了过氧化氢的存在。
研究显示:水蒸气冷凝为粒径小于10微米的液滴时,部分水分子会转化为过氧化氢分子。
水微滴中形成的过氧化氢含量随液滴尺寸的增大而减少。过氧化氢的产生量与温度、湿度等环境条件密切相关。
(1)过氧化氢不稳定的原因是______ (用文字表达式表示)。
(2)下列说法错误的是______(填字母序号)。
过氧化氢可用于消毒杀菌,具有不稳定性。将水蒸气冷凝在硅、玻璃、塑料、金属等材料表面,均发现了过氧化氢的存在。
研究显示:水蒸气冷凝为粒径小于10微米的液滴时,部分水分子会转化为过氧化氢分子。
水微滴中形成的过氧化氢含量随液滴尺寸的增大而减少。过氧化氢的产生量与温度、湿度等环境条件密切相关。
(1)过氧化氢不稳定的原因是
(2)下列说法错误的是______(填字母序号)。
| A.水蒸气在冷凝过程中可能发生化学变化 |
| B.水蒸气在玻璃表面冷凝得到的液滴一定为纯净物 |
| C.一定条件下,水蒸气冷凝可用于材料表面的绿色消毒 |
您最近一年使用:0次
【推荐3】氮元素是农作物生长必需元素,科学家一直探索将空气中N2转化为植物可吸收的含氮物质。某化学小组对N2及含氮化合物作如下探究:
(1)豆科植物根部的根瘤菌中存在固氮酶能将N2转化NH3该过程发生_________ (填“物理变化”或“化学变化”)。
(2)化学反应中有元素化合价升高,必有元素化合价降低。某同学猜想Mg(NO3)2受热分解的产物为:MgO、NO2、N2,此猜想_________ (填“合理”或“不合理”),理由是 _________ 。
(3)模拟放电条件下N2和O2反应(如图甲),观察到有红棕色气体生成;采集实验数据如图乙。
[资料] ①常温下,NO为无色气体,NO2为红棕色气体。
②同温同体积下,气体压强与气体分子个数成正比。

对于N2和O2反应生成NO2有以下两种推测:I. N2 + O2 2NO2;Ⅱ.2N2+O2
2NO2;Ⅱ.2N2+O2 2NO;2NO+2O2 = 2NO2。从图乙推测出该反应按Ⅱ进行,理由是
2NO;2NO+2O2 = 2NO2。从图乙推测出该反应按Ⅱ进行,理由是 _________ 。
(4)在推测Ⅱ合理的情况下,继续探究NO2与水反应(原理为3NO2 + H2O = 2HNO3 + NO)
[反思]④当O2与NO2体积比按_______ (填最简比)通入水中,气体能完全转化为HNO3。
(1)豆科植物根部的根瘤菌中存在固氮酶能将N2转化NH3该过程发生
(2)化学反应中有元素化合价升高,必有元素化合价降低。某同学猜想Mg(NO3)2受热分解的产物为:MgO、NO2、N2,此猜想
(3)模拟放电条件下N2和O2反应(如图甲),观察到有红棕色气体生成;采集实验数据如图乙。
[资料] ①常温下,NO为无色气体,NO2为红棕色气体。
②同温同体积下,气体压强与气体分子个数成正比。

对于N2和O2反应生成NO2有以下两种推测:I. N2 + O2
 2NO2;Ⅱ.2N2+O2
2NO2;Ⅱ.2N2+O2 2NO;2NO+2O2 = 2NO2。从图乙推测出该反应按Ⅱ进行,理由是
2NO;2NO+2O2 = 2NO2。从图乙推测出该反应按Ⅱ进行,理由是 (4)在推测Ⅱ合理的情况下,继续探究NO2与水反应(原理为3NO2 + H2O = 2HNO3 + NO)
[反思]④当O2与NO2体积比按
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】甲烷(CH4)在空气中燃烧生成水和二氧化碳。1L甲烷恰好能与2L氧气完全燃烧,生成1L的二氧化碳和一定量的液态水。
(1)甲烷燃烧的符号表达式为:_______ ;_______ (填“是”或“否”)氧化反应。
(2)在标准状况下,假设每22.4L的任何气体,含有该气体分子数目为NA个,则44.8L甲烷气体中含有的原子个数为________ 。
(3)若1L甲烷在空气中燃烧,则必须有_________ L的空气才能将甲烷反应完。
(1)甲烷燃烧的符号表达式为:
(2)在标准状况下,假设每22.4L的任何气体,含有该气体分子数目为NA个,则44.8L甲烷气体中含有的原子个数为
(3)若1L甲烷在空气中燃烧,则必须有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】学习化学后,我们学会了从宏观与微观两个角度认识事物。
(1)晋代葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银”,丹砂指的是HgS。该反应的微观示意图可以表示为(已知原子体积由大到小的顺序是Hg>S>O):
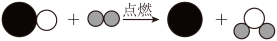
请写出该反应的化学方程式___________ ,反应中是否发生了“氧化反应”___________ (选填“是”或“否”)。
(2)随着计算化学的发展,研究人员通过“晶体结构预测”模型进行演算发现,一定条件下可实现如下反应: 。下列说法正确的是___________。
。下列说法正确的是___________。
(1)晋代葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银”,丹砂指的是HgS。该反应的微观示意图可以表示为(已知原子体积由大到小的顺序是Hg>S>O):

请写出该反应的化学方程式
(2)随着计算化学的发展,研究人员通过“晶体结构预测”模型进行演算发现,一定条件下可实现如下反应:
 。下列说法正确的是___________。
。下列说法正确的是___________。| A.反应物Na和He均为金属单质 | B.Na2He中Na为+1价,He为-1价 |
| C.Na2He由2个钠元素和1个氦元素组成 | D.一定条件下稀有气体也能参与反应 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】火灾的警示:文物保护意识应警钟长鸣,并构建安全保护机制。机制内容之一可在可燃建筑材料中加入阻燃剂,而Mg(OH)2是一种常见的阻燃剂,在380℃时分解成水蒸气和耐高温的MgO,并吸收大量的热。
(1)写出Mg(OH)2阻燃时发生反应的化学方程式:__________ ;
(2)写出Mg(OH)2阻燃的一个原因:_______ 。
(1)写出Mg(OH)2阻燃时发生反应的化学方程式:
(2)写出Mg(OH)2阻燃的一个原因:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的化学方程式,并指明基本反应的类型。
(1)镁条在氧气中燃烧______ ( )
(2)铁在氧气中燃烧______ ( )
(3)电解水______ ( )
(4)实验室制氧气_______ ( )
(5)红磷燃烧_______ ( )
(6)氢气在空气中燃烧________ ( )
(7)铜丝在空气中加热_______ ( )
(1)镁条在氧气中燃烧
(2)铁在氧气中燃烧
(3)电解水
(4)实验室制氧气
(5)红磷燃烧
(6)氢气在空气中燃烧
(7)铜丝在空气中加热
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】苏州是中国历史文化名城和重要的风景旅游城市,是长江三角洲重要的中心城市之一。
(1)苏州的美食精巧别致、名扬海内外。


①清明前后正是品尝酒酿饼的好时节,品尝后饼中飘着一股酒香味,口齿留香。面皮的主要成分为淀粉,淀粉属于_____ (填字母)。
A 糖类 B 油脂 C 蛋白质
②松鼠桂鱼含蛋白质。蛋白质是有机高分子化合物,在人体内转化为能被吸收的小分子化合物,这类化合物称为_____ 。
③在苏州,松子糖要数采芝斋的最为出名。一颗糖果里可以吃到五六个松子,带着糖果和坚果的香气,甜而不腻,松子糖属于_____ (选填“纯净物”或“混合物”)。
(2)苏州的建筑沿河而建、白墙黛瓦,诉说着苏州的历史。
①用青砖砌墙,《天工开物》中介组了烧制青砖的方法,其中载有“灌水其上”“水火既济”。相关反应为水蒸气与灼热的碳生成CO和一种气体单质,其化学方程式为_____ 。
②古代建筑工匠常用糯米灰浆粘合墙砖,糯米灰浆由糯米汁、熟石灰和砂土等混合制成。糯米灰浆属于_____ (填“复合材料”或“金属材料”),熟石灰的化学式为_____ ,其在空气中发生的化学反应是_____ (填化学方程式)。
③苏州老建筑的外墙涂成白粉墙,增加墙身保持的时间,也有加速水流、防污的作用,白粉主要是白垩,其主要成分是_____ (填物质名称)。
(1)苏州的美食精巧别致、名扬海内外。


①清明前后正是品尝酒酿饼的好时节,品尝后饼中飘着一股酒香味,口齿留香。面皮的主要成分为淀粉,淀粉属于
A 糖类 B 油脂 C 蛋白质
②松鼠桂鱼含蛋白质。蛋白质是有机高分子化合物,在人体内转化为能被吸收的小分子化合物,这类化合物称为
③在苏州,松子糖要数采芝斋的最为出名。一颗糖果里可以吃到五六个松子,带着糖果和坚果的香气,甜而不腻,松子糖属于
(2)苏州的建筑沿河而建、白墙黛瓦,诉说着苏州的历史。
①用青砖砌墙,《天工开物》中介组了烧制青砖的方法,其中载有“灌水其上”“水火既济”。相关反应为水蒸气与灼热的碳生成CO和一种气体单质,其化学方程式为
②古代建筑工匠常用糯米灰浆粘合墙砖,糯米灰浆由糯米汁、熟石灰和砂土等混合制成。糯米灰浆属于
③苏州老建筑的外墙涂成白粉墙,增加墙身保持的时间,也有加速水流、防污的作用,白粉主要是白垩,其主要成分是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】康康同学对化学中的计算问题十分感兴趣,他自己命制了两道试题请同学解答。
(1)试题1:将四种盐①Na2CO3、②NaHCO3、③CaCO3、④K2CO3分别投入等质量、等浓度的足量稀盐酸中,充分反应后所得四种溶液的质量相等,则投入盐的质量由小到大的顺序为________ (填序号)。
(2)试题2:在由上述四种盐组成的混合物中,若氧元素的质量分数为32%,则混合物中碳元素的质量分数为_________ ?小明同学经过思考后,指出该题存在一个科学性错误,请你指出该错误:_________ 。
(1)试题1:将四种盐①Na2CO3、②NaHCO3、③CaCO3、④K2CO3分别投入等质量、等浓度的足量稀盐酸中,充分反应后所得四种溶液的质量相等,则投入盐的质量由小到大的顺序为
(2)试题2:在由上述四种盐组成的混合物中,若氧元素的质量分数为32%,则混合物中碳元素的质量分数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】激动人心、令人赏心悦月的体育运动中,处处充满化学知识。
(1)体操、举重等运动员赛前常在手上涂抹碳酸镁粉末用于防滑。碳酸镁是由______ (填微粒符号)和 构成。
构成。
(2)足球比赛中可向球员受伤部位喷氯乙烷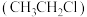 米缓解疼痛。当氯乙烷药液喷洒在运动员受伤部位时,会很快“消失”在空气中,是因为药液分子
米缓解疼痛。当氯乙烷药液喷洒在运动员受伤部位时,会很快“消失”在空气中,是因为药液分子______ ,该过程______ (“吸热”或“放热”),使表面皮肤温度骤降,知觉减退,起锁痛和麻醉作用。
(3)赛跑时发令枪响的同时会产生白烟,反应的化学方程式为 的化学式为
的化学式为______ 。
(4)体育机构允许运动员使用的药物有:葡萄糖、氨基酸混合物和维生素 等。
等。
①葡萄糖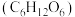 在人体内酶的他化下与
在人体内酶的他化下与 反应生成
反应生成 和
和 ,同时提供人体所需能量。该反应的化学方程式为
,同时提供人体所需能量。该反应的化学方程式为______ 。
②丙氨酸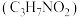 是一种常见的氨基酸,其中氮元素的质量分数是
是一种常见的氨基酸,其中氮元素的质量分数是______ 。(精确到 )
)
(1)体操、举重等运动员赛前常在手上涂抹碳酸镁粉末用于防滑。碳酸镁是由
 构成。
构成。(2)足球比赛中可向球员受伤部位喷氯乙烷
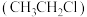 米缓解疼痛。当氯乙烷药液喷洒在运动员受伤部位时,会很快“消失”在空气中,是因为药液分子
米缓解疼痛。当氯乙烷药液喷洒在运动员受伤部位时,会很快“消失”在空气中,是因为药液分子(3)赛跑时发令枪响的同时会产生白烟,反应的化学方程式为
 的化学式为
的化学式为(4)体育机构允许运动员使用的药物有:葡萄糖、氨基酸混合物和维生素
 等。
等。①葡萄糖
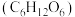 在人体内酶的他化下与
在人体内酶的他化下与 反应生成
反应生成 和
和 ,同时提供人体所需能量。该反应的化学方程式为
,同时提供人体所需能量。该反应的化学方程式为②丙氨酸
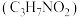 是一种常见的氨基酸,其中氮元素的质量分数是
是一种常见的氨基酸,其中氮元素的质量分数是 )
)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】理解化学概念和认识身边的化学物质,也是学好化学的一条重要途径。
(1)相对原子质量和原子结构是化学的重要概念。
①已知碳-12原子的质量1.993×10-26kg,一种氧原子的质量为2.657×10-26kg,计算该氧原子的相对原子质量为_____ (只列出计算式)。
②下表是几种原子的构成及其相对原子质量近似值
通过阅读,你获得的信息有:________ (只写出一条即可)。
(2)氧气具有广泛用途,工业制取氧气主要流程为:

①氧气的沸点_____ (填“高”或“低”或“等”)于-196℃;
②通过上述流程得到的“液体剩余物”是_____ (填“纯净物”或“混合物”)。
(3)水是生命之源,人类的生活生产离不开水。
①硬水中含有较多可溶性钙镁化合物,日常生活中常采用______ 的方法来降低水的硬度。
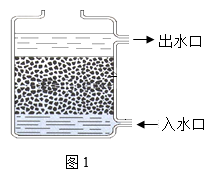
②如图1是活性炭净水器的示意图,图中活性炭作用是_____ ,水从下方进入上方出来的目的是_____ 。
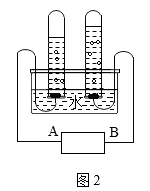
③电解水实验如图2所示,电源的正极是_____ (填A或B),科学家们用“电解法”证明了水的组成,其依据的原理是_____ 。
④36g水中含有氢元素的质量与______ g过氧化氢中所含氢元素的质量相同。
(1)相对原子质量和原子结构是化学的重要概念。
①已知碳-12原子的质量1.993×10-26kg,一种氧原子的质量为2.657×10-26kg,计算该氧原子的相对原子质量为
②下表是几种原子的构成及其相对原子质量近似值
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 相对原子质量(近似值) |
| 氢 | 1 | 0 | 1 | 1 |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
(2)氧气具有广泛用途,工业制取氧气主要流程为:

①氧气的沸点
②通过上述流程得到的“液体剩余物”是
(3)水是生命之源,人类的生活生产离不开水。
①硬水中含有较多可溶性钙镁化合物,日常生活中常采用
②如图1是活性炭净水器的示意图,图中活性炭作用是

③电解水实验如图2所示,电源的正极是

④36g水中含有氢元素的质量与
您最近一年使用:0次



