为除去粗盐中的泥沙和CaC12、MgCl2杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后取粗盐水按以下流程进行实验探究。
粗盐→溶解→依次加入过量的①氢氧化钠溶液、②碳酸钠溶液→过滤→③加入适量盐酸→蒸发→精盐
(1)写出溶解、过滤、蒸发操作中都用到的一种玻璃仪器名称。
(2)写出一个碳酸钠溶液参与反应的化学方程式。
(3)准备加入氢氧化钠溶液时,同学们发现装氢氧化钠溶液的试剂瓶已经被打开,同学们如何可以证明氢氧化钠已部分变质。(写出操作步骤、现象)
(4)有同学提出用此部分变质的氢氧化钠溶液,也可完成实验;你认为他说的可行吗?若可行你认为可以省去哪一步?请从下列答案中找到正确答案的选项。
粗盐→溶解→依次加入过量的①氢氧化钠溶液、②碳酸钠溶液→过滤→③加入适量盐酸→蒸发→精盐
(1)写出溶解、过滤、蒸发操作中都用到的一种玻璃仪器名称。
(2)写出一个碳酸钠溶液参与反应的化学方程式。
(3)准备加入氢氧化钠溶液时,同学们发现装氢氧化钠溶液的试剂瓶已经被打开,同学们如何可以证明氢氧化钠已部分变质。(写出操作步骤、现象)
(4)有同学提出用此部分变质的氢氧化钠溶液,也可完成实验;你认为他说的可行吗?若可行你认为可以省去哪一步?请从下列答案中找到正确答案的选项。
| A.不可行 | B.可行,可以省掉② | C.可行,可以省掉③ |
2022·河南南阳·一模 查看更多[2]
更新时间:2022-04-22 10:37:00
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】一瓶敞口放置的NaOH,设计实验证明它是部分变质的___ ,并写出实验过程中发生反应的化学方程式____ ,若要把变质后的杂质除去得到较纯净的NaOH溶液,写出除杂发生反应的化学方程式_____ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】小明在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验:
请回答以下几个问题:

(1)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验①_________________ 。实验③_________________ 。
(2)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶 ,以使实验取得成功,你将选用的物品是________________ ,改进后能看到的实验现象是______________________ 。
(3)请你进一步设计实验来检验CO2和NaOH溶液反应生成了Na2CO3,并将有关的实验操作、现象、结论填入下表:
请回答以下几个问题:

(1)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验①
(2)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的
(3)请你进一步设计实验来检验CO2和NaOH溶液反应生成了Na2CO3,并将有关的实验操作、现象、结论填入下表:
实验操作 | 实验现象 | 结 论 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】为实现废物“资源化利用的目的,以电石渣[主要成份为Ca(OH)2 和 CaCO3 ]为原料制备 KClO3 ,其主要流程如图所示:

(已知:Cl2有毒,Ca(OH)2微溶于水)
(1)氯化过程,Cl2与Ca(OH)2作用,发生了一系列变化,最终生成Ca(ClO3)2 和 CaCl2,该反应的化学方程式中Ca(ClO3)2和CaCl2化学计量数比为 1:5
①生成Ca(ClO3)2的化学方程式为________ ;
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有___________ (填标号)。
A 适当减缓通Cl2速率
B充分搅拌浆料
C加水使Ca(OH)2完全溶解
(2)步骤甲的操作名称为________ ;加活性炭的目的是__________ 。
(3)向步骤甲得到的溶液中加入稍过量 KCl 固体可将Ca(ClO3)2 转化为KClO3 ,该反应的基本反应类型为_________ 。

(已知:Cl2有毒,Ca(OH)2微溶于水)
(1)氯化过程,Cl2与Ca(OH)2作用,发生了一系列变化,最终生成Ca(ClO3)2 和 CaCl2,该反应的化学方程式中Ca(ClO3)2和CaCl2化学计量数比为 1:5
①生成Ca(ClO3)2的化学方程式为
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有
A 适当减缓通Cl2速率
B充分搅拌浆料
C加水使Ca(OH)2完全溶解
(2)步骤甲的操作名称为
(3)向步骤甲得到的溶液中加入稍过量 KCl 固体可将Ca(ClO3)2 转化为KClO3 ,该反应的基本反应类型为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
【推荐2】图中表示的是几种常见物质的转化关系(部分反应物、生成物及反应条件省略),已知C为生活中不可缺少的调味品,F为某种建筑材料的主要成分,请回答以下问题:

(1)写出E的化学式__ ;
(2)写出F和B反应的化学方程式__ ;
(3)写出D和I的溶液反应的现象__ ;
(4)写出I的一种用途__ .

(1)写出E的化学式
(2)写出F和B反应的化学方程式
(3)写出D和I的溶液反应的现象
(4)写出I的一种用途
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】醋酸钙[Ca(Ac)2]是国家允许使用的补钙制剂之一。以蛋壳为原料回收膜并制备醋酸钙的一种工艺流程如下:

(1)写出煅烧时的化学方程式:________ 。CO2的任意排放会引发的环境问题是________ 。CO2与CH4一定条件下化合生成甲醛(HCHO),则此反应中CO2与CH4的最佳质量比是______ 。下列做法能减少二氧化碳排放的是_____ (填序号)。
A.尽量选择公共交通工具出行 B.用焚烧的方式处理稻草 C.大力发展风能
(2)在反应Ⅰ中制备石灰乳,而不是制备澄清石灰水的目的是_______ 。写出熟石灰的一种用途:__________ 。
(3)在反应Ⅱ中醋酸过量的目的是_________ 。写出反应Ⅱ的化学方程式:___________ 。

(1)写出煅烧时的化学方程式:
A.尽量选择公共交通工具出行 B.用焚烧的方式处理稻草 C.大力发展风能
(2)在反应Ⅰ中制备石灰乳,而不是制备澄清石灰水的目的是
(3)在反应Ⅱ中醋酸过量的目的是
您最近一年使用:0次
【推荐1】某企业将海水综合利用与联合制碱法结合,实现资源利用最大化。
①母液中含有大量MgCl2、少量的CaCl2等。
②NaHCO3受热易分解。
③氨气极易溶于水,二氧化碳能溶于水。
(1)从海水中获得粗盐的方法是______ (填“蒸发结晶”或“降温结晶”),得到的母液是氯化钠的______ (填“饱和”或“不饱和”)溶液。
(2)向饱和食盐水中先通足量的NH3,再缓缓通入CO2的目的是______ 。
(3)制备NaHCO3固体过程中采用水浴加热,温度维持在42℃左右。温度过低,反应速率太慢,不利于晶体析出,温度也不宜过高,原因是______ 、______ 。
(4)向母液中加入石灰乳,生成氢氧化镁的化学方程式为______ ;工业上常常选用石灰乳而不选用澄清石灰水的理由是______ ,实际工业生产中,部分企业选择价格较高的NaOH进行沉镁而不选用石灰乳的理由是______ 。
(5)为了尽可能除尽Ca2+,同时减少Mg2+的损耗,某同学设计了利用Na2CO3做脱钙剂,控制不同反应条件的实验,结果如下:(A表示Na2CO3与CaCl2的质量比)
以去除钙离子为核心,综合考虑多方面因素,你认为最优的方案是______ (填实验序号),理由是______ 。

①母液中含有大量MgCl2、少量的CaCl2等。
②NaHCO3受热易分解。
③氨气极易溶于水,二氧化碳能溶于水。
(1)从海水中获得粗盐的方法是
(2)向饱和食盐水中先通足量的NH3,再缓缓通入CO2的目的是
(3)制备NaHCO3固体过程中采用水浴加热,温度维持在42℃左右。温度过低,反应速率太慢,不利于晶体析出,温度也不宜过高,原因是
(4)向母液中加入石灰乳,生成氢氧化镁的化学方程式为
(5)为了尽可能除尽Ca2+,同时减少Mg2+的损耗,某同学设计了利用Na2CO3做脱钙剂,控制不同反应条件的实验,结果如下:(A表示Na2CO3与CaCl2的质量比)
| 实验序号 | A | 温度/℃ | 反应时间 | 静置时间 | Ca2+去除率 | Mg2+损耗率 |
| 1 | 106.0:111 | 25 | 2min | 30 min/ | 65.8% | 7.4% |
| 2 | 106.0:111 | 30 | 4min | 60 min | 77.6% | 9.4% |
| 3 | 127.2:111 | 25 | 4min | 90min | 82.4% | 14% |
| 4 | 127.2:111 | 30 | 6min | 30min | 90.5% | 12.6% |
| 5 | 148.4:111 | 25 | 6min | 60min | 90.8% | 15.9% |
| 6 | 148.4:111 | 30 | 2min | 90min | 83.4% | 16.4% |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】食盐是一种重要的化工原料。粗盐中常含有少量的CaCl2、MgCl2、Na2SO4等杂质,将粗盐进行精制的流程如下图:

(1)过量X(纯净物)溶液中的溶质是_________________ 。
(2)加入过量稀盐酸的目的可以除去滤液中过量的碳酸钠溶液,还有一个作用是_______ (用化学方程式表示。)
(3)在操作Ⅲ中玻璃棒的作用是什么___________ ?

(1)过量X(纯净物)溶液中的溶质是
(2)加入过量稀盐酸的目的可以除去滤液中过量的碳酸钠溶液,还有一个作用是
(3)在操作Ⅲ中玻璃棒的作用是什么
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】水是人类宝贵的自然资源,与人类的生产、生活密切相关。
(1)水__________ (“属于”或“不属于”)人类所需的六大基本营养素之一。写出一个反应生成水又属于化合反应的化学方程式:____________________ 。

(2)在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如上图所示,甲、丙还有剩余固体,乙固体全部溶解。升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化。
室温时,_____ (填“甲”、“乙”或“丙”)溶液可能是不饱和溶液。
如图中能表示乙物质的溶解度曲线的是________ (填“a”、“b”或“c”)。
t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中溶质质量分数由大到小的顺序是________ 。

(3)粗盐提纯过程如图,操作I中要用到的玻璃仪器有烧杯、玻璃棒和______________ 。某同学所得精盐比其他同学明显要少,原因可能是________ 。
A.溶解时将粗盐一次全部倒入水中,立即过滤 B.提纯后所得精盐尚未完全干燥
(1)水

(2)在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如上图所示,甲、丙还有剩余固体,乙固体全部溶解。升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化。
室温时,
如图中能表示乙物质的溶解度曲线的是
t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中溶质质量分数由大到小的顺序是

(3)粗盐提纯过程如图,操作I中要用到的玻璃仪器有烧杯、玻璃棒和
A.溶解时将粗盐一次全部倒入水中,立即过滤 B.提纯后所得精盐尚未完全干燥
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】为探究某化工厂固体废物的成分,以便回收有用物质,除掉有害物质。已知固体废物的主要成分是NaCl,还可能含有Na2CO3、K2SO4、NH4NO3、MgSO4、FeCl3,通过以下探究回答下列问题。
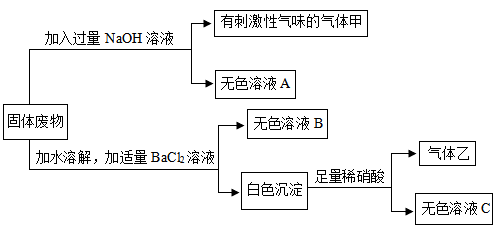
(1)无色溶液A中存在的阴离子有_________ 。
(2)反应生成气体甲的化学方程式为__________ 。
(3)原固体废物中一定存在的物质有_________ 。

(1)无色溶液A中存在的阴离子有
(2)反应生成气体甲的化学方程式为
(3)原固体废物中一定存在的物质有
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成.为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含______ ,______ ;
(2)生成白色沉淀的化学方程式为____________________ .

(3)为最终确定白色粉末的组成,某同学称取10.0g该白色粉末溶于水,加入足量的盐酸,产生气体的量与加入盐酸的质量如图所示.则原粉末中一定含有NaOH,你认为此结论_____ (选填“是”或“否”)正确.并计算Na2CO3的质量分数为______ .

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含
(2)生成白色沉淀的化学方程式为

(3)为最终确定白色粉末的组成,某同学称取10.0g该白色粉末溶于水,加入足量的盐酸,产生气体的量与加入盐酸的质量如图所示.则原粉末中一定含有NaOH,你认为此结论
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】现有一固体混合物A,可能含有NaCl、Na2CO3或两者之一,另有一固体混合物B,可能含有NH4NO3、MgCl2、CuO三种物质中的一种或多种。按图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行)。

试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体C的化学式是________ 。
(2)溶液M中肯定存在的酸根离子是___________ (写离子符号)。
(3)写出过程③中生成沉淀H的化学方程式_________ 。
(4)根据上述实验,在混合物B中,肯定不存在的物质是(写化学式)__________ ;得此结论的理由是_________ 。

试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体C的化学式是
(2)溶液M中肯定存在的酸根离子是
(3)写出过程③中生成沉淀H的化学方程式
(4)根据上述实验,在混合物B中,肯定不存在的物质是(写化学式)
您最近一年使用:0次



