敞口放置的氢氧化钠溶液易吸收空气中的二氧化碳而变质生成碳酸钠。现向100g部分变质的氢氧化钠溶液中逐滴加入盐酸,并振荡。反应过程中溶液质量随盐酸质量变化的曲线如图。请回答:
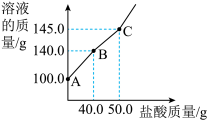
(1)氢氧化钠溶液变质的化学方程式是__________ 。
(2)图中线段AB表示盐酸与氢氧化钠反应,则BC对应的实验现象是__________ 。
(3)反应生成的二氧化碳的质量是__________ 。
(4)该100g溶液中碳酸钠的质量是______ ?请写出计算过程。

(1)氢氧化钠溶液变质的化学方程式是
(2)图中线段AB表示盐酸与氢氧化钠反应,则BC对应的实验现象是
(3)反应生成的二氧化碳的质量是
(4)该100g溶液中碳酸钠的质量是
更新时间:2022-04-29 21:15:52
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】候德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下: ,请回答:
,请回答:
(1)标出NH4Cl中氮元素的化合价:_____ 。
(2)消耗117t氯化钠,理论上可以生产氯化铵的质量是多少?
 ,请回答:
,请回答:(1)标出NH4Cl中氮元素的化合价:
(2)消耗117t氯化钠,理论上可以生产氯化铵的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某学校的学习小组对当地的石灰石矿区进行调查。采用的方法如下:现取25g石灰石样品于烧杯中,缓慢加入稀盐酸(石灰石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示:

(1)石灰石中碳酸钙的质量_______ 。
(2)所用稀盐酸的溶质质量分数(写出计算过程,下同)。
(3)求恰好完全反应时,所得溶液的溶质质量分数(保留0.1%)。

(1)石灰石中碳酸钙的质量
(2)所用稀盐酸的溶质质量分数(写出计算过程,下同)。
(3)求恰好完全反应时,所得溶液的溶质质量分数(保留0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某兴趣小组协助教师整理药品时,发现有一瓶装有烧碱试剂瓶的瓶塞没塞紧,实验兴趣小组想测定该瓶中氢氧化钠的质量分数。小东取一定量的烧碱样品加水稀释,倒入放在电子秤上的烧杯内,然后将 100g稀盐酸分 5 次加入烧杯中,记录实验数据如下表。
(1)加入盐酸的过程中,观察到的现象是______ 。
(2)实验取用的稀盐酸的质量分数是多少?
(3)该瓶中氢氧化钠的质量分数是多少?(不考虑氢氧化钠吸水潮解,结果保留到 0.1%)
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸质量/g | 20 | 20 | 20 | 20 | 20 |
| 充分反应后电子秤的读数/g | 220 | 240 | 258.9 | 276.7 | 295.6 |
(2)实验取用的稀盐酸的质量分数是多少?
(3)该瓶中氢氧化钠的质量分数是多少?(不考虑氢氧化钠吸水潮解,结果保留到 0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室中某实验小组同学,正在测定某赤铁矿石样品中氧化铁的含量(杂质不溶于水,也不与其他物质反应),进行了如下实验:

(1)上述实验过程中发生反应的化学方程式为______ 。
(2)根据已知条件列出求解稀盐酸中溶质质量(X)的比例式为______ 。
(3)该样品中氧化铁的含量为______ 。
(4)若向所得滤液中加入9g水,则所得溶液中溶质的质量分数为______ 。
(5)配制7.3%的稀盐酸400g,需要36.5%的浓盐酸的质量为______ 。
(6)某钢铁厂每天用上述赤铁矿石1200t来生产生铁,则理论上日产含杂质4%的生铁的质量为______ 。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解稀盐酸中溶质质量(X)的比例式为
(3)该样品中氧化铁的含量为
(4)若向所得滤液中加入9g水,则所得溶液中溶质的质量分数为
(5)配制7.3%的稀盐酸400g,需要36.5%的浓盐酸的质量为
(6)某钢铁厂每天用上述赤铁矿石1200t来生产生铁,则理论上日产含杂质4%的生铁的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某实验小组取用铜和氧化铜的混合物20g,向其中逐滴加入稀H2SO4,测得剩余固体的质量与加入稀H2SO4的质量关系如图所示。回答下列问题:

(1)氧化铜中铜元素的质量分数______ 。
(2)计算稀H2SO4中溶质的质量分数(写出计算过程)。

(1)氧化铜中铜元素的质量分数
(2)计算稀H2SO4中溶质的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】小明用变质的氢氧化钠样品进行了如图所示的实验。请回答:

(1)小慧分析,小明计算的样品中碳酸钠的质量分数有可能偏大,你认为她的理由是_____ 。
(2)请计算样品中碳酸钠的质量分数(计算结果精确到0.1%)。

(1)小慧分析,小明计算的样品中碳酸钠的质量分数有可能偏大,你认为她的理由是
(2)请计算样品中碳酸钠的质量分数(计算结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】氢氧化钠是一种重要的化工原料,广泛用于造纸、纺织、石油化工等方面。
(1)氢氧化钠具有强烈的腐蚀性,使用时必须十分小心。如果不慎沾在皮肤上,要立即用大量水冲洗,然后涂上___________ (填“氢氧化钙”“硼酸”之一)溶液。
(2)氢氧化钠固体放在空气中易吸收水分,并能与二氧化碳反应而变质,所以应该密封保存。氢氧化钠在空气中变质的原因是(用化学方程式表示)___________ 。
(3)室温下,某实验小组的同学取一定量的Na2CO3粉末于烧杯中,加入足量水溶解后,再逐滴加入溶质质量分数为11.1%的CaCl2溶液,反应生成沉淀的质量与加入CaCl2溶液的质量关系如下图所示。试回答:

①Na2CO3的水溶液显___________ (填“酸性”“中性”“碱性”之一)。
②当滴入CaCl2溶液60g时(即图中A点),烧杯中溶液里含有的溶质为___________ (写化学式)。
③当滴入11.1%的CaCl2溶液100g时(即图中B点),恰好完全反应,试通过计算,求所取碳酸钠的质量(计算结果精确至0.1g)__________ 。
(1)氢氧化钠具有强烈的腐蚀性,使用时必须十分小心。如果不慎沾在皮肤上,要立即用大量水冲洗,然后涂上
(2)氢氧化钠固体放在空气中易吸收水分,并能与二氧化碳反应而变质,所以应该密封保存。氢氧化钠在空气中变质的原因是(用化学方程式表示)
(3)室温下,某实验小组的同学取一定量的Na2CO3粉末于烧杯中,加入足量水溶解后,再逐滴加入溶质质量分数为11.1%的CaCl2溶液,反应生成沉淀的质量与加入CaCl2溶液的质量关系如下图所示。试回答:

①Na2CO3的水溶液显
②当滴入CaCl2溶液60g时(即图中A点),烧杯中溶液里含有的溶质为
③当滴入11.1%的CaCl2溶液100g时(即图中B点),恰好完全反应,试通过计算,求所取碳酸钠的质量(计算结果精确至0.1g)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐3】某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠和一瓶未标浓度的稀盐酸。为测定氢氧化钠的变质情况和稀盐酸的浓度,他们取9.3g变质的氢氧化钠样品于锥形瓶中,加入50g水,充分溶解,再向锥形瓶中滴加未知浓度的稀盐酸。实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如下图所示。

求:(1)9.3g样品中碳酸钠的质量。
(2)未知浓度的稀盐酸的溶质质量分数。

求:(1)9.3g样品中碳酸钠的质量。
(2)未知浓度的稀盐酸的溶质质量分数。
您最近一年使用:0次

 可实现氢气的存储,请计算23kg金属钠最多可吸收氢气的质量。
可实现氢气的存储,请计算23kg金属钠最多可吸收氢气的质量。


