2022北京冬奥会首钢滑雪大跳台造型设计来自敦煌“飞天”飘带形象,曲线优美。
(1)跳台主体为钢结构,钢的硬度_______ (填“大于”或“小于”)纯铁。
(2)跳台采用的耐火耐候钢自带防火和防锈功能。工业上常用稀盐酸除铁锈,该反应的化学方程式为_______ 。
(3)耐火耐候钢还含有铜、镍(Ni)等金属,资料显示金属活动性:Fe>Ni>H>Cu,Ni在化合物中通常呈+2价。为验证这三种金属的活动性顺序,你所选择的试剂是_______ 。
(1)跳台主体为钢结构,钢的硬度
(2)跳台采用的耐火耐候钢自带防火和防锈功能。工业上常用稀盐酸除铁锈,该反应的化学方程式为
(3)耐火耐候钢还含有铜、镍(Ni)等金属,资料显示金属活动性:Fe>Ni>H>Cu,Ni在化合物中通常呈+2价。为验证这三种金属的活动性顺序,你所选择的试剂是
更新时间:2022-05-02 09:25:54
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】各种物质之间存在着某种联系,请用“>”“=”“<”“≥”“≤”填空:
(1)熔点:硬铝_____ 铝;
(2)含碳量:生铁_____ 钢;
(3)质子数:氧原子_____ 氧离子;
(4)amL酒精中加入bmL水,混合后的体积为cmL,则a+b_____ c;
(5)xg镁与yg氧气充分反应,得到zg氧化镁,则x+y_____ z。
(1)熔点:硬铝
(2)含碳量:生铁
(3)质子数:氧原子
(4)amL酒精中加入bmL水,混合后的体积为cmL,则a+b
(5)xg镁与yg氧气充分反应,得到zg氧化镁,则x+y
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】随着“共享经济”的概念迅速普及,共享汽车也随之悄然进入了人们的视野,共享汽车的出现为人们的生活带来方便快捷,如图所示,“共享汽车”使用的是纯电动汽车,请回答下列问题。

(1)“共享汽车”的外部材料中的橡胶轮胎属于______ 材料。
(2)铝合金在日常生活、工农业生产中具有广泛的用途,铝合金具有等性能______ (填字母序号)。
A.强度和硬度好B.抗腐蚀性能好C.密度大
(3)电动汽车中应用最广泛的电池是铅酸蓄电池,放电时可把PbO2转化为PbSO4,则放电时铅元素的化合价变化为______ ,放电时的能量转化是______ 。
(4)电动汽车的使用减少了化石燃料的消耗,同时,电动汽车与传统燃油汽车相比,还具有的主要优点是______ 。

(1)“共享汽车”的外部材料中的橡胶轮胎属于
(2)铝合金在日常生活、工农业生产中具有广泛的用途,铝合金具有等性能
A.强度和硬度好B.抗腐蚀性能好C.密度大
(3)电动汽车中应用最广泛的电池是铅酸蓄电池,放电时可把PbO2转化为PbSO4,则放电时铅元素的化合价变化为
(4)电动汽车的使用减少了化石燃料的消耗,同时,电动汽车与传统燃油汽车相比,还具有的主要优点是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】2019年10月1日北京天安门广场,纪念抗日战争胜利74周年暨世界反法西斯战争胜利74周年大会隆重举行。11时23分许,11个空中梯队从远方飞来,全场目光投向天安门上空。请回答问题:

(1)制造飞机排气口的材料是钛合金,这主要是利用了钛合金_____ 的性质(填字母)。
A 硬度大 B 熔点高 C 密度大
(2)飞机用航空煤油做燃料,飞机飞行过程中的能量转化过程是_____ (用“→”表示转化)
(3)工业上用钛酸亚铁(FeTiO3)先制得四氯化钛(TiC14),再用镁置换出四氯化钛中的钛。首先,钛酸亚铁与碳、氯气在高温条件下反应生成四氯化钛、一种黄色溶液及一种污染空气的气体,请写出该反应的化学方程式_____ ,反应前后铁元素化合价变化情况为_______ 。
(4)飞机飞行时会产生有害气体和烟尘污染空气,请写出空气污染的危害_____ (一点即可)

(1)制造飞机排气口的材料是钛合金,这主要是利用了钛合金
A 硬度大 B 熔点高 C 密度大
(2)飞机用航空煤油做燃料,飞机飞行过程中的能量转化过程是
(3)工业上用钛酸亚铁(FeTiO3)先制得四氯化钛(TiC14),再用镁置换出四氯化钛中的钛。首先,钛酸亚铁与碳、氯气在高温条件下反应生成四氯化钛、一种黄色溶液及一种污染空气的气体,请写出该反应的化学方程式
(4)飞机飞行时会产生有害气体和烟尘污染空气,请写出空气污染的危害
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属在生产和生活中应用广泛。请回答下列问题。
(1)用铜作导线,利用了铜的延展性和_______ 性。
(2)厨房中铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法_______ 。
(3)铝合金制造的飞机外壳,具有轻量化、能抗击强大气流的冲击、耐受水雾和雨雪侵蚀等特点。这是利用了铝合金的_______ 等优点(写出一条即可)。
(4)某研究小组为探究铁、铜、锰(Mn)的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用5%的盐酸体积相同)。
【实验记录与分析】
(5)近年来,我国高铁飞速发展,已经为世界上唯一高铁成网运行的国家。请回答下列问题:
①高铁所用金属材料主要来源于金属资源。下列有关保护金属资源的说法中合理的是_______ (填字母序号)。
A 不顾国家的利益乱采矿 B 常用水清洗铁制品表面
C 铁生锈后没有回收价值 D 用塑料代替金属做水管
②建造高铁使用了大量铁合金,构成金属铁的粒子是_______ (填“分子”或“原子”或“离子”)。
③将一定质量的铁投入到硝酸镁、硝酸银和硝酸铜的混合溶液中,充分反应后过滤。得到滤渣和滤液。将滤渣洗涤、干燥。取滤渣滴加稀盐酸,无气泡产生,则滤渣中一定含有的物质是_______ ;取滤液滴加氯化钠溶液,无明显现象,则滤液中一定不含有的溶质是_______ 。
(1)用铜作导线,利用了铜的延展性和
(2)厨房中铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法
(3)铝合金制造的飞机外壳,具有轻量化、能抗击强大气流的冲击、耐受水雾和雨雪侵蚀等特点。这是利用了铝合金的
(4)某研究小组为探究铁、铜、锰(Mn)的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用5%的盐酸体积相同)。
【实验记录与分析】
| 实验一 | 实验二 | 实验三 | |
| 实验操作 | 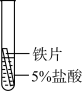 |  | 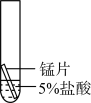 |
| 实验现象 | 立即产生气泡,速率较慢 | 无明显现象 | 立即产生气泡,速率较快 |
| 实验结论 | 铁、铜、锰的金属活动性顺序由强到弱为 | ||
①高铁所用金属材料主要来源于金属资源。下列有关保护金属资源的说法中合理的是
A 不顾国家的利益乱采矿 B 常用水清洗铁制品表面
C 铁生锈后没有回收价值 D 用塑料代替金属做水管
②建造高铁使用了大量铁合金,构成金属铁的粒子是
③将一定质量的铁投入到硝酸镁、硝酸银和硝酸铜的混合溶液中,充分反应后过滤。得到滤渣和滤液。将滤渣洗涤、干燥。取滤渣滴加稀盐酸,无气泡产生,则滤渣中一定含有的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】通过一学期的化学学习,我们已经了解了常见金属的活动性顺序。铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行了探究,过程如下:
【提出假设】对三种金属的活动性顺序提出的三种可能的假设:
A.Al>Cr>Cu B.Cr>Al>Cu C._________
【设计实验】相同温度下,取大小相同的打磨过的金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象,记录如下:
【控制实验条件】打磨三种金属的原因是_______ ,上述实验使用等浓度的盐酸的理由是_______ 。
【得出结论】原假设中正确的是_______ (填“A”“B”或“C”)。写出铬与盐酸反应的化学方程式:_______ (已知铬的硫酸化合物化学式为CrSO4)。
【应用】根据探究结果,在CuCl2和AlCl3的混合液中加入一定量的金属铬,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有的溶质成分是________ 。
【提出假设】对三种金属的活动性顺序提出的三种可能的假设:
A.Al>Cr>Cu B.Cr>Al>Cu C.
【设计实验】相同温度下,取大小相同的打磨过的金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象,记录如下:
金属 | Cr | Al | Cu |
| 与盐酸反应的现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生剧烈,金属迅速溶解 | 无气泡产生,金属无变化 |
【得出结论】原假设中正确的是
【应用】根据探究结果,在CuCl2和AlCl3的混合液中加入一定量的金属铬,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有的溶质成分是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属及金属材料广泛应用于生产、生活,其应用推动了社会的发展。
(1)下列金属应用的实例中,主要利用金属导电性的是________(填标号)。
(2)钢铁是使用最多的金属材料。钢和生铁在性能上有较大差异的主要原因是________ 。
(3)《天工开物》中记载“铁器淬于胆矾水中,即成铜色”,胆矾水即硫酸铜溶液,写出该反应的化学方程式________ ,该反应的基本反应类型为________ 反应。
(4)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是________ (填标号)。
①Fe、Cu、Ag、稀盐酸
②FeSO4溶液、Cu、AgNO3溶液
③Fe、CuSO4溶液、Ag
④FeSO4溶液、CuSO4溶液、Ag
⑤FeSO4溶液、Cu、Ag
(5)将锌粉加入盛有一定量硝酸银和硝酸铜的混合溶液中,反应过程如图所示:

滤渣中一定含有________ (填化学式)。
(1)下列金属应用的实例中,主要利用金属导电性的是________(填标号)。
| A.铜导线 | B.银手镯 | C.铁锅 | D.金属乐器 |
(3)《天工开物》中记载“铁器淬于胆矾水中,即成铜色”,胆矾水即硫酸铜溶液,写出该反应的化学方程式
(4)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是
①Fe、Cu、Ag、稀盐酸
②FeSO4溶液、Cu、AgNO3溶液
③Fe、CuSO4溶液、Ag
④FeSO4溶液、CuSO4溶液、Ag
⑤FeSO4溶液、Cu、Ag
(5)将锌粉加入盛有一定量硝酸银和硝酸铜的混合溶液中,反应过程如图所示:

滤渣中一定含有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
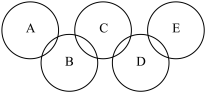
【推荐1】如图,A、B、C、D、E是初中化学常见的五种不同类别的物质,其中E是单质,且A、E均为黑色粉末,人体胃液中含有B,物质C与D是配制农药波尔多液的原料,图中两圆相交表示圆中的物质间能发生化学反应,请回答:_______ 。
(2)C物质除了能配制农药波尔多液外,还有很多用途,请列举一个_______ 。
(3)C溶液与D溶液反应的化学方程式是_______ 。
(4)D与E的反应基本类型是______ 。
(2)C物质除了能配制农药波尔多液外,还有很多用途,请列举一个
(3)C溶液与D溶液反应的化学方程式是
(4)D与E的反应基本类型是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】小芳结合所学有关酸、碱的知识,用图 1 总结了盐酸的四条化学性质(即盐酸与这四类物质能 够发生化学反应)。
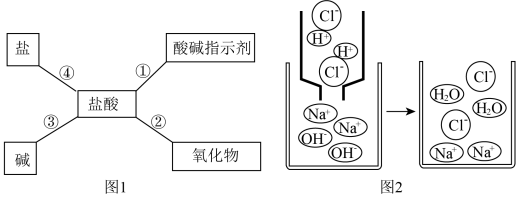
(1)为了验证性质①,小芳将紫色石蕊试液滴入盐酸溶液中,溶液变成_____ 色。
(2)依据性质②,盐酸常用于金属的除锈,用盐酸除去生锈铁钉表面铁锈的反应的化学方程式为_____ 。
(3)小明用微观示意图(图 2)来说明性质③反应的发生过程,用化学反应方程式表示为_____ 。从该图可以看出,该反应的微观实质是:_____ 。
(4)为了验证性质④反应能够发生,你选择的物质是_____ 。
A Na2CO3 B HCl C CuSO4 D NaCl

(1)为了验证性质①,小芳将紫色石蕊试液滴入盐酸溶液中,溶液变成
(2)依据性质②,盐酸常用于金属的除锈,用盐酸除去生锈铁钉表面铁锈的反应的化学方程式为
(3)小明用微观示意图(图 2)来说明性质③反应的发生过程,用化学反应方程式表示为
(4)为了验证性质④反应能够发生,你选择的物质是
A Na2CO3 B HCl C CuSO4 D NaCl
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组利用“盐酸、硫酸铜、氢氧化钠、碳酸钠、硝酸钾”五种溶液对“复分解反应发生的条件”进行微观探析。
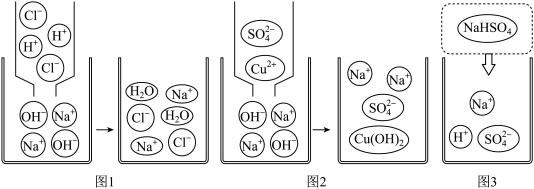
(1)图1是向滴有酚酞试剂的氢氧化钠溶液中滴加稀盐酸的微观示意图,该反应过程没有变化的微粒是___________ ,反应的微观实质是___________ 。
(2)图2向氢氧化钠溶液中滴加硫酸铜溶液的微观示意图,其反应的化学方程式是___________ ,反应的微观实质是___________ 。
(3)图3是硫酸氢钠在水中解离的微观示意图,溶液中存在的离子是___________ (填离子符号),向其中滴加___________ (填化学式)溶液既能降低该溶液的酸性又能生成沉淀。
(4)将碳酸钠溶液滴加到图3溶液中,现象是___________ ,若将硝酸钾溶液滴加到图3溶液中现象是___________ 。
【归纳小结】
(5)复分解反应发生的条件是___________ 。

(1)图1是向滴有酚酞试剂的氢氧化钠溶液中滴加稀盐酸的微观示意图,该反应过程没有变化的微粒是
(2)图2向氢氧化钠溶液中滴加硫酸铜溶液的微观示意图,其反应的化学方程式是
(3)图3是硫酸氢钠在水中解离的微观示意图,溶液中存在的离子是
(4)将碳酸钠溶液滴加到图3溶液中,现象是
【归纳小结】
(5)复分解反应发生的条件是
您最近一年使用:0次



