利用海洋资源是我们国家建设海洋强国的必然需要。
(1)①海水晒盐的基本原理为______ (填"蒸发"或"降温")结晶。
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质可加下了物质,利用过建等操作进行除杂,则加入下列三种物质的先后顺序为______ (填字母序号)。
A.适量的盐酸
B.稍过量的Na2CO3溶液
C.稍过量的Ba(OH)2溶液
③加入过量的Na2CO3溶液的目的是______ 。
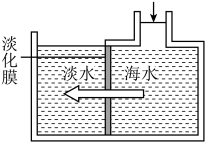
(2)海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过谈化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是______(填选项序号)。
(3)海水制镁的工艺流程如图。

其中发生的中和反应的化学方程式为______ 。
(4)海水制碱:我国著名制碱专家侯德榜创立“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如下:
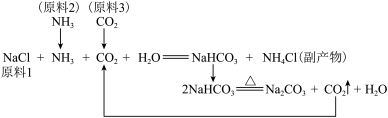
①由上图可知制碱过程中可以循环利用的物质是______ ,产物中可作氮肥的是______ 。
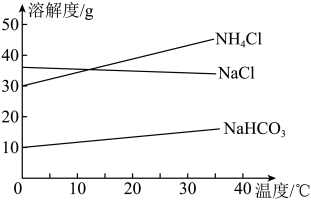
②产物中NaHCO3比NH4Cl先结晶析出。请结合生产原理及如图解释其原因:______ (共答两条)。
(1)①海水晒盐的基本原理为
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质可加下了物质,利用过建等操作进行除杂,则加入下列三种物质的先后顺序为
A.适量的盐酸
B.稍过量的Na2CO3溶液
C.稍过量的Ba(OH)2溶液
③加入过量的Na2CO3溶液的目的是
(2)海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过谈化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是______(填选项序号)。

| A.溶质质量减少 | B.溶剂质量减少 | C.溶液质量减少 | D.溶质质量分数减小 |
(3)海水制镁的工艺流程如图。

其中发生的中和反应的化学方程式为
(4)海水制碱:我国著名制碱专家侯德榜创立“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如下:

①由上图可知制碱过程中可以循环利用的物质是
②产物中NaHCO3比NH4Cl先结晶析出。请结合生产原理及如图解释其原因:

更新时间:2022-05-25 20:10:46
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A~I九种物质均为初中化学常见物质。它们存在如图所示的转化关系,“→”表示可以向箭头所指方向一步转化,“—”表示两种物质之间可以发生反应(反应条件与某些生成物均已略去)。其中A广泛用于玻璃、造纸、纺织和洗涤剂的生产等。E为胃酸中含有的一种酸。H为有毒的气体。A和B反应生成C和D;H和I反应生成G和F.请回答下列问题:
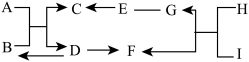
(1)请写出H物质的化学式:______ ;
(2)请写出D生成B的化学方程式:______ 。

(1)请写出H物质的化学式:
(2)请写出D生成B的化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A-E均为初中化学常见的物质,都含有形成化合物种类最多的元素,A是一种难溶性盐,其金属元素含量为40%,C、E组成元素相同。它们之间的关系如下图所示(“→”表示转化关系,涉及反应为初中化学常见反应),请回答下列问题:

(1)D在生产生活中的用途_______ 。
(2)B转化为A的化学方程式为___________________ 。
(3)C转化为E的化学方程式为___________________ 。

(1)D在生产生活中的用途
(2)B转化为A的化学方程式为
(3)C转化为E的化学方程式为
您最近一年使用:0次
【推荐1】海洋是重要的资源宝库,人们正在从海洋中获取大量资源。

(1)海水淡化:下列方法中能淡化海水的是______(填字母序号)。
(2)海水晒盐:利用________ 原理可以获得粗盐。
(3)海水制碱:
①步骤Ⅲ中先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是氨气溶于水显碱性可提高二氧化碳的吸收率,请写出该步骤的化学方程式________ 。
②我国化学家侯德榜创立的联合制碱法的优点有________ (填字母序号)。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作氮肥
(4)海水提镁:
①提取氯化镁历经V、Ⅵ两步转换的目的是________ 。
②请写出第Ⅶ步中,电解熔融状态的MgCl2制取Mg的化学方程式________ 。

(1)海水淡化:下列方法中能淡化海水的是______(填字母序号)。
| A.过滤法 | B.分解法 | C.多级闪急蒸馏法 | D.膜法 |
(2)海水晒盐:利用
(3)海水制碱:
①步骤Ⅲ中先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是氨气溶于水显碱性可提高二氧化碳的吸收率,请写出该步骤的化学方程式
②我国化学家侯德榜创立的联合制碱法的优点有
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作氮肥
(4)海水提镁:
①提取氯化镁历经V、Ⅵ两步转换的目的是
②请写出第Ⅶ步中,电解熔融状态的MgCl2制取Mg的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海水蕴藏着丰富的海洋资源,某兴趣小组设计的综合利用海水的部分流程图如下。
据图回答:

(1)海水制镁。步骤①制氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是__________ 。
(2)海水晒盐。通常采用__________ (填“降温”或“蒸发”)结晶的方法使海水中氯化钠析出。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是________ 。
(3)海水制碱。步骤⑥⑦是氨碱法制纯碱的流程,步骤⑥中需要向NaCl饱和溶液中先后通入的两种物质是_________ (写化学式)。步骤⑦中发生反应的化学方程式是_________ 。
据图回答:

(1)海水制镁。步骤①制氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是
(2)海水晒盐。通常采用
(3)海水制碱。步骤⑥⑦是氨碱法制纯碱的流程,步骤⑥中需要向NaCl饱和溶液中先后通入的两种物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】海水是资源的宝库,海水淡化可获得淡水和浓海水。浓海水中主要离子的浓度如下:
从浓海水中提取金属镁的一段工艺流程如图所示:
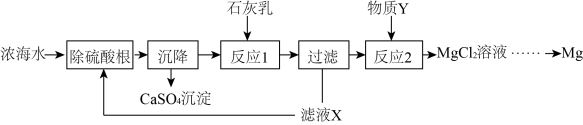
(1)可用______ 鉴别海水是硬水还是软水。
(2)写出由贝壳(主要成分为碳酸钙)生产石灰乳的相应转化中的化学方程式:
贝壳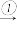 生石灰
生石灰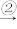 石灰乳
石灰乳
①______ ;②______ 。
(3)流程中用石灰乳而不使用澄清石灰的原因是______ 。
(4)写出流程中“反应2”的化学方程式:______ 。
(5)上述流程中可循环利用的阳离子是______ (填写符号)。
| 离子 | Na+ | Mg2+ | Cl﹣ |  |
| 浓度/(g/L) | 63.7 | 28.8 | 144.6 | 46.4 |

(1)可用
(2)写出由贝壳(主要成分为碳酸钙)生产石灰乳的相应转化中的化学方程式:
贝壳
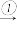 生石灰
生石灰 石灰乳
石灰乳①
(3)流程中用石灰乳而不使用澄清石灰的原因是
(4)写出流程中“反应2”的化学方程式:
(5)上述流程中可循环利用的阳离子是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】海洋是一个巨大的资源库。例如,利用海水可以提取食盐,也可以从海水中提取用途广泛的金属镁和溴,其制取工艺流程如下:
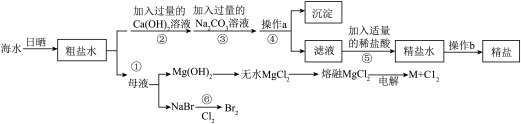
(1)粗盐提纯过程中操作b的名称是:______ ;
(2)写出⑥化学方程式______
(3)如果将步骤②和步骤③的顺序颠倒,则所制得的精盐水中还含有______ 。
(4)在提取镁的流程中,电解氯化镁时产生的Cl2具有强氧化性和剧毒,但在本工业流程中却得到充分应用,极大降低生产成本和减少污染,请写出本工业流程中利用Cl2其中一点:______ 。

(1)粗盐提纯过程中操作b的名称是:
(2)写出⑥化学方程式
(3)如果将步骤②和步骤③的顺序颠倒,则所制得的精盐水中还含有
(4)在提取镁的流程中,电解氯化镁时产生的Cl2具有强氧化性和剧毒,但在本工业流程中却得到充分应用,极大降低生产成本和减少污染,请写出本工业流程中利用Cl2其中一点:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】从海水得到的粗盐,往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须分离和提纯后才能用于工业生产和人们的日常生活。粗盐提纯的部分流程如图:
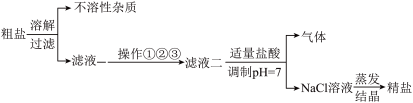
其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠,除去滤液中的Ca2+;
操作②:加入过量的X,除去滤液中的Mg2+;
操作③:加入过量的氯化钡,除去滤液中的 。
。
请回答:
(1)操作中的物质X为_________ ,正确的操作顺序为_________ (填序号),
(2)为最终获得精盐,操作①、②和③后还需增加的操作是_________ 。

其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠,除去滤液中的Ca2+;
操作②:加入过量的X,除去滤液中的Mg2+;
操作③:加入过量的氯化钡,除去滤液中的
 。
。请回答:
(1)操作中的物质X为
(2)为最终获得精盐,操作①、②和③后还需增加的操作是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐1】工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:

(1)在①〜③三个过程中,发生分解反应的是_____ (填序号)。
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①在t1℃时,Na2CO3的溶解度是____ g。
②t2℃时,NaCl的溶解度___ Na2CO3的溶解度(填“大于”“等于”“小于”之一)。
③要从海水中提取NaCl,应采用的方法是___ (填“蒸发结晶”或“降温结晶”)。
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是__ g。

(1)在①〜③三个过程中,发生分解反应的是
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①在t1℃时,Na2CO3的溶解度是
②t2℃时,NaCl的溶解度
③要从海水中提取NaCl,应采用的方法是
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋是巨大的资源宝库。学习小组模拟化工厂生产流程,利用海水制取纯碱和金属镁,设计方案如图所示。请回答下列问题:

(1)流程Ⅰ为海水“晒盐”:由海水获得粗盐的结晶方法是______ 。
(2)流程Ⅱ为粗盐精制:粗盐中通常含有泥沙等难溶性杂质和Ca2+、Mg2+、 等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解并依次加入下列试剂,流程如下:过量NaOH溶液→过量BaCl2溶液→a→过滤→向滤液中加适量稀盐酸→蒸发结晶。
等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解并依次加入下列试剂,流程如下:过量NaOH溶液→过量BaCl2溶液→a→过滤→向滤液中加适量稀盐酸→蒸发结晶。
上述除杂过程中,a是____ 溶液。
(3)流程Ⅲ为海水“制碱”:滤液A中碳酸氢钠是否饱和?____ (填“是”或“否”),流程Ⅲ中循环利用的物质X是____ (填写化学式)。
(4)母液中本来就有氯化镁,不直接进行电解来制取金属镁,而是经过了加石灰乳、盐酸等过程,这样做的目的是______ 。

(1)流程Ⅰ为海水“晒盐”:由海水获得粗盐的结晶方法是
(2)流程Ⅱ为粗盐精制:粗盐中通常含有泥沙等难溶性杂质和Ca2+、Mg2+、
 等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解并依次加入下列试剂,流程如下:过量NaOH溶液→过量BaCl2溶液→a→过滤→向滤液中加适量稀盐酸→蒸发结晶。
等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解并依次加入下列试剂,流程如下:过量NaOH溶液→过量BaCl2溶液→a→过滤→向滤液中加适量稀盐酸→蒸发结晶。上述除杂过程中,a是
(3)流程Ⅲ为海水“制碱”:滤液A中碳酸氢钠是否饱和?
(4)母液中本来就有氯化镁,不直接进行电解来制取金属镁,而是经过了加石灰乳、盐酸等过程,这样做的目的是
您最近一年使用:0次


 ”代表的离子是
”代表的离子是

