早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺,其中氢氧化钾(KOH)是用氢氧化钙和草木灰(主要成分是碳酸钾)反应制备而成的。某同学运用上述反应原理,将一定质量的氢氧化钙固体加入202.6g碳酸钾溶液中,恰好完全反应,生成10g沉淀,并得到氢氧化钾的不饱和溶液。
(1)工业上生产氢氧化钙,常用_____ (填物质的俗称)和水反应制得。
(2)与反应前的碳酸钾溶液相比,反应后溶液中显著减少的离子是_____ (填离子符号)。
(3)计算加入的氢氧化钙的质量_____ 。(写出计算过程)
(4)若反应结束后,过滤时对沉淀未进行洗涤,则(3)中的计算结果比实际结果____ (选填“偏大”、“偏小”或“不变”),反应后溶液中氢氧化钾的质量分数是______ 。
(1)工业上生产氢氧化钙,常用
(2)与反应前的碳酸钾溶液相比,反应后溶液中显著减少的离子是
(3)计算加入的氢氧化钙的质量
(4)若反应结束后,过滤时对沉淀未进行洗涤,则(3)中的计算结果比实际结果
2022·江西·模拟预测 查看更多[1]
更新时间:2022-06-10 17:05:11
|
相似题推荐
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】提出问题:蛋壳中的 含量是多少呢?称取
含量是多少呢?称取  蛋壳设计了以下的实验方案如图所示的实验装置。
蛋壳设计了以下的实验方案如图所示的实验装置。

【实验步骤】
 按如图连接好装置后,并
按如图连接好装置后,并 ______ ;
 向B装置中加入蛋壳样品后,先通入空气一会儿;
向B装置中加入蛋壳样品后,先通入空气一会儿;
 接下来的实验操作是
接下来的实验操作是 ______ ,直到 ______ 为止 填实验现象
填实验现象 ;
;
 再通入空气一会儿,至装置C中不再产生沉淀为止;
再通入空气一会儿,至装置C中不再产生沉淀为止;
 将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;
将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;  重复上述实验。
重复上述实验。
【实验数据】重复实验,3次数据记录如下:
【实验分析及数据处理】
 上述数据能否用托盘天平称量
上述数据能否用托盘天平称量 ______ 。 填“能”或“不能”
填“能”或“不能”
 若无A装置,直接通入空气,则测定结果将
若无A装置,直接通入空气,则测定结果将 ______ 。 填“偏大”、“偏小”或“不变”
填“偏大”、“偏小”或“不变” 装置的作用是
装置的作用是 ______ 。
 实验重复3次的目的是
实验重复3次的目的是 ______ 。
 请利用3次实验数据的平均值,计算该蛋壳中的
请利用3次实验数据的平均值,计算该蛋壳中的 质量分数是
质量分数是 ______ 。 写出计算过程
写出计算过程
 含量是多少呢?称取
含量是多少呢?称取  蛋壳设计了以下的实验方案如图所示的实验装置。
蛋壳设计了以下的实验方案如图所示的实验装置。
【实验步骤】
 按如图连接好装置后,并
按如图连接好装置后,并  向B装置中加入蛋壳样品后,先通入空气一会儿;
向B装置中加入蛋壳样品后,先通入空气一会儿; 接下来的实验操作是
接下来的实验操作是  填实验现象
填实验现象 ;
; 再通入空气一会儿,至装置C中不再产生沉淀为止;
再通入空气一会儿,至装置C中不再产生沉淀为止; 将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;
将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;  重复上述实验。
重复上述实验。【实验数据】重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量 |  |  |  |
 上述数据能否用托盘天平称量
上述数据能否用托盘天平称量  填“能”或“不能”
填“能”或“不能”
 若无A装置,直接通入空气,则测定结果将
若无A装置,直接通入空气,则测定结果将  填“偏大”、“偏小”或“不变”
填“偏大”、“偏小”或“不变” 装置的作用是
装置的作用是  实验重复3次的目的是
实验重复3次的目的是  请利用3次实验数据的平均值,计算该蛋壳中的
请利用3次实验数据的平均值,计算该蛋壳中的 质量分数是
质量分数是  写出计算过程
写出计算过程
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】学习化学近半年,同学们学会了由现象到性质、由宏观到微观、由定性到定量多角度认识化学变化。
(1)某课外小组做如图这一组对比实验,该对比实验得出的结论是_______。(填写正确选项的序号)
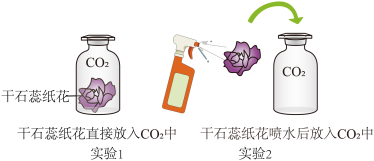
①CO2密度比空气密度大
②CO2能够与水发生化学反应
③CO2不能使干石蕊纸花变色
④CO2不支持燃烧
(2)下图是某反应的微观示意图(其中“○”和“●”分别表示氧原子和氢原子)
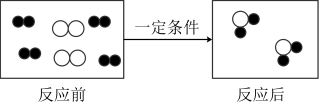
①“反应后”图示中应再填入_______ 个“ ”微粒;
”微粒;
②请写出此反应的化学方程式_______ 。
(3)随着科学研究的进展,化学实验也从定性到定量,发生了质的转变,若按实验方法分类,应将实验C与实验_______ (填A或B或D)为一类,分类依据是_______ 。
A. B.
B. C.
C.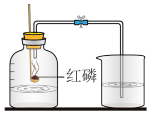 D.
D. 
(4)质量守恒定律是化学由定性走向定量的第一步,根据图回答问题:
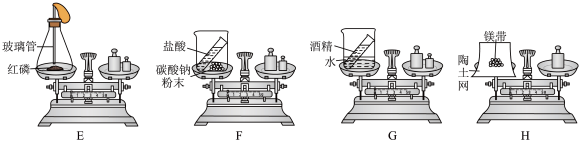
资料: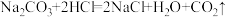
①如图E、F、G三个实验的变化中,遵守质量守恒定律的是_______ (填序号)。
②用图F实验来验证质量守恒定律时,若所用试剂不变,你的改进方案是_______ 。
③H装置中利用镁带在空气中燃烧来验证质量守恒定律。
2.4g镁完全燃烧生成氧化镁的质量是______ g。小明认为根据质量守恒定律,天平应该向左倾斜。镁带完全燃烧后,发现天平向右倾斜,请分析其主要原因是_______ 。分析上述宏观实验可知一切化学变化都遵守质量守恒定律的微观原因是_______ 。
(1)某课外小组做如图这一组对比实验,该对比实验得出的结论是_______。(填写正确选项的序号)

①CO2密度比空气密度大
②CO2能够与水发生化学反应
③CO2不能使干石蕊纸花变色
④CO2不支持燃烧
| A.①② | B.②③ | C.③④ | D.①④ |
(2)下图是某反应的微观示意图(其中“○”和“●”分别表示氧原子和氢原子)

①“反应后”图示中应再填入
 ”微粒;
”微粒;②请写出此反应的化学方程式
(3)随着科学研究的进展,化学实验也从定性到定量,发生了质的转变,若按实验方法分类,应将实验C与实验
A.
 B.
B. C.
C. D.
D. 
(4)质量守恒定律是化学由定性走向定量的第一步,根据图回答问题:

资料:
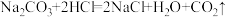
①如图E、F、G三个实验的变化中,遵守质量守恒定律的是
②用图F实验来验证质量守恒定律时,若所用试剂不变,你的改进方案是
③H装置中利用镁带在空气中燃烧来验证质量守恒定律。
2.4g镁完全燃烧生成氧化镁的质量是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】锰( )是维持人体正常生命活动所必须的微量元素。锰及其化合物在生产生活中有广泛的应用。
)是维持人体正常生命活动所必须的微量元素。锰及其化合物在生产生活中有广泛的应用。
(一)锰元素
(1)结构:图为锰原子结构示意图及在元素周期表中的信息。下列说法正确的是______。
(2)单质的活动性:
①已知金属锰可从酸溶液中置换出 ,产物中锰元素的化合价为
,产物中锰元素的化合价为 价,则锰和稀硫酸反应的化学方程式为
价,则锰和稀硫酸反应的化学方程式为_______ 。
②欲验证铁、铜、锰三种金属的活动性强弱为: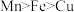 ,可设计的实验方案为
,可设计的实验方案为_______ 。(可选择试剂: 溶液、
溶液、 溶液、
溶液、 片、
片、 片、
片、 片)
片)
(3)含锰合金:
锰钢是铁、锰、碳的合金,可用来制造钢轨。钢轨的制造与应用主要体现了锰钢具有的性质有_____。
(二)含锰化合物的应用 为紫红色。用如图1所示装置电解
为紫红色。用如图1所示装置电解 溶液,一段时间后,U型管两端溶液颜色有明显差异,其原因是
溶液,一段时间后,U型管两端溶液颜色有明显差异,其原因是_______ 。
(5)某研究小组采用图2装置通过焙烧 制取
制取 ,发生反应的化学方程式为:
,发生反应的化学方程式为: 。
。
①焙烧过程中产生的气体不含锰元素。X的化学式为_______ 。从 升高到
升高到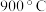 过程中,剩余固体含锰元素的质量分数逐渐
过程中,剩余固体含锰元素的质量分数逐渐_______ (填“增大”或“减少”)。
②在实验室中,焙烧 ,最多可获得
,最多可获得 的质量是
的质量是_______ 。(写出计算过程)
 )是维持人体正常生命活动所必须的微量元素。锰及其化合物在生产生活中有广泛的应用。
)是维持人体正常生命活动所必须的微量元素。锰及其化合物在生产生活中有广泛的应用。(一)锰元素
(1)结构:图为锰原子结构示意图及在元素周期表中的信息。下列说法正确的是______。

| A.图中X的数值为18 |
| B.锰元素的原子序数为25 |
| C.锰原子在化学变化中得到电子 |
| D.锰元素对人体健康具有重要意义 |
(2)单质的活动性:
①已知金属锰可从酸溶液中置换出
 ,产物中锰元素的化合价为
,产物中锰元素的化合价为 价,则锰和稀硫酸反应的化学方程式为
价,则锰和稀硫酸反应的化学方程式为②欲验证铁、铜、锰三种金属的活动性强弱为:
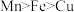 ,可设计的实验方案为
,可设计的实验方案为 溶液、
溶液、 溶液、
溶液、 片、
片、 片、
片、 片)
片)(3)含锰合金:
锰钢是铁、锰、碳的合金,可用来制造钢轨。钢轨的制造与应用主要体现了锰钢具有的性质有_____。
| A.导热性 | B.导电性 | C.硬度大 | D.有光泽 |
(二)含锰化合物的应用


 为紫红色。用如图1所示装置电解
为紫红色。用如图1所示装置电解 溶液,一段时间后,U型管两端溶液颜色有明显差异,其原因是
溶液,一段时间后,U型管两端溶液颜色有明显差异,其原因是(5)某研究小组采用图2装置通过焙烧
 制取
制取 ,发生反应的化学方程式为:
,发生反应的化学方程式为: 。
。①焙烧过程中产生的气体不含锰元素。X的化学式为
 升高到
升高到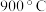 过程中,剩余固体含锰元素的质量分数逐渐
过程中,剩余固体含锰元素的质量分数逐渐②在实验室中,焙烧
 ,最多可获得
,最多可获得 的质量是
的质量是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】我国的海岸线长达3.2万千米,海洋专属经济区幅员辽阔,海洋资源丰富,开发前景十分远大。
(1)海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水,海水晒盐利用了___________ (填“蒸发结晶”“降温结晶”之一)的原理。
(2)镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”。下图为从海水或卤水中制取单质镁的转化过程,试回答下列问题:

①所加石灰乳的主要成分是___________ (填化学式)。
②海水或卤水中本来就含有MgCl2,为什么还要加入石灰乳、稀盐酸来制取MgCl2,这样做的目的是___________ 。
③小雪同学在实验室进行海水提取氯化镁的模拟实验,在过滤操作中使用了玻璃棒,其作用是___________ 。
④流程图中发生分解反应的化学方程式为___________ 。
(3)同学取100g某氯化镁溶液于一只洁净的烧杯中,然后逐滴加入溶质质量分数为10%的NaOH溶液至过量,烧杯内溶液的质量与加入NaOH溶液的质量关系如图所示。试回答:

①当滴入NaOH溶液46g时(即图中A点),烧杯中溶液里大量存在的金属阳离子是___________ (填离子符号)。
②当滴入10%的NaOH溶液80g时(即B点)恰好完全反应,试通过计算,求该氯化镁溶液的溶质质量分数(计算结果精确至0.1%)。
(1)海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水,海水晒盐利用了
(2)镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”。下图为从海水或卤水中制取单质镁的转化过程,试回答下列问题:

①所加石灰乳的主要成分是
②海水或卤水中本来就含有MgCl2,为什么还要加入石灰乳、稀盐酸来制取MgCl2,这样做的目的是
③小雪同学在实验室进行海水提取氯化镁的模拟实验,在过滤操作中使用了玻璃棒,其作用是
④流程图中发生分解反应的化学方程式为
(3)同学取100g某氯化镁溶液于一只洁净的烧杯中,然后逐滴加入溶质质量分数为10%的NaOH溶液至过量,烧杯内溶液的质量与加入NaOH溶液的质量关系如图所示。试回答:

①当滴入NaOH溶液46g时(即图中A点),烧杯中溶液里大量存在的金属阳离子是
②当滴入10%的NaOH溶液80g时(即B点)恰好完全反应,试通过计算,求该氯化镁溶液的溶质质量分数(计算结果精确至0.1%)。
您最近一年使用:0次
【推荐2】硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性。实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeSO4。

(1)在右图中,应选用图________ 作为制取H2S的装置。
(2)收集H2S气体时,应从C装置中的_________ 导管进入,对产生尾气的处理方法
是:________ 。
(3)实验室若制取6.8克的硫化氢气体,理论上需要多少克20%的硫酸溶液?_______

(1)在右图中,应选用图
(2)收集H2S气体时,应从C装置中的
是:
(3)实验室若制取6.8克的硫化氢气体,理论上需要多少克20%的硫酸溶液?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】《石灰吟》是明代文学家于谦创作的一首七言绝句,全诗内容如下:“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间。”全诗所涉及的化学反应用流程图表示如下:

(1)过程①所发生的反应属于_______ 反应(填“化合”“分解”“置换”“复分解”之一)。
(2)写出过程③的化学方程式________________ 。
(3)上述过程所涉及的物质中经常用作干燥剂的是________ (填化学式)。
(4)为制取氢氧化钠,取一定质量的步骤②所得石灰乳,向其中滴入质量分数为10.6%的Na2CO3溶液,使其充分反应。加入Na2CO3溶液的质量和所得沉淀的质量关系如下图所示:

①当滴入10.6%的碳酸钠溶液至图中B点时,溶液中的溶质有______________ (填化学式)。
②计算恰好完全反应(至图中A点)时所得氢氧化钠的质量。(计算结果精确至0.1 g)____

(1)过程①所发生的反应属于
(2)写出过程③的化学方程式
(3)上述过程所涉及的物质中经常用作干燥剂的是
(4)为制取氢氧化钠,取一定质量的步骤②所得石灰乳,向其中滴入质量分数为10.6%的Na2CO3溶液,使其充分反应。加入Na2CO3溶液的质量和所得沉淀的质量关系如下图所示:

①当滴入10.6%的碳酸钠溶液至图中B点时,溶液中的溶质有
②计算恰好完全反应(至图中A点)时所得氢氧化钠的质量。(计算结果精确至0.1 g)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】有限的元素可组成种类繁多的物质,依据表中的元素回答下列问题。
(1)中国科学院院士_____在相对原子质量的测定做出了杰出贡献。
(2)我国实施“西气东输”计划,输出的气体的名称为_____ 。
(3)社会上有一些不法商贩利用黄铜(铜、锌合金)制作假黄金首饰牟取暴利,可用_____ (填化学式)的溶液鉴别真假黄金。
(4)为了节约石油资源,可向汽油中加入一定量酒精,写出酒精燃烧的化学方程式_____ 。
(5)A、B、C、D都是由上述元素组成的不同类别的初中常见物质,其中B物质可做建筑材料,D物质可用于配制具有杀菌作用的波尔多液,图中“—”表示两端物质可以反应,“→”表示物质间的转化关系(注:转化过程中所涉及到的物质均要求由上表中的元素组成),部分反应物、生成物及反应条件已略去。下列说法正确的是(不定项选择,填序号)_____ 。

a.D溶液一定显蓝色
b.物质B一定是盐
c.物质A一定是硫酸
d.物质C一定可以引起温室效应
| 元素名称 | 氢 | 碳 | 氧 | 钙 | 硫 | 铜 |
| 元素符号 | H | C | O | Ca | S | Cu |
| A.屠呦呦 | B.门捷列夫 | C.张青莲 | D.道尔顿 |
(3)社会上有一些不法商贩利用黄铜(铜、锌合金)制作假黄金首饰牟取暴利,可用
(4)为了节约石油资源,可向汽油中加入一定量酒精,写出酒精燃烧的化学方程式
(5)A、B、C、D都是由上述元素组成的不同类别的初中常见物质,其中B物质可做建筑材料,D物质可用于配制具有杀菌作用的波尔多液,图中“—”表示两端物质可以反应,“→”表示物质间的转化关系(注:转化过程中所涉及到的物质均要求由上表中的元素组成),部分反应物、生成物及反应条件已略去。下列说法正确的是(不定项选择,填序号)

a.D溶液一定显蓝色
b.物质B一定是盐
c.物质A一定是硫酸
d.物质C一定可以引起温室效应
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】化学用语是学习化学的重要工具。
(1)写出下列微粒的化学符号 :
①2个氖原子_____ ②铵根离子_____ ③五氧化二氮分子_____ ④镁离子_____
(2)用下列字母 填空:
a.氢气 b.小苏打 c.无水氯化钙 d.硝酸钾
①用于做复合肥_____ ②用做干燥剂_____ ③用于发酵粉_____ ④用于做燃料_____
(3)写出下列反应的化学方程式:
①铁在氧气中点燃_____ ②碳铵的受热分解_____
③铁和稀盐酸反应_____ ④硫酸铵和氢氧化钙反应_____
(1)写出下列微粒的
①2个氖原子
(2)用下列
a.氢气 b.小苏打 c.无水氯化钙 d.硝酸钾
①用于做复合肥
(3)写出下列反应的化学方程式:
①铁在氧气中点燃
③铁和稀盐酸反应
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献。
(1)主产品为Na2CO3,它的俗名叫 (填一种),其水溶液呈 性(选填“酸”“碱”“中”)。
(2)在实际生产中,产品Na2CO3中常混有少量的NaCl,现有样品11.0g,将其放入干净的烧杯中,向烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,反应后烧杯中物质的质量与滴入稀盐酸的质量关系如图所示。

①图中B点的溶质为 。(填名称)
④计算恰好完全反应后溶液的溶质质量分数。(计算结果精确至0.1%)
(1)主产品为Na2CO3,它的俗名叫 (填一种),其水溶液呈 性(选填“酸”“碱”“中”)。
(2)在实际生产中,产品Na2CO3中常混有少量的NaCl,现有样品11.0g,将其放入干净的烧杯中,向烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,反应后烧杯中物质的质量与滴入稀盐酸的质量关系如图所示。

①图中B点的溶质为 。(填名称)
④计算恰好完全反应后溶液的溶质质量分数。(计算结果精确至0.1%)
您最近一年使用:0次



