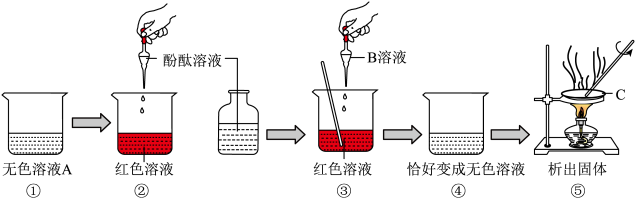
氯化钙可用作混凝土防冻剂等。某兴趣小组利用硬水受热后产生的水垢(水垢的主要成分是碳酸钙和氢氧化镁,其他成分不参与反应),来制取纯净的氯化钙固体,具体流程如下:

(1)生活中软化硬水最常见的方法是______ 。
(2)向水垢中加入过量的盐酸时,属于中和反应的化学方程式为______ ,所得溶液A中的溶质除了氯化钙、氯化镁之外,还有______ (填化学式)。
(3)操作Ⅱ的名称为______ ;产生沉淀C的化学方程式为______ 。
(4)溶液B转化为D时,所发生化学反应的基本反应类型为______ 。
(5)操作Ⅲ的名称为蒸发,操作中玻璃棒的作用是______ 。

(1)生活中软化硬水最常见的方法是
(2)向水垢中加入过量的盐酸时,属于中和反应的化学方程式为
(3)操作Ⅱ的名称为
(4)溶液B转化为D时,所发生化学反应的基本反应类型为
(5)操作Ⅲ的名称为蒸发,操作中玻璃棒的作用是
更新时间:2022-06-17 22:00:34
|
相似题推荐
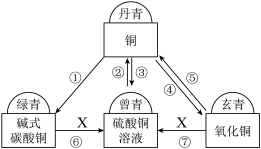
【推荐1】2023年春晚的《满庭芳·国色》节目点燃了国人复古寻色的热潮。小明同学以“青”为线构建铜及其化合物的知识结构图。______ 、氧气和水同时接触。
(2)“绿青”“玄青”分别与同种物质X充分反应可转化为“曾青”,X物质的化学式为______ ,反应⑦的实验现象是______ ,其基本反应类型为______ 反应。
(3)农业上可用______ (填化学式)与“曾青”等配制成具有杀菌作用的波尔多液。
(4)“丹青”和“玄青”可以相互转化,④⑤两个变化的共同点是______ (填序号)。
a.相同的基本反应类型 b.都有元素化合价发生变化
(2)“绿青”“玄青”分别与同种物质X充分反应可转化为“曾青”,X物质的化学式为
(3)农业上可用
(4)“丹青”和“玄青”可以相互转化,④⑤两个变化的共同点是
a.相同的基本反应类型 b.都有元素化合价发生变化
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A~D是我们学习的常见物质,其中A是红色固体,物质D的俗称为纯碱,已知 A、B、C、D不是酸和碱,它们与稀 H2SO4、Ca(OH)2之间的相互关系如图所示(“→”表示物质间的转化关系,“—”表示物质间可以相互反应)。

请回答下列问题:
(1)H2SO4与 Ca(OH)2反应的实质是______ 结合成水分子,反应基本类型是______ 。
(2)写出下列反应编号②的化学方程式:______ 。
(3)若①是工业冶炼生铁的主要反应,则该反应的化学方程式是______ 。

请回答下列问题:
(1)H2SO4与 Ca(OH)2反应的实质是
(2)写出下列反应编号②的化学方程式:
(3)若①是工业冶炼生铁的主要反应,则该反应的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某工厂生产硫酸的过程中产生的炉渣,主要成分为Fe2O3、SiO2、FeO和锰的氧化物等。现以该炉渣为原料制备铁红(Fe2O3)的生产流程如图所示:

【已知:SiO2不溶于水,也不与稀硫酸反应】
(1)操作1的名称是_______ ,滤渣a的主要成分是_______ (写化学式)。
(2)步骤①中,硫酸与Fe2O3反应的化学方程式为_______ ,该反应属于_______ 反应(填基本反应类型)。
(3)步骤②中,使用足量H2O2的目的是_______ 。
(4)步骤③中,几种金属离子开始沉淀和完全沉淀时的pH如表所示:
要使Fe3+完全沉淀为Fe(OH)3,从而与Mn2+分离,则调节pH的最大范围是:_______ ≤pH<8.1。
(5)写出步骤④中反应的化学方程式_______ 。

【已知:SiO2不溶于水,也不与稀硫酸反应】
(1)操作1的名称是
(2)步骤①中,硫酸与Fe2O3反应的化学方程式为
(3)步骤②中,使用足量H2O2的目的是
(4)步骤③中,几种金属离子开始沉淀和完全沉淀时的pH如表所示:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 |
(5)写出步骤④中反应的化学方程式
您最近一年使用:0次
【推荐1】人类的日常生活和工农业生产离不开水,请回答:
(1)水______ (填“属于”或“不属于”)人类所需的六大基本营养素之一。
(2)含有较多可溶性钙、镁化合物的水叫做______ (填“软水“或“硬水”)。
(3)能说明水是由氧元素和氢元素组成的实验是______ (填序号)。
A通电分解水B水的净化C氢气在氧气中燃烧
(4)如图是A、B、C三种固体物质的溶解度曲线,据图回答:

①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是______ (填写字母序号)。
②t1℃时,将30gA物质加入到50g水中不断搅拌,形成的溶液质量为______ g。
③将t1℃时,A、B、C三种物质饱和溶液的温度升高到t2℃,此时这三种溶液的溶质质量分数由大到小的关系是______ 。
④t1℃时,A物质中含有少量的B物质,提纯A的方法是______ 。
⑤t2℃时,等质量的A、B、C三种物质形成饱和溶液,其溶液的质量由大到小的顺序是_______ 。
(1)水
(2)含有较多可溶性钙、镁化合物的水叫做
(3)能说明水是由氧元素和氢元素组成的实验是
A通电分解水B水的净化C氢气在氧气中燃烧
(4)如图是A、B、C三种固体物质的溶解度曲线,据图回答:

①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是
②t1℃时,将30gA物质加入到50g水中不断搅拌,形成的溶液质量为
③将t1℃时,A、B、C三种物质饱和溶液的温度升高到t2℃,此时这三种溶液的溶质质量分数由大到小的关系是
④t1℃时,A物质中含有少量的B物质,提纯A的方法是
⑤t2℃时,等质量的A、B、C三种物质形成饱和溶液,其溶液的质量由大到小的顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】水是人类重要的自然资源,人类的生活、生产都离不开水.

(1)自来水厂(如图甲)利用沉淀、过滤、_________ 和消毒等方法净化水.在实验室进行过滤操作时,需要用到的玻璃仪器有玻璃棒、烧杯、_________ 。
(2)取某小区等量的自来水和直饮水(如图乙),分别加入_________ 并搅拌,发现直饮水中有大量泡沫,没有浮渣,自来水中泡沫少且有浮渣,说明直饮水的硬度较_________ (填“大”或“小”)。
(3)生活中硬水会带来许多麻烦,家庭生活中既能降低水的硬度,又可以杀菌消毒的方法是_________ 。
(4)某同学用电解水的方法探究水的组成,按图丙所示装置进行实验.电解时,该反应的表达式为_________ 此装置中a管产生的气体名称是_________ ,已知在相同条件下氧气在水中的溶解性强于氢气,那么,在a、b两玻璃管中气体的体积比的测定结果比2:1略_________ (填“小”或“大”)。

(1)自来水厂(如图甲)利用沉淀、过滤、
(2)取某小区等量的自来水和直饮水(如图乙),分别加入
(3)生活中硬水会带来许多麻烦,家庭生活中既能降低水的硬度,又可以杀菌消毒的方法是
(4)某同学用电解水的方法探究水的组成,按图丙所示装置进行实验.电解时,该反应的表达式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐3】人类的生产和生活都离不开水。下图是自来水厂净水过程示意图。
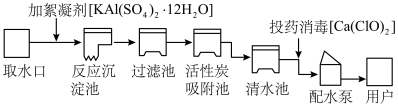
请根据示意图回答下列问题:
(1)自来水厂生产自来水时,不会使用的净水方法有___________ ;(写字母)
(2)水中Al3+超标有害健康,可能造成自来水Al3+超标的操作是_______________ ;
(3)家庭最常用的降低水硬度的方法是______________ ;
(4)每一滴水都来之不易,列举一条生活中具体可行的节水措施___________________________ 。

请根据示意图回答下列问题:
(1)自来水厂生产自来水时,不会使用的净水方法有
| A.沉淀 | B.过滤 | C.吸附 | D.蒸馏 |
(2)水中Al3+超标有害健康,可能造成自来水Al3+超标的操作是
(3)家庭最常用的降低水硬度的方法是
(4)每一滴水都来之不易,列举一条生活中具体可行的节水措施
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】稀硫酸与氢氧化钠溶液反应时没有明显现象,为证明反应确实发生了,实验小组同学进行了如下实验,将稀硫酸慢慢滴入装有氢氧化钠稀溶液的烧杯中,利用温度传感器测出烧杯中溶液的温度随稀硫酸滴加量的变化曲线如图。

(1)A到B过程中溶液的pH将____________ (填“变大”、“变小”或“不变”);
(2)曲线说明该反应是放热反应,则B点后溶液温度下降的原因是什么?______ 。
(3)写出C点时溶液中含有离子的符号:______ 。

(1)A到B过程中溶液的pH将
(2)曲线说明该反应是放热反应,则B点后溶液温度下降的原因是什么?
(3)写出C点时溶液中含有离子的符号:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】回答问题:
食盐样品中含有少量沙土、氯化钙和氯化镁。某同学思考后按以下流程除去食盐样品中的沙土、氯化钙和氯化镁,请根据流程图回答:

(1)操作Ⅰ是___________ 。
(2)试剂A是___________ (写名称)。
(3)加入试剂B后发生中和反应的化学方程式为___________ 。
食盐样品中含有少量沙土、氯化钙和氯化镁。某同学思考后按以下流程除去食盐样品中的沙土、氯化钙和氯化镁,请根据流程图回答:

(1)操作Ⅰ是
(2)试剂A是
(3)加入试剂B后发生中和反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组三位同学在学习了稀硫酸与氢氧化钠溶液反应后,分别结合自己在实验室中所做的实验,从不同方面对其进行图像描述。
图A是实际操作图,图B是反应过程中溶液的酸碱度变化图,图C是微观粒子结合过程的示意图。根据下图所示,回答问题:

(1)依据图A、B图可知,该实验是将______ (填物质名称)滴加到另一种溶液中。
(2)图B中b点溶液中溶质是______ 。
(3)请写出图C中方框内乙粒子的符号______ 。
(4)请写出该实验的反应方程式______ 。
图A是实际操作图,图B是反应过程中溶液的酸碱度变化图,图C是微观粒子结合过程的示意图。根据下图所示,回答问题:

(1)依据图A、B图可知,该实验是将
(2)图B中b点溶液中溶质是
(3)请写出图C中方框内乙粒子的符号
(4)请写出该实验的反应方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】硫酸钠是制造纸浆、燃料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaCl2和MgCl2杂质,实验室进行提纯的流程如图1:


回答下列问题:
(1)用NaOH除杂时,反应的化学方程式为________ ,除杂、过滤后得到的滤渣成分的化学式是________ .
(2)NaOH和Na2CO3如果添加过量了,最好加入适量________ 溶液除去.
(3)“后续处理”的主要操作是蒸发,为了获得较纯净的硫酸钠,应蒸发至_______ (填序号).
A. 完全蒸干时停止加热
B. 快干时停止加热,利用余热蒸干
C. 有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如图2所示.40℃时,100g蒸馏水中约溶解________ g硫酸钠达到饱和.将该饱和溶液升高温度至90℃,观察到的现象是________ .


回答下列问题:
(1)用NaOH除杂时,反应的化学方程式为
(2)NaOH和Na2CO3如果添加过量了,最好加入适量
(3)“后续处理”的主要操作是蒸发,为了获得较纯净的硫酸钠,应蒸发至
A. 完全蒸干时停止加热
B. 快干时停止加热,利用余热蒸干
C. 有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如图2所示.40℃时,100g蒸馏水中约溶解
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】用废黄铜生产硫酸铜晶体(CuSO4•5H2O)的流程如下:

(1)“酸溶”时加入过量稀硫酸的目的是_______ 。
(2)操作1用到的玻璃仪器有烧杯、漏斗、_______ 。
(3)操作2包括:蒸发浓缩、_______ 、过滤、洗涤等。
(4)“转化”时发生的反应方程式为:_______ ,CuO+H2SO4=CuSO4+H2O。

(1)“酸溶”时加入过量稀硫酸的目的是
(2)操作1用到的玻璃仪器有烧杯、漏斗、
(3)操作2包括:蒸发浓缩、
(4)“转化”时发生的反应方程式为:
您最近一年使用:0次