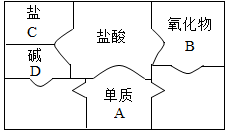
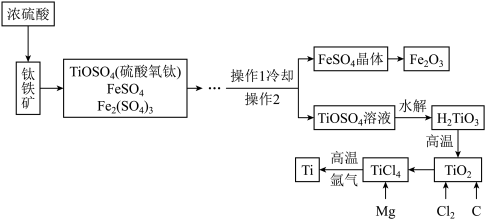
金属钛广泛用于航空航天、工业、化工、医疗等领域。用钛铁矿(主要成分为FeTiO3,同时含有少量的 Fe2O3、FeO等)制取钛并获得副产品Fe2O3的主要工艺流程如图所示:
【查阅资料】钛、镁在高温下易与空气中的氧气、二氧化碳等反应。
请回答下列问题:
(1)构成金属钛的微粒是____ (填“分子”“原子”或“离子”),H2TiO3中钛元素的化合价为____ 。
(2)写出工艺流程中生成硫酸铁的化学方程式:____ 。
(3)工艺流程中,“水解”属于____ (填“化学”或“物理”)变化。
(4)工业上常在高温和氩气环境中,用金属镁和TiCl4反应的方法制备Ti,氩气的作用是____ 。

【查阅资料】钛、镁在高温下易与空气中的氧气、二氧化碳等反应。
请回答下列问题:
(1)构成金属钛的微粒是
(2)写出工艺流程中生成硫酸铁的化学方程式:
(3)工艺流程中,“水解”属于
(4)工业上常在高温和氩气环境中,用金属镁和TiCl4反应的方法制备Ti,氩气的作用是
更新时间:2022-06-29 20:37:05
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】拥有“天蓝、地绿、水净”的美好家园是每个中国人的梦想。
①我们需要洁净的空气。大气中的臭氧(O3)能吸收紫外线,与臭氧互为同素异形体的物质是_______ ,下列不会增加空气中PM2.5的是_______ (填编号)。
A. 露天焚烧垃圾 B. 治理工地扬尘 C. 发展轨道交通,低碳出行
②我们需要清洁的能源。目前人们利用最多的能源是煤、_______ 和天然气等化石燃料。化石燃料不可再生,氢能作为理想的新能源,重要原因是它的燃烧产物无污染,氢气燃烧的化学方程式为_______ 。科学家正在努力开发和利用的新能源除了氢能还有_______ 等(写一个)。
③我们需要洁净的水。FeCl3也可作自来水生产的净水剂。FeCl3中Cl元素为-1价,Fe元素的化合价为_______ ;1mol FeCl3中约含有_______ 个Fe离子(用科学记数法表示)。
①我们需要洁净的空气。大气中的臭氧(O3)能吸收紫外线,与臭氧互为同素异形体的物质是
A. 露天焚烧垃圾 B. 治理工地扬尘 C. 发展轨道交通,低碳出行
②我们需要清洁的能源。目前人们利用最多的能源是煤、
③我们需要洁净的水。FeCl3也可作自来水生产的净水剂。FeCl3中Cl元素为-1价,Fe元素的化合价为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】请用化学用语填空。
(1)由60个碳原子构成的单质分子_____ 。
(2)两个钙离子_____ 。
(3)标出氨气中氮元素的化合价_____ 。
(1)由60个碳原子构成的单质分子
(2)两个钙离子
(3)标出氨气中氮元素的化合价
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】发展利用太阳能可以推进节能减排,晶体硅是制造太阳能电池板的重要原料,如图是工业上以石英砂(SiO2)为主要原料制取纯硅的一种方法,请回答以下问题。

(1)将石英砂粉碎的目的是______ ,石英砂SiO2中Si元素的化合价为______ 。
(2)写出流程②的化学方程式:______ ,流程②要在无氧气的环境中进行,原因是______ 。(答出一种即可)
(3)写出副产品CO的一种用途(用化学方程式表示):______ 。

(1)将石英砂粉碎的目的是
(2)写出流程②的化学方程式:
(3)写出副产品CO的一种用途(用化学方程式表示):
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学就在我们身边,它与我们的生活息息相关 有下列几种物质,请选出与各用途相对应的物质的序号填写在空白处:
有下列几种物质,请选出与各用途相对应的物质的序号填写在空白处:
A铝 B氧气 C二氧化碳 D氖气 E水 F活性炭
(1)供给人类呼吸的气体是___________ ;
(2)可制作电线的物质是___________ ;
(3)可用作霓虹灯的物质是___________ ;
(4)人体中含量最多的物质是___________ ;
(5)可除去水中异味的物质是___________ ;
(6)植物光合作用不可缺少的气体是___________ 。
 有下列几种物质,请选出与各用途相对应的物质的序号填写在空白处:
有下列几种物质,请选出与各用途相对应的物质的序号填写在空白处:A铝 B氧气 C二氧化碳 D氖气 E水 F活性炭
(1)供给人类呼吸的气体是
(2)可制作电线的物质是
(3)可用作霓虹灯的物质是
(4)人体中含量最多的物质是
(5)可除去水中异味的物质是
(6)植物光合作用不可缺少的气体是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学就在我们身边,请从下列物质中选择①氧气②碳酸钙③生石灰④小苏打⑤火碱⑥干冰。按要求填空(填序号):
(1)可用于医疗急救的气体是______ 。
(2)可作食品干燥剂的是______ 。
(3)可用做炉具清洁剂的是______ 。
(4)可用作人工降雨的是______ 。
(5)用做补钙剂的是______ 。
(6)可用于治疗胃酸过多的是______ 。
(1)可用于医疗急救的气体是
(2)可作食品干燥剂的是
(3)可用做炉具清洁剂的是
(4)可用作人工降雨的是
(5)用做补钙剂的是
(6)可用于治疗胃酸过多的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】依据所学知识回答问题
Ⅰ.根据①氦气;②氮气;③木炭;④氧气等物质的性质或用途,填写下列空格(填序号):
(1)空气中含量最多的气体是_______ ;
(2)医疗急救时用到的气体是_______ ;
(3)可填充霓虹灯且通电时会发出有色光的气体是_______ ;
(4)能作燃料的是_______ 。
Ⅱ.我们生活在物质世界中,每天都要接触很多物质,如:
(5)①二氧化碳、②铁粉、③氮气。其中属于化合物物的有________ (填序号,下同),属于单质的有_______ 。
Ⅰ.根据①氦气;②氮气;③木炭;④氧气等物质的性质或用途,填写下列空格(填序号):
(1)空气中含量最多的气体是
(2)医疗急救时用到的气体是
(3)可填充霓虹灯且通电时会发出有色光的气体是
(4)能作燃料的是
Ⅱ.我们生活在物质世界中,每天都要接触很多物质,如:
(5)①二氧化碳、②铁粉、③氮气。其中属于化合物物的有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
真题
解题方法
【推荐1】A﹣H为初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去)已知A、B是组成元素相同的两种物质,D是一种固体单质,H是蓝色沉淀。
请按要求回答下列问题:

(1)A的化学式是_____ 。
(2)写出反应⑤的化学方程式_____ 。
(3)写出D的一种用途_____ (合理即可)。
请按要求回答下列问题:

(1)A的化学式是
(2)写出反应⑤的化学方程式
(3)写出D的一种用途
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐2】柠檬酸亚铁(FeC6H6O7)是一种补血剂,易溶于水,难溶于乙醇。某科研小组在实验室研究制备柠檬酸亚铁。
I.制碳酸亚铁
用预处理后的硫铁矿烧渣(主要成分Fe2O3,含少量不溶性杂质)制备碳酸亚铁的流程如图:
b.FeSO4在碱性条件下生成Fe(OH)2沉淀。
(1)“酸浸”时,为提高铁元素的浸出率,可采取的措施是_______ (任写一条)。
(2)“还原”时,加入铁粉,溶液由黄色变为浅绿色,同时有无色气体生成。“酸浸”所得溶液中含有的阳离子是_______ (填离子符号)。
(3)“操作X”是为了除去过量铁粉和不溶性杂质。“操作X”是_______ (填操作名称)。
(4)“沉铁”时,反应原理为FeSO4+Na2CO3=FeCO3↓+Na2SO4。
①该反应的基本类型为_______ 。
②实验时需将Na2CO3溶液滴入FeSO4溶液中,而不能反向滴加,其原因是______ 。
③待FeSO4完全反应后,过滤,洗涤。洗涤前,FeCO3沉淀表面吸附的主要杂质是______ (填化学式)。
II.制柠檬酸亚铁
(5)用如图所示装置制备柠檬酸亚铁:
步骤2:将所得混合溶液加热浓缩,加入适量无水乙醇,静置,过滤,洗涤,干燥,得到柠檬酸亚铁晶体。
制备原理为FeCO3+C6H8O7=FeC6H6O7+X+H2O,物质X是______ (填化学式)。
②“步骤2”中,加入无水乙醇的目的是_______ 。
③实验所得柠檬酸亚铁的质量大于根据原理计算所得的质量,原因是______ 。
I.制碳酸亚铁
用预处理后的硫铁矿烧渣(主要成分Fe2O3,含少量不溶性杂质)制备碳酸亚铁的流程如图:
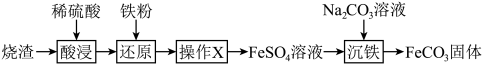
b.FeSO4在碱性条件下生成Fe(OH)2沉淀。
(1)“酸浸”时,为提高铁元素的浸出率,可采取的措施是
(2)“还原”时,加入铁粉,溶液由黄色变为浅绿色,同时有无色气体生成。“酸浸”所得溶液中含有的阳离子是
(3)“操作X”是为了除去过量铁粉和不溶性杂质。“操作X”是
(4)“沉铁”时,反应原理为FeSO4+Na2CO3=FeCO3↓+Na2SO4。
①该反应的基本类型为
②实验时需将Na2CO3溶液滴入FeSO4溶液中,而不能反向滴加,其原因是
③待FeSO4完全反应后,过滤,洗涤。洗涤前,FeCO3沉淀表面吸附的主要杂质是
II.制柠檬酸亚铁
(5)用如图所示装置制备柠檬酸亚铁:

步骤2:将所得混合溶液加热浓缩,加入适量无水乙醇,静置,过滤,洗涤,干燥,得到柠檬酸亚铁晶体。
制备原理为FeCO3+C6H8O7=FeC6H6O7+X+H2O,物质X是
②“步骤2”中,加入无水乙醇的目的是
③实验所得柠檬酸亚铁的质量大于根据原理计算所得的质量,原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】A~G是初中化学常见物质,其中,A的浓溶液挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀。如图是这些物质的转化关系,部分反应物、生成物及反应物条件已省略。

(1)请写出化学式:A________ 、G ________ 。
(2)写出D→E的化学方程式:_____________________________________________________ 。
(3)写出C→B的化学方程式:______________________________________________________ 。

(1)请写出化学式:A
(2)写出D→E的化学方程式:
(3)写出C→B的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】用废弃的镍催化剂(主要成分是Ni,少量的Fe、Cu等)制备NiCO3的实验流程如图:

提示:①在酸性溶液中,铜能与过氧化氢溶液反应;②NiCO3难溶于水
请回答:
(1)“酸溶”中Fe与稀硫酸反应的化学方程式为_____ 。
(2)“氧化”的反应为:H2O2+2FeSO4+X=Fe2(SO4)3+2H2O,则X为_____ (填化学式)。
(3)经操作Ⅰ后,滤渣的成分除Fe(OH)3外,还有_____ (填化学式)。
(4)“沉镍”是将Na2CO3溶液加入NiSO4溶液中,反应的化学方程式为_____ 。

提示:①在酸性溶液中,铜能与过氧化氢溶液反应;②NiCO3难溶于水
请回答:
(1)“酸溶”中Fe与稀硫酸反应的化学方程式为
(2)“氧化”的反应为:H2O2+2FeSO4+X=Fe2(SO4)3+2H2O,则X为
(3)经操作Ⅰ后,滤渣的成分除Fe(OH)3外,还有
(4)“沉镍”是将Na2CO3溶液加入NiSO4溶液中,反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙、丁4种常见物质,由氢、碳、氧、钠、钙5种元素中的2~3种组成。
(1)甲俗称纯碱,其化学式为____________ 。
(2)乙是一种氧化物,遇水放出大量的热,乙的名称是____________ 。
(3)丙与氧气在点燃条件下反应,其微观示意图如图1,请在方框中补全相应微粒的图示_____________ ,写出相应的化学方程式_____________ 。

(4)如图2所示(夹持仪器略去,K1、K2均关闭),打开K1,待液体全部流下,立即关闭K1,观察到产生大量气泡,且烧杯中丁的溶液变浑浊。充分反应后,打开K1和K2,使液体全部流入锥形瓶,瓶中无明显现象。
①用化学方程式表示烧杯中溶液变浑浊的原因____________ 。
②取反应后锥形瓶中的溶液,测得pH=3,则该溶液中含有的溶质除HCl外,还有____________ 。
(1)甲俗称纯碱,其化学式为
(2)乙是一种氧化物,遇水放出大量的热,乙的名称是
(3)丙与氧气在点燃条件下反应,其微观示意图如图1,请在方框中补全相应微粒的图示

(4)如图2所示(夹持仪器略去,K1、K2均关闭),打开K1,待液体全部流下,立即关闭K1,观察到产生大量气泡,且烧杯中丁的溶液变浑浊。充分反应后,打开K1和K2,使液体全部流入锥形瓶,瓶中无明显现象。
①用化学方程式表示烧杯中溶液变浑浊的原因
②取反应后锥形瓶中的溶液,测得pH=3,则该溶液中含有的溶质除HCl外,还有
您最近一年使用:0次