学习完金属的化学性质,同学们来到实验室进行铜、锌、银三种金属活动性顺序的探究活动。实验桌上提供的药品有:铜片、锌片、银片、硫酸锌溶液、硫酸铜溶液、硝酸银溶液和稀硫酸。
【制定计划】在老师的指导下,经过讨论,同学们设计出了以下几种实验方案:
方案一:铜片、硫酸锌溶液、硝酸银溶液;
方案二:锌片、铜片、硝酸银溶液、稀硫酸;
方案三:锌片、铜片、硫酸铜溶液、硝酸银溶液;
你的设计方案是_______ 。
【进行实验】小华同学选用方案三进行如下探究,请你帮他完成表格中的空白。
【解释与结论】根据上述实验,小华得出了三种金属的活动性顺序。
【反思与评价】探究活动结束后,同学们分享自己的收获与不足,并进行反思:
(1)有同学提出,小华的实验中不用提供的硫酸铜溶液也能得到相同的实验结论,简要说明原因________ 。
(2)小华提出,试管中的金属可以回收再利用,这样做的意义是_______ 。
【拓展与延伸】好奇的小华在老师的指导下,把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时间后过滤,发现滤液呈无色。此时,滤渣中一定含有_____ ,滤液中的溶质一定有_____ 。
【制定计划】在老师的指导下,经过讨论,同学们设计出了以下几种实验方案:
方案一:铜片、硫酸锌溶液、硝酸银溶液;
方案二:锌片、铜片、硝酸银溶液、稀硫酸;
方案三:锌片、铜片、硫酸铜溶液、硝酸银溶液;
你的设计方案是
【进行实验】小华同学选用方案三进行如下探究,请你帮他完成表格中的空白。
| 实验操作 | 实验现象 | 分析与结论 |
 | 金属活动性:Cu | |
| 锌片表面附着一层红色物质,溶液由蓝色逐渐变为无色 | 金属活动性:Zn> Cu,涉及的化学反应方程式 |
【反思与评价】探究活动结束后,同学们分享自己的收获与不足,并进行反思:
(1)有同学提出,小华的实验中不用提供的硫酸铜溶液也能得到相同的实验结论,简要说明原因
(2)小华提出,试管中的金属可以回收再利用,这样做的意义是
【拓展与延伸】好奇的小华在老师的指导下,把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时间后过滤,发现滤液呈无色。此时,滤渣中一定含有
更新时间:2022-07-07 12:28:11
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】同学们在实验室完成实验探究后得到废液 A,其中含有稀硫酸、硫酸亚铁和硫酸铜。老师将同学们分成甲乙两组,继续进行如下实验,请完成相关问题:
【甲组任务】将废液转化成硫酸亚铁晶体。实验流程如图1:
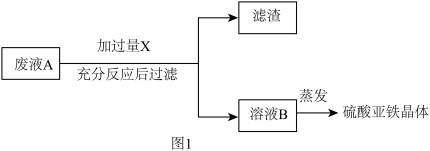
①实验流程中X 是_____ (写物质名称),过量的目的是_____ ,反应现象是_____ ,写出一个涉及的化学方程式是_____ ,该反应的基本类型_____ 。
【乙组任务】利用废液来探究金属铝的化学性质。实验流程如图2:
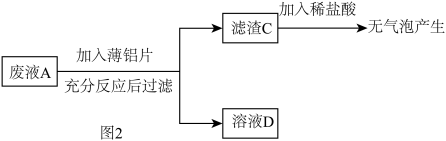
②滤渣 C 中一定没有_____ 。
③滤液 D 中一定含有的溶质是_____ (填化学式,下同),可能含有的溶质是_____ 。
【甲组任务】将废液转化成硫酸亚铁晶体。实验流程如图1:

①实验流程中X 是
【乙组任务】利用废液来探究金属铝的化学性质。实验流程如图2:

②滤渣 C 中一定没有
③滤液 D 中一定含有的溶质是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用如图所示装置进行实验:

(1)丙装置作用______________________ 。
(2)甲中发生反应的化学方程式为___________________ ,乙中现象是___________________ 。
(3)探究反应后甲中黑色固体成分(已知:Fe3O4不与CuSO4反应)。
猜想一:黑色固体成分为Fe
猜想二:黑色固体成分为Fe3O4
猜想三:___________________ 。
步骤一:通过以下三次实验,分别得到甲中固体样品A、B、C。
(4)步骤二:向样品A、B、C中分别加入足量CuSO4溶液。
(5)根据上述实验,若通入CO时间为90s,要得到纯铁粉,则加热时间应选_________________ s。

(1)丙装置作用
(2)甲中发生反应的化学方程式为
(3)探究反应后甲中黑色固体成分(已知:Fe3O4不与CuSO4反应)。
猜想一:黑色固体成分为Fe
猜想二:黑色固体成分为Fe3O4
猜想三:
步骤一:通过以下三次实验,分别得到甲中固体样品A、B、C。
| 加热/s | 通入CO/s | 样品 |
| 90 | 30 | A |
| 90 | 90 | B |
| 180 | 90 | C |
| 样品 | 现象 | 结论 |
| A | 无明显现象 | 猜想 |
| B | 有红色固体析出,有少量黑色固体剩余 | 猜想 |
| C | 猜想 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】蒸汽眼罩逐渐走进日常生活,它借助铁生锈产生热量,使材料内部的水分稳定蒸发,利用产生的热度和湿度缓解眼部疲劳。某小组从化学视角对蒸汽眼罩进行探究活动。
【实验探究】
(1)探究一:检验蒸汽眼罩内部材料中有铁粉(用化学方法)
(2)探究二:蒸汽眼罩快速发热的原因
铁生锈,是铁与_______ 共同作用的结果,但放热缓慢。哪些因素能加快反应,使蒸汽眼罩快速发热?小组同学设计了以下实验方案进行验证:将药品放入密闭容器中,通过数字传感器分别测得氧气含量变化和温度变化。
(查阅资料:蒸汽眼罩内部材料有铁粉、活性、氯化钠、水等。)
实验2中应取用氯化钠的质量是_______ g。实验4中温度迅速上升的原因是铁粉与_______ 共同作用的结果。
【拓展延伸】小组同学想知道炭粉的量对铁粉生锈快慢的影响,于是利用浓度为3.6%的NaCl溶液,2.0g铁粉与不同质量的炭粉混合进行如图所示实验,打开止水夹,记录烧杯中水开始倒吸进入烧瓶所消所耗的时间,如下表:

分析实验数据,可得出的结论是_______ 。
【反思评价】
①炭粉、氯化钠等在一定条件下能促进铁的锈蚀。但在实际生产蒸汽眼罩时,炭粉等物质的质量要控制在一定的比例范围,并不是越多越好,你分析原因是_______ (写出一条)。
②结合上述探究,谈谈你对铁生锈的辩证认识:_______ 。
【实验探究】
(1)探究一:检验蒸汽眼罩内部材料中有铁粉(用化学方法)
| 选用试剂 | 预计观察到的实验现象 | 涉及的化学方程式 |
(2)探究二:蒸汽眼罩快速发热的原因
铁生锈,是铁与
(查阅资料:蒸汽眼罩内部材料有铁粉、活性、氯化钠、水等。)
| 方案 | 药品 | 1分钟前后氧气含量变化 | 1分钟前后温度变化 |
| 实验1 | 4g铁粉、2mL水 | 20.1%→20.1% | 16℃→16℃ |
| 实验2 | 4g铁粉、2mL水、__?__g氯化钠 | 20.1%→20.1% | 16℃→16℃ |
| 实验3 | 4g铁粉、2mL水、2g活性炭 | 20.1%→20.1% | 16℃→16℃ |
| 实验4 | 4g铁粉、2mL水、2g氯化钠、2g活性炭 | 20.1%→15% | 16℃→55℃→26℃ |
【拓展延伸】小组同学想知道炭粉的量对铁粉生锈快慢的影响,于是利用浓度为3.6%的NaCl溶液,2.0g铁粉与不同质量的炭粉混合进行如图所示实验,打开止水夹,记录烧杯中水开始倒吸进入烧瓶所消所耗的时间,如下表:

| 炭粉的质量/g | 0.5 | 1 | 2.0 | 2.5 | …… |
| 时间/s | 1468 | 376 | 212 | 162 | …… |
【反思评价】
①炭粉、氯化钠等在一定条件下能促进铁的锈蚀。但在实际生产蒸汽眼罩时,炭粉等物质的质量要控制在一定的比例范围,并不是越多越好,你分析原因是
②结合上述探究,谈谈你对铁生锈的辩证认识:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】化学规律建立在实验基础之上,质量守恒定律可以用许多化学实验加以验证。
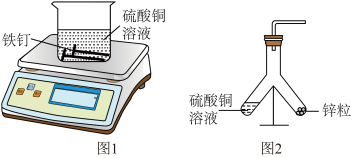
(1)小东同学按照课本上的实验进行验证(如图1所示)。一段时间后,可以观察到铁钉表面出现_____ ,其反应的化学反应方程式为_____ ,反应前后天平读数不变,但溶液颜色变化不明显。
(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
【实验分析】从以上现象分析,实验1中溶液颜色几乎不变的原因可能是_____ (填序号)。
a.铁与饱和硫酸铜溶液不反应
b.铁表面形成了一层氧化膜,阻止了反应的进一步进行
c.生成的铜快速沉积在铁表面,阻止了反应的进一步进行
d.水也参与了该反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸铜溶液呈酸性,所以总质量减小的原因可能是_____ 。
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水,将实验2中的烧杯换成如图2所示装置,均能达到实验目的,但该装置并不完善,请你在装置图中补充完善。_____

(1)小东同学按照课本上的实验进行验证(如图1所示)。一段时间后,可以观察到铁钉表面出现
(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
| 实验内容 | 实验现象 | |
| 实验1 | 烧杯中换成饱和硫酸铜溶液 | ①1小时后溶液颜色几乎不变 ②天平读数不变 ③铁钉表面有变化 |
| 实验2 | 铁钉换成锌粒 | ①溶液颜色明显变浅 ②天平读数减小 ③锌粒表面有变化 |
a.铁与饱和硫酸铜溶液不反应
b.铁表面形成了一层氧化膜,阻止了反应的进一步进行
c.生成的铜快速沉积在铁表面,阻止了反应的进一步进行
d.水也参与了该反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸铜溶液呈酸性,所以总质量减小的原因可能是
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水,将实验2中的烧杯换成如图2所示装置,均能达到实验目的,但该装置并不完善,请你在装置图中补充完善。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐2】化学兴趣小组的同学将足量的锌粒加入到某未知浓度硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究。
已知,锌与稀硫酸反应的化学方程式__________
【提出问题】锌粒加入某未知浓度硫酸后生成的气体是什么?
【查阅资料】
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色;
③H2+CuO Cu+H2O
Cu+H2O
【提出猜想】
甲:气体是H2 ; 乙:气体是SO2 ; 丙:气体是SO2和H2 。
【实验探究】
为了验证上述猜想,同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:

(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有________ 。
(2)C装置在点燃酒精灯加热之前应先通一段时间的气体,加热一段时间后,观察到______ ,证明气体中含有H2。
【讨论】
(1)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?
用文字简述原因:_________ 。
(2)锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是____ (任填一种合理的答案)。
已知,锌与稀硫酸反应的化学方程式
【提出问题】锌粒加入某未知浓度硫酸后生成的气体是什么?
【查阅资料】
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色;
③H2+CuO
 Cu+H2O
Cu+H2O【提出猜想】
甲:气体是H2 ; 乙:气体是SO2 ; 丙:气体是SO2和H2 。
【实验探究】
为了验证上述猜想,同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:

(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有
(2)C装置在点燃酒精灯加热之前应先通一段时间的气体,加热一段时间后,观察到
【讨论】
(1)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?
用文字简述原因:
(2)锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】为研究铝和铜的金属活动性,某研究小组进行了如下探究。
(1)小明设计的实验方案是:将铝片和铜片分别放入稀盐酸中,观察反应的现象。写出铝与稀盐酸反应的化学方程式_______________ 。你认为小明的实验能否比较铜和铝的金属活动性强弱?__________ (填“能”或“不能”)。
(2)小芳将铝片放入浓氯化铜溶液中,看到有气泡逸出,且在一段时间内气泡越来越多,收集该气体点燃可产生淡蓝色的火焰,则生成的气体可能是________________ 。
(3)小芳在(2)实验后,观察到溶液中有“白色固体”,于是她对这一“异常”现象进行探究。
【提出问题】白色固体中含有什么?
【查阅资料】①AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。
②CuCl为白色固体,不溶于水、乙醇;溶于浓盐酸且溶液变褐色;溶于浓氨水且溶液变蓝色。
【提出合理假设】假设a:该白色固体可能含有Al;
假设b:该白色固体可能含有AlCl3;
假设c:该白色固体可能含有________________ 。
【设计并完成实验】取白色固体分别进行如下实验:
【得出结论】由实验①可判断假设a________________ (填“成立”或“不成立”),再结合实验②和③可得出该白色固体的成分是___________ 。
(1)小明设计的实验方案是:将铝片和铜片分别放入稀盐酸中,观察反应的现象。写出铝与稀盐酸反应的化学方程式
(2)小芳将铝片放入浓氯化铜溶液中,看到有气泡逸出,且在一段时间内气泡越来越多,收集该气体点燃可产生淡蓝色的火焰,则生成的气体可能是
(3)小芳在(2)实验后,观察到溶液中有“白色固体”,于是她对这一“异常”现象进行探究。
【提出问题】白色固体中含有什么?
【查阅资料】①AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。
②CuCl为白色固体,不溶于水、乙醇;溶于浓盐酸且溶液变褐色;溶于浓氨水且溶液变蓝色。
【提出合理假设】假设a:该白色固体可能含有Al;
假设b:该白色固体可能含有AlCl3;
假设c:该白色固体可能含有
【设计并完成实验】取白色固体分别进行如下实验:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量浓盐酸 | 无气泡产生,固体全部溶解,得到褐色溶液 |
| ② | 加入适量无水乙醇 | 固体部分溶解 |
| ③ | 加入适量浓氨水 | 固体部分溶解,得到蓝色溶液 |
【得出结论】由实验①可判断假设a
您最近一年使用:0次
【推荐1】甲同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬的。她想到在学过的金属活动性顺序中并没有金属铬,为比较铬与常见金属铜的活动性强弱,她和同学们在应用所学知识进行分析的基础上,提出了以下猜想,并进行了实验探究。
【作出猜想】
猜想一:Cr>Cu ;猜想二:_____ 。
【查阅资料】
①铬是一种银白色金属。
②铬能与稀盐酸反应,生成蓝色的氯化亚铬(铬元素显+2 价)溶液。请写出铬与稀盐酸反应的化学方程式_____ 。
【实验验证】请你设计实验验证猜想一,并将相关内容填在下表。 限选药品:铬片、铜片、稀盐酸、氯化铜溶液、氯化亚铬溶液。
【实验拓展】
另一同学利用下列药品中的其中三种验证了镁、铬、铁的金属活动性强弱为 Mg>Cr>Fe,他选择的三种药品可能是_____ (填序号)。
①铬片、②铁片、③镁片、④稀盐酸、⑤氯化亚铬溶液、⑥氯化镁溶液、⑦氯化亚铁溶液
【作出猜想】
猜想一:Cr>Cu ;猜想二:
【查阅资料】
①铬是一种银白色金属。
②铬能与稀盐酸反应,生成蓝色的氯化亚铬(铬元素显+2 价)溶液。请写出铬与稀盐酸反应的化学方程式
【实验验证】请你设计实验验证猜想一,并将相关内容填在下表。 限选药品:铬片、铜片、稀盐酸、氯化铜溶液、氯化亚铬溶液。
| 实验操作 | 实验现象 | 结论 |
| 猜想一正确。铬、铜两种金属的活 动性强弱为:Cr>Cu。 |
【实验拓展】
另一同学利用下列药品中的其中三种验证了镁、铬、铁的金属活动性强弱为 Mg>Cr>Fe,他选择的三种药品可能是
①铬片、②铁片、③镁片、④稀盐酸、⑤氯化亚铬溶液、⑥氯化镁溶液、⑦氯化亚铁溶液
您最近一年使用:0次
【推荐2】某化学兴趣小组为了探究铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行了如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜。铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu;猜想②:Cr>Cu>Al;猜想③:Al>Cr>Cu;猜想④:Al>Cu>Cr
(1)【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的猜想有______ (填序号)。
【实验设计及过程】请将表中的内容填写完整。
【实验反思】(2)①将金属片投入稀硫酸前应先打磨金属片的目的是______ 。
②有同学提出探究金属活动性强弱还可以依据“金属与盐溶液是否发生置换反应”来判断。为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:
①把甲放入乙的盐溶液中 ②把乙放入丙的盐溶液中 ③把甲放入丙的盐溶液中
你认为该方案中的______ (填序号)没有必要做。
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜。铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu;猜想②:Cr>Cu>Al;猜想③:Al>Cr>Cu;猜想④:Al>Cu>Cr
(1)【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的猜想有
【实验设计及过程】请将表中的内容填写完整。
| 实验操作 | 实验现象 | 实验结论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片铜片分别投入盛有体积相同、溶质质量分数相的稀硫酸的试管中、 | 铬片表面产生气泡缓慢,铝片表面产生气泡较快,铜片表面无现象 | 猜想 |
②有同学提出探究金属活动性强弱还可以依据“金属与盐溶液是否发生置换反应”来判断。为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:
①把甲放入乙的盐溶液中 ②把乙放入丙的盐溶液中 ③把甲放入丙的盐溶液中
你认为该方案中的
您最近一年使用:0次
【推荐3】铁是应用最为广泛的金属,以下为某同学所做的与铁相关的两个实验。图1是他设计的为验证铁、铜、锌、银的金属活动性顺序及与氢的相对位置的实验。(所用金属已打磨,且形状、大小相同,稀盐酸体积、浓度均相同)。图2是他模拟工业炼铁的装置图。


(1)关于上述图1中的实验,下列说法正确的是_____ (填序号)。
A 甲试管中的实验现象为有气泡产生,溶液变为黄色
B 乙试管中反应后溶液的质量变大
C 实验室不用丙中原理制取H2,因为产生H2的中含有的HCl气体不纯
D 为达到实验目的,还需要补充的实验是铜放入硫酸亚铁溶液中
(2)乙试管中发生反应的方程式为:_____ 。
(3)用图2所示装置模拟工业炼铁,关于该实验说法错误的是_____ (填序号)。
A 实验过程中先通入一氧化碳后加热,目的是排出装置中空气,防止加热时爆炸
B 反应过程中硬质玻璃管内的现象为红棕色粉末变黑
C 装有氢氧化钠溶液的多功能瓶,其作用仅为吸收二氧化碳
D 停止加热后,继续通入CO直至装置冷却,可防止氧气进入将铁再次氧化


(1)关于上述图1中的实验,下列说法正确的是
A 甲试管中的实验现象为有气泡产生,溶液变为黄色
B 乙试管中反应后溶液的质量变大
C 实验室不用丙中原理制取H2,因为产生H2的中含有的HCl气体不纯
D 为达到实验目的,还需要补充的实验是铜放入硫酸亚铁溶液中
(2)乙试管中发生反应的方程式为:
(3)用图2所示装置模拟工业炼铁,关于该实验说法错误的是
A 实验过程中先通入一氧化碳后加热,目的是排出装置中空气,防止加热时爆炸
B 反应过程中硬质玻璃管内的现象为红棕色粉末变黑
C 装有氢氧化钠溶液的多功能瓶,其作用仅为吸收二氧化碳
D 停止加热后,继续通入CO直至装置冷却,可防止氧气进入将铁再次氧化
您最近一年使用:0次



