取MgCl2、KCl两种固体的混合物与一定质量的KOH溶液恰好完全反应,过滤得到5.8g沉淀和244g溶质质量分数为10%的KCl溶液。计算:原混合物中KCl质量分数。
更新时间:2022-07-17 12:49:16
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】石灰石的主要成分是碳酸钙。欲测定某石灰石样品中碳酸钙的质量分数,请回答下列问题:
(1)欲配制100g的7.3%的稀盐酸,需36.5%的浓盐酸的质量是__________________________ ;
(2)将石灰石粉碎,加入稀盐酸后发生反应的化学方程式是______________________________ ;
(3)若称取12.5 g 石灰石粉末放在烧杯里,然后往烧杯中加入刚配制的稀盐酸100 g,恰好完全反应后,称得反应剩余物为108.1 g 。(假设其他物质不与盐酸反应),求解石灰石中碳酸钙质量(X)的比例式为____________________ ;
(4)此石灰石样品中碳酸钙的质量分数为____________________ ;
(5)向反应后过滤所得滤液中加入5.4g水,则最终溶液中溶质的质量分数是________ ;
(6)若某建筑工地需要含杂质5%的生石灰2240t,用煅烧石灰石的方法制取,则需这种石灰石的质量是__________ t(假设制取过程中石灰石的利用率为95%)。
(1)欲配制100g的7.3%的稀盐酸,需36.5%的浓盐酸的质量是
(2)将石灰石粉碎,加入稀盐酸后发生反应的化学方程式是
(3)若称取12.5 g 石灰石粉末放在烧杯里,然后往烧杯中加入刚配制的稀盐酸100 g,恰好完全反应后,称得反应剩余物为108.1 g 。(假设其他物质不与盐酸反应),求解石灰石中碳酸钙质量(X)的比例式为
(4)此石灰石样品中碳酸钙的质量分数为
(5)向反应后过滤所得滤液中加入5.4g水,则最终溶液中溶质的质量分数是
(6)若某建筑工地需要含杂质5%的生石灰2240t,用煅烧石灰石的方法制取,则需这种石灰石的质量是
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
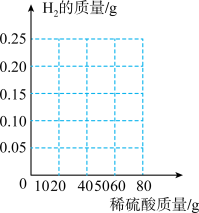
【推荐2】铁粉中混入了少量的某种盐杂质,为测定混合物中铁粉的质量分数,某小组进行了如下操作:称取7.7g混合物,然后将80 g稀硫酸分四次加入盛装混合物的容器中,测得加入稀硫酸的质量与生成氢气的质量关系如下表。( 盐杂质不与单质铁反应)
(1)表中m的值为______;第三次加入的硫酸________(填“被”或“未被")反应完。
(2)计算混合物中铁粉的质量分数是多少?(写出计算过程,结果精确到0.1%)
(3)请根据数据和计算结果,在坐标中画出对应的曲线。
(4)第一次加入稀硫酸时,产生的氢气只有0.05g 的原因可能是________
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量/ g | 20 | 20 | 20 | 20 |
| 产生氢气的累计质量/g | 0.05 | 0.15 | 0.20 | m |
(1)表中m的值为______;第三次加入的硫酸________(填“被”或“未被")反应完。
(2)计算混合物中铁粉的质量分数是多少?(写出计算过程,结果精确到0.1%)
(3)请根据数据和计算结果,在坐标中画出对应的曲线。

(4)第一次加入稀硫酸时,产生的氢气只有0.05g 的原因可能是________
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】在实验室里,甲同学用氯酸钾和二氧化锰混合固体加热制取一定量的氧气后,得到44.4 g的固体。乙同学继续加热这些固体至完全反应后又制得了一些氧气,同时得到的34.8g固体,乙同学将其充分溶解于170.2 g水中,搅拌后过滤,得一定质量的滤液,并将过滤后所得固体洗涤、干燥,得到5g黑色固体。请回答下列问题:
(1)甲同学的实验中发生反应的化学方程式;
(2)乙同学所做的实验中制得氧气的质量;
(3)在乙同学的实验中,列出求解氯酸钾质量(x)的比例;
(4)上述实验所得滤液中溶质的质量分数;
(5)甲同学和乙同学在实验中消耗氯酸钾的质量比;
(6)上述氯酸钾和二氧化锰混合固体中氯酸钾的含量。
(1)甲同学的实验中发生反应的化学方程式;
(2)乙同学所做的实验中制得氧气的质量;
(3)在乙同学的实验中,列出求解氯酸钾质量(x)的比例;
(4)上述实验所得滤液中溶质的质量分数;
(5)甲同学和乙同学在实验中消耗氯酸钾的质量比;
(6)上述氯酸钾和二氧化锰混合固体中氯酸钾的含量。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】把10g含杂质的锌片(杂质不与硫酸反应,也不溶于水)放在100g稀硫酸中,恰好完全反应,反应后得到的混合物总质量是109.8g。
(1)反应后生成的氢气质量是_____g;
(2)所用稀硫酸的溶质质量分数_____。
(1)反应后生成的氢气质量是_____g;
(2)所用稀硫酸的溶质质量分数_____。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐2】将适量的二氧化碳通入到一定质量的氢氧化钠的溶液中,恰好完全反应,得到106g质量分数为10%的碳酸钠溶液。
(1)反应生成的碳酸钠质量为 g。
(2)反应前氢氧化钠溶液的溶质质量分数。(写出计算过程,最终结果保留0.1%)
(1)反应生成的碳酸钠质量为 g。
(2)反应前氢氧化钠溶液的溶质质量分数。(写出计算过程,最终结果保留0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】为测定海洋化工集团生产的碳酸钠样品(杂质既不溶于水也不发生任何反应)中碳酸钠的含量(即碳酸钠的质量分数),诗琪同学进行如下实验:
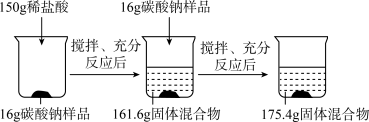
(1)上述实验过程中发生反应的化学方程式为______;
(2)样品中碳酸钠的含量是______;
(3)根据已知条件列出求解150g稀盐酸中氯化氢质量(x)的比例式______;
(4)向161.6g固液混合物中加入16g碳酸钠样品的实验中生成水的质量为______。

(1)上述实验过程中发生反应的化学方程式为______;
(2)样品中碳酸钠的含量是______;
(3)根据已知条件列出求解150g稀盐酸中氯化氢质量(x)的比例式______;
(4)向161.6g固液混合物中加入16g碳酸钠样品的实验中生成水的质量为______。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】为测定某镁矿石中镁元素的质量分数,兴趣小组的同学取了10g该镁矿石粉末,加入过量的稀盐酸,充分反应后过滤、除杂,得到只含有 和
和 两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
请计算:
(1)该镁矿石中镁元素的质量分数为________ 。(假设10g镁矿石中的镁元素全部转化到100g混合溶液中)
(2)加入的氢氧化钠溶液的溶质质量分数为_____________ 。
(3)将恰好完全反应时的溶液过滤,再将滤液蒸发掉89.18g水,所得溶液中溶质质量分数为多少?(假设整个过程无损耗)
 和
和 两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:实验编号 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 |
加入氢氧化钠溶液质量/g | 10 | 10 | 10 | 10 | 10 | 10 |
烧杯中生成沉淀的总质量/g | 0 | 0.58 | 1.16 | 1.74 | 2.32 | 2.32 |
(1)该镁矿石中镁元素的质量分数为
(2)加入的氢氧化钠溶液的溶质质量分数为
(3)将恰好完全反应时的溶液过滤,再将滤液蒸发掉89.18g水,所得溶液中溶质质量分数为多少?(假设整个过程无损耗)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】实验技能训练中,小亮同学向氧化铜和稀硫酸充分反应后的废液中加入一定量的氢氧化钠溶液,发现无明显现象。小亮同学在老师的指导下对氧化铜和稀硫酸充分反应后的废液进行了实验:他分别取50g废液,并向其中逐渐加入等浓度的氢氧化钠溶液,三组实验的数据与图像如下:
请根据以上信息回答下列问题:
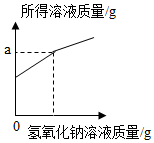
(1)氧化铜粉末与稀硫酸反应的现象为___________。
(2)废液中的溶质有_______________(填化学式) ,并计算废液中硫酸铜的溶质质量分数________。(写出计算过程)
请根据以上信息回答下列问题:
| 实验组数 | 第一组 | 第二组 | 第三组 |
| 加入氢氧化钠溶液质量/g | 50 | 100 | 80 |
| 产生沉淀的质量/g | 0.98 | 2.94 | 2.94 |

(1)氧化铜粉末与稀硫酸反应的现象为___________。
(2)废液中的溶质有_______________(填化学式) ,并计算废液中硫酸铜的溶质质量分数________。(写出计算过程)
您最近一年使用:0次



