为除去粗盐中的CaCl2、MgCl2杂质,某化学小组设计了如下方案:
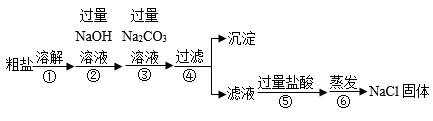
已知:Mg(OH)2难溶于水。
(1)过滤和蒸发时都用到一种玻璃仪器,该仪器在蒸发操作中的作用是_____________ 。
(2)设计实验证明滤液中除去了NaCl以外的其他杂质成分_____________ 。
(3)加入过量盐酸的目的是____________________ 。

已知:Mg(OH)2难溶于水。
(1)过滤和蒸发时都用到一种玻璃仪器,该仪器在蒸发操作中的作用是
(2)设计实验证明滤液中除去了NaCl以外的其他杂质成分
(3)加入过量盐酸的目的是
2021·海南·二模 查看更多[1]
更新时间:2022-07-24 22:28:16
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E为初中化学常见的五种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“—”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。

⑴若A的固体可用于人工降雨,B为植物光合作用的产物之一,E在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。则B为__________ ;D与E反应的基本类型为___________
⑵若A为人体胃酸的士要成分,D与E经混合研磨可产生刺激性气味的气体,且图中体现了A的四种不同化学性质。则C物质的类别是__________ ;D与E反应的化学方程式为___________________________ 。

⑴若A的固体可用于人工降雨,B为植物光合作用的产物之一,E在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。则B为
⑵若A为人体胃酸的士要成分,D与E经混合研磨可产生刺激性气味的气体,且图中体现了A的四种不同化学性质。则C物质的类别是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】A~H都是初中化学中的常见物质,它们之间的转化关系如图所示.A是天然气的主要成分,E是一种常见的食品干燥剂.请回答:
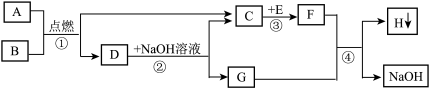
(1)物质C的化学式________ ; (2)反应③的基本反应类型是___________ ;
(3)写出有关反应的化学方程式:
②______________________ ,
④________________________ .

(1)物质C的化学式
(3)写出有关反应的化学方程式:
②
④
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】国家对化学实验室废弃药品的处理有严格要求,处理关键是确定其成分。某校化学实验室有一包固体废弃物,可能由铁粉、碳粉,碳酸钠、氧化铜、氯化钠、氢氧化钾中的一种或几种组成,为确定其成分,同学们取样进行了如下实验:
【实验一】

(1)操作I的名称是_________________ 。
(2)向固体A中加入足量稀盐酸充分反应,没有气泡冒出,固体未完全溶解,溶液由无色变成蓝色,说明原废弃物中一定有________________ (填化学式,下同),一定没有_________________ ,发生反应的化学方程式是_________________ 。
【实验二】
步骤一:

步骤二:
取混合物D中的上层清液少许,滴加酚酞溶液,溶液变红。
(3)混合物D中有白色沉淀,则原废弃物中有_________________ ,发生反应的化学方程式是_________________ 。
(4)向混合物D中加过量稀硝酸现象是_________________ ,加入稀硝酸后一定发生反应的化学方程式是_________________ (一个即可)。
(5)混合物F中有白色沉淀,其上层清液中一定含有的溶质是NaNO3、HNO3和_________________ 。
【反思与交流】
上述实验一、二的结果不能确定氢氧化钾是否存在,为了确认其是否存在,且不影响其他物质的检验,需要对步骤一中的氢氧化钡溶液改为_________________ 。
【实验一】

(1)操作I的名称是
(2)向固体A中加入足量稀盐酸充分反应,没有气泡冒出,固体未完全溶解,溶液由无色变成蓝色,说明原废弃物中一定有
【实验二】
步骤一:

步骤二:
取混合物D中的上层清液少许,滴加酚酞溶液,溶液变红。
(3)混合物D中有白色沉淀,则原废弃物中有
(4)向混合物D中加过量稀硝酸现象是
(5)混合物F中有白色沉淀,其上层清液中一定含有的溶质是NaNO3、HNO3和
【反思与交流】
上述实验一、二的结果不能确定氢氧化钾是否存在,为了确认其是否存在,且不影响其他物质的检验,需要对步骤一中的氢氧化钡溶液改为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】为除去粗盐中的可溶性杂质MgSO4、CaCl2,某化学小组设计了以下方案:

(1)该方案中发生了多个反应,请写出发生中和反应的化学方程式。
(2)向溶液X中加入适量的稀盐酸,发现刚开始时,无明显现象,过了一段时间,有气泡产生,请解释原因。
(3)请设计实验加以证明溶液X的成分。(简要写出实验步骤和现象)

(1)该方案中发生了多个反应,请写出发生中和反应的化学方程式。
(2)向溶液X中加入适量的稀盐酸,发现刚开始时,无明显现象,过了一段时间,有气泡产生,请解释原因。
(3)请设计实验加以证明溶液X的成分。(简要写出实验步骤和现象)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“粗盐提纯”指除去NaCl中的泥沙和CaCl2、MgCl2、Na2SO4等杂质。某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中加入过量的Na2CO3、Ca(OH)2、BaCl2溶液充分反应后过滤、向滤液中加入足量的稀盐酸,蒸发结晶。
(1)上述实验中,加入溶液的次序有误,请改正____________________ 。
(2)正确次序时加入过量Na2CO3溶液的目是_______________________ 。
(3)上述实验过程中发生了几个复分解反应___________________ 。
(1)上述实验中,加入溶液的次序有误,请改正
(2)正确次序时加入过量Na2CO3溶液的目是
(3)上述实验过程中发生了几个复分解反应
您最近一年使用:0次
【推荐3】汕头是滨海城市,盛产海盐。食盐是生活必需品,也是重要的化工原料。
(1)某学习小组进行粗盐提纯实验,主要经过以下操作步骤:称量→溶解→_____ →蒸发→再次称量→计算产率。在蒸发操作中使用到玻璃棒,作用是 __________ 。实验结束后,该小组发现所得食盐产率明显低于其他小组,其原因可能是 _____________ 。
A. 粗盐未充分溶解就过滤
B. 倾倒时,有部分氯化钠溶液溅出
C. 蒸发后,所得的精盐较潮湿
(2)电解饱和食盐水可以得到多种化工产品,主要过程如下:

①气体A是密度最小的气体,该气体的名称为_____ ,写出一个由酸D转化为气体A 的化学方程式 ____________________________________ 。
②电解后生成的碱B的化学式为______________________ ,你猜想的依据是 ____________________ 。
(1)某学习小组进行粗盐提纯实验,主要经过以下操作步骤:称量→溶解→
A. 粗盐未充分溶解就过滤
B. 倾倒时,有部分氯化钠溶液溅出
C. 蒸发后,所得的精盐较潮湿
(2)电解饱和食盐水可以得到多种化工产品,主要过程如下:

①气体A是密度最小的气体,该气体的名称为
②电解后生成的碱B的化学式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】近年来高锰酸钾在饮用水和工业污水处理领域的消费增长较快,实验室可用软锰矿(主要成分MnO2)为原料制备高锰酸钾。其部分流程如下:

(1)因瓷坩埚中含SiO2,能被氢氧化钾腐蚀,反应原理同二氧化碳与氢氧化钠的反应,请写出SiO2与氢氧化钾反应的化学方程式_____________ ,故反应只能在铁坩埚中进行。
(2)加热浓缩时需用玻璃棒不断搅拌溶液,其目的是______________________ 。
(3)在烘干箱中烘干时温度不宜过高的原因是________________ (用化学方程式表示)

(1)因瓷坩埚中含SiO2,能被氢氧化钾腐蚀,反应原理同二氧化碳与氢氧化钠的反应,请写出SiO2与氢氧化钾反应的化学方程式
(2)加热浓缩时需用玻璃棒不断搅拌溶液,其目的是
(3)在烘干箱中烘干时温度不宜过高的原因是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐2】为了除去氯化钠中的氯化钙、氯化镁、硫酸钠三种杂质。小明设计如下的操作步骤:①加水溶解后,依次加入过量氯化钡溶液、过量碳酸钠溶液、过量氢氧化钙溶液;②过滤;③向滤液中加入适量稀盐酸;④蒸发滤液得氯化钠固体。
(1)请指出步骤①中所加的试剂顺序的不足之处______________ 。
(2)改正步骤①中所加试剂的顺序后,整个提纯过程中共发生______ 个复分解反应。
(3)在蒸发过程中,玻璃棒的作用是__________________ ?
(1)请指出步骤①中所加的试剂顺序的不足之处
(2)改正步骤①中所加试剂的顺序后,整个提纯过程中共发生
(3)在蒸发过程中,玻璃棒的作用是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:

(1)反应塔1中的反应为:MnO2+SO2═MnSO4,其中化合价发生改变的元素是_____ 。
(2)洗涤塔中喷水的目的是_____ 。
(3)烘干塔中需选择“低温”干燥的原因是_____ 。
(4)上述流程中的产品除高纯MnCO3外,还有_____ 。

(1)反应塔1中的反应为:MnO2+SO2═MnSO4,其中化合价发生改变的元素是
(2)洗涤塔中喷水的目的是
(3)烘干塔中需选择“低温”干燥的原因是
(4)上述流程中的产品除高纯MnCO3外,还有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】Na2SO4主要用于制造纸浆、医药品、玻璃等。某Na2SO4样品中含有少量CaSO4和MgSO4,某化学兴趣小组在实验室提纯Na2SO4的流程如下图。(所加试剂均过量)
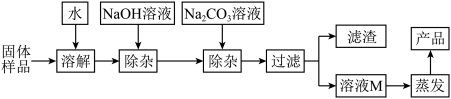
(1)请写出加入氢氧化钠溶液时反应的化学方程式___________ 。
(2)蒸发操作中玻璃棒的作用是什么?___________
(3)所得产品是否是纯净的Na2SO4,为什么?___________

(1)请写出加入氢氧化钠溶液时反应的化学方程式
(2)蒸发操作中玻璃棒的作用是什么?
(3)所得产品是否是纯净的Na2SO4,为什么?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】覆铜板是制作印刷线路板的基本材料。覆铜板中的金属 占2-10%,
占2-10%, 占90-98%。简易工艺流程如
占90-98%。简易工艺流程如

(1)将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是_______ 的性质(填字母代号)。
a 溶解性不同 b 密度不同 c 沸点不同
(2)步骤④中涉及的分离操作是_______ (填操作名称)。
(3)通过步骤⑤和⑥所得洗涤液的
_______ 7(填“>”、“<”、“=”)。
(4)设计步骤⑦的主要目的是_______ 。
 占2-10%,
占2-10%, 占90-98%。简易工艺流程如
占90-98%。简易工艺流程如
(1)将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是
a 溶解性不同 b 密度不同 c 沸点不同
(2)步骤④中涉及的分离操作是
(3)通过步骤⑤和⑥所得洗涤液的

(4)设计步骤⑦的主要目的是
您最近一年使用:0次




