流程与推断。
(1)工业上,常将煤气化,煤气化示意图如下。回答下列问题。
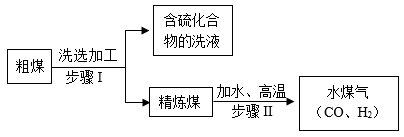
①煤属于_____ (填“混合物”或“纯净物”)。
②步骤Ⅰ分离操作的名称是_____ 。
③该工艺没有直接把粗煤作为燃料,而经过系列加工转化为生产生活中的重要燃料水煤气,主要原因是_____ (一点即可)。
(2)A、B、C、D、E是初中化学常见的物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,如图表示它们的转化关系。回答下列问题。
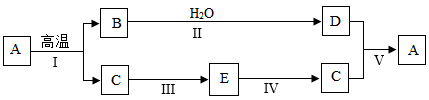
①反应Ⅰ用于工业制取二氧化碳,化学反应方程式为_____ 。
②属于放热反应的是_____ (填写“Ⅱ”或“Ⅲ”或“Ⅱ和Ⅲ”)
③E物质虽然有毒,但也是重要的化工原料,填写E物质的一种用途_____ 。
④反应Ⅴ的化学反应方程式为_____ 。
(1)工业上,常将煤气化,煤气化示意图如下。回答下列问题。

①煤属于
②步骤Ⅰ分离操作的名称是
③该工艺没有直接把粗煤作为燃料,而经过系列加工转化为生产生活中的重要燃料水煤气,主要原因是
(2)A、B、C、D、E是初中化学常见的物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,如图表示它们的转化关系。回答下列问题。

①反应Ⅰ用于工业制取二氧化碳,化学反应方程式为
②属于放热反应的是
③E物质虽然有毒,但也是重要的化工原料,填写E物质的一种用途
④反应Ⅴ的化学反应方程式为
更新时间:2022-08-10 09:42:22
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】回答问题
(1)质量守恒定律的发现,使得化学由定性研究走向定量研究,促进了化学科学的发展。李明同学用如图装置进行实验,验证质量守恒定律。

①上述实验中,能直接用来验证质量守恒定律的是___________ (填字母序号)。
②若选择A装置进行实验,实验过程中观察到气球的变化是___________ ,写出该反应的化学方程式___________ 。
③下列各项中在化学反应前后一定保持不变的是___________ 。
a.元素化合价 b.原子种类 c.分子个数 d.原子数目 e.元素种类 f.分子种类
(2)鸡蛋壳中的主要成分是碳酸钙,李明为检测鸡蛋壳中碳酸钙的含量,进行的实验及实验数据如图所示(鸡蛋壳中其他成分与稀盐酸接触不产生气体)。

请根据图中信息,计算鸡蛋壳中碳酸钙的质量分数(写出计算过程)。
(1)质量守恒定律的发现,使得化学由定性研究走向定量研究,促进了化学科学的发展。李明同学用如图装置进行实验,验证质量守恒定律。

①上述实验中,能直接用来验证质量守恒定律的是
②若选择A装置进行实验,实验过程中观察到气球的变化是
③下列各项中在化学反应前后一定保持不变的是
a.元素化合价 b.原子种类 c.分子个数 d.原子数目 e.元素种类 f.分子种类
(2)鸡蛋壳中的主要成分是碳酸钙,李明为检测鸡蛋壳中碳酸钙的含量,进行的实验及实验数据如图所示(鸡蛋壳中其他成分与稀盐酸接触不产生气体)。

请根据图中信息,计算鸡蛋壳中碳酸钙的质量分数(写出计算过程)。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】(原创) 已知,过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂,利用人呼出的二氧化碳与过氧化钠反应放出氧气,供给人的正常生命活动,该反应的化学方程式为:2Na2O2+2CO2===2Na2CO3+O2。某同学利用该反应原理制取氧气,设计实验装置如下图所示:

(1)装置①中CO2的制取方法有多种:
若用稀盐酸和碳酸钠制取CO2,该反应的化学方程式为:_______________________ ;若用稀盐酸和大理石制取CO2,该反应的化学方程式为:____________________ ;若用加热NaHCO3固体制取CO2,应该选用的发生装置为________ (选填下图字母),该反应的化学方程式为_______________ ;

(2)装置③中盛装的试剂为____________ ,作用是________________________ 。
(3)④为O2的收集装置,若想得到较为纯净的O2,应选用装置______ (选填上图字母)。

(1)装置①中CO2的制取方法有多种:
若用稀盐酸和碳酸钠制取CO2,该反应的化学方程式为:

(2)装置③中盛装的试剂为
(3)④为O2的收集装置,若想得到较为纯净的O2,应选用装置
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】从古至今,铁及其化合物一直被人类广泛应用。
一、铁的应用
(1)我国早在春秋战国时期就开始生产和使用铁器。深埋的古墓中有些铁器保存至今是因为______ (选填序号)。
a.铁不活泼 b.密封缺氧 c.干燥少水
(2)铁的化合物在现代更多领域发挥着重要作用。
①活性FeOOH可除去石油开采过程中的有害气体H2S,并获得S,原理如下:
 ,吸收中生成的另一种物质的名称为
,吸收中生成的另一种物质的名称为______ 。
②碳酸亚铁(FeCO3)可作补血剂,药片表面包裹着淀粉制作的糖衣,淀粉______ (选填“属于”或“不属于”)糖类,服用药片后与胃酸反应生成______ 被人体吸收,促进血红蛋白生成。
二、铁的化合物制备
实验室利用废铁屑(含少量Fe2O3)为原料制备碳酸亚铁(FeCO3)的流程如下:

(3)酸溶时适当提高反应温度和H2SO4浓度,目的是______ 。
(4)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为______ 。
(5)转化2中温度不宜过高的原因是______ 。
(6)在空气中灼烧FeCO3可获得颜料铁红(Fe2O3)和CO2,反应的化学方程式为______ 。
三、铁的化合物含量测定
称取含FeCO3的Fe2O3样品21.8g,放入下图所示装置中通入CO,控温在300℃,加热至质量不再改变,测得剩余固体质量为19.6g。

资料:
①FeCO3在282℃分解为FeO。
②用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:
阶段2:
阶段3:
继续向装置中通CO,分阶段升温,进行CO还原铁的氧化物,加热时测得剩余固体质量随温度变化的曲线如图所示。

(7)图中N点固体的成分及对应的质量为______ 。(写出计算过程)
一、铁的应用
(1)我国早在春秋战国时期就开始生产和使用铁器。深埋的古墓中有些铁器保存至今是因为
a.铁不活泼 b.密封缺氧 c.干燥少水
(2)铁的化合物在现代更多领域发挥着重要作用。
①活性FeOOH可除去石油开采过程中的有害气体H2S,并获得S,原理如下:
 ,吸收中生成的另一种物质的名称为
,吸收中生成的另一种物质的名称为②碳酸亚铁(FeCO3)可作补血剂,药片表面包裹着淀粉制作的糖衣,淀粉
二、铁的化合物制备
实验室利用废铁屑(含少量Fe2O3)为原料制备碳酸亚铁(FeCO3)的流程如下:

(3)酸溶时适当提高反应温度和H2SO4浓度,目的是
(4)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为
(5)转化2中温度不宜过高的原因是
(6)在空气中灼烧FeCO3可获得颜料铁红(Fe2O3)和CO2,反应的化学方程式为
三、铁的化合物含量测定
称取含FeCO3的Fe2O3样品21.8g,放入下图所示装置中通入CO,控温在300℃,加热至质量不再改变,测得剩余固体质量为19.6g。

资料:
①FeCO3在282℃分解为FeO。
②用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:

阶段2:

阶段3:

继续向装置中通CO,分阶段升温,进行CO还原铁的氧化物,加热时测得剩余固体质量随温度变化的曲线如图所示。

(7)图中N点固体的成分及对应的质量为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】A~G表示初中化学常见物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,A和G均为红色,它们之间的转化关系如图所示(反应条件,部分反应物及生成物已略去),请回答下列问题:
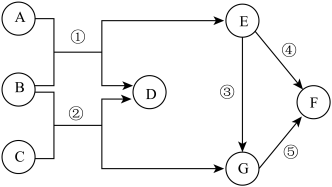
(1)D的化学式为_______ 。
(2)B的一种用途是_______ 。
(3)反应③的化学方程式为:_______ 。
(4)E、F、G三种金属的活动性由强到弱的顺序为______ 。

(1)D的化学式为
(2)B的一种用途是
(3)反应③的化学方程式为:
(4)E、F、G三种金属的活动性由强到弱的顺序为
您最近一年使用:0次
【推荐2】有限的元素可以组成种类繁多的物质,依据表中的元素回答下列问题。
(1)易使人中毒的气体,该物质的化学式是___________ 。
(2)某物质是氮肥且常温下呈液态,该物质的化学式是___________ 。
(3)写出一种你知道的酸的化学式是___________ 。
(4)小红妈妈烧排骨,使用了天然气灶具,天然气燃烧的化学方程为_______ 。
(5)下图所示物质均由上述元素组成,甲经过一步反应转化为乙有两种途径①或②,乙经过一步反应③也可转化为甲,下列说法错误的是 (填字母序号)。

| 元素名称 | 铜 | 铁 | 钠 | 氧 | 氮 | 碳 | 氢 |
| 元素符号 | Cu | Fe | Na | O | N | C | H |
(1)易使人中毒的气体,该物质的化学式是
(2)某物质是氮肥且常温下呈液态,该物质的化学式是
(3)写出一种你知道的酸的化学式是
(4)小红妈妈烧排骨,使用了天然气灶具,天然气燃烧的化学方程为
(5)下图所示物质均由上述元素组成,甲经过一步反应转化为乙有两种途径①或②,乙经过一步反应③也可转化为甲,下列说法错误的是 (填字母序号)。

| A.若甲是Fe3O4,则乙是Fe |
| B.若乙是金属,则单质、氧化物中可能含有同种元素 |
| C.若甲的相对分子质量比乙小16,则甲、乙一定分别是H2和H2O |
| D.若甲是氧化物,则①和③的基本反应类型一定相同 |
您最近一年使用:0次
【推荐3】(1)下面是教材下册中“物质溶解时的吸热或放热现象”的活动与探究。请你一同完成该探究并回答有关问题:
③根据物质溶解过程中发生的变化,说明NH4NO3固体溶解时扩散过程吸收的热量_____ 水合过程放出的热量(填“<”或“>”或“=”符号)。
(2)下图“→”表示A在一定条件下可以转化为B,“—”表示相连的两种物质间在一定条件下可以发生反应。A、B、C、D各是一氧化碳、木炭粉、氧化铜、氧气中的某一种物质,请你推断(用化学式表示):

B是________ ,D是________ 。
| 水中加入的溶质 | NaCl固体 | NH4NO3固体 | NaOH固体 |
| 加溶质前水的温度/℃ | 20 | 20 | 20 |
| 溶解现象 | 全部溶解 | 全部溶解 | 全部溶解 |
| 溶质溶解后溶液的温度变化 | 温度无明显变化 | 温度降低 | 温度升高 |
| 结论(“放热”或“吸热”) | 固体氯化钠溶于水无明显放热和吸热现象 | ① | ② |
(2)下图“→”表示A在一定条件下可以转化为B,“—”表示相连的两种物质间在一定条件下可以发生反应。A、B、C、D各是一氧化碳、木炭粉、氧化铜、氧气中的某一种物质,请你推断(用化学式表示):

B是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】为探究燃烧的条件,某兴趣小组进行了如下实验,实验装置如图1所示。

【实验步骤】
步骤1:取一小块白磷(着火点为40℃),放在一铝箔制的小盒中,然后放入装有生石灰的锥形瓶内。点燃蜡烛,塞紧胶塞,蜡烛燃烧一会儿就熄灭了。
步骤2:待装置冷却后,打开分液漏斗的活塞,向锥形瓶中注入少量水,立即关闭活塞,观察到铝盒中的白磷燃烧。
【实验分析】
(1)小明认为步骤1中蜡烛燃烧一会儿就熄灭了,是因为装置内没有氧气了,你___________ (填“赞同”或“不赞同”)小明的观点,原因是___________ 。
(2)上述步骤2中白磷燃烧应满足的条件:①温度达到白磷的着火点;②___________ 。
【实验反思】
(3)在该实验中,生石灰的主要作用是___________ ,该反应的化学方程式为___________ 。
【实验拓展】
为探究蜡烛的组成,将1.6g蜡烛放入足量氧气中燃烧,并将生成的气体全部通入图2装置(忽略所有影响因素),实验中测得有关数据如下表所示:

【查阅资料】干燥剂用于吸收水分。
(4)①实验结束后生成二氧化碳的质量为___________ g。
②通过计算,蜡烛中所含碳元素的质量为___________ g,该蜡烛中___________ (填“是”或“否”)含有氧元素。

【实验步骤】
步骤1:取一小块白磷(着火点为40℃),放在一铝箔制的小盒中,然后放入装有生石灰的锥形瓶内。点燃蜡烛,塞紧胶塞,蜡烛燃烧一会儿就熄灭了。
步骤2:待装置冷却后,打开分液漏斗的活塞,向锥形瓶中注入少量水,立即关闭活塞,观察到铝盒中的白磷燃烧。
【实验分析】
(1)小明认为步骤1中蜡烛燃烧一会儿就熄灭了,是因为装置内没有氧气了,你
(2)上述步骤2中白磷燃烧应满足的条件:①温度达到白磷的着火点;②
【实验反思】
(3)在该实验中,生石灰的主要作用是
【实验拓展】
为探究蜡烛的组成,将1.6g蜡烛放入足量氧气中燃烧,并将生成的气体全部通入图2装置(忽略所有影响因素),实验中测得有关数据如下表所示:

| 实验前 | 实验后 | |
| 装置I总质量 | 105.0g | 106.8g |
| 装置Ⅱ总质量 | 286.1g | 288.3g |
(4)①实验结束后生成二氧化碳的质量为
②通过计算,蜡烛中所含碳元素的质量为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】《石灰吟》是明代文学家于谦创作的一首七言绝句,全诗内容如下:“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间。”全诗所涉及的化学反应用流程图表示如下:

(1)过程①所发生的反应属于_______ 反应(填“化合”“分解”“置换”“复分解”之一)。
(2)写出过程③的化学方程式________________ 。
(3)上述过程所涉及的物质中经常用作干燥剂的是________ (填化学式)。
(4)为制取氢氧化钠,取一定质量的步骤②所得石灰乳,向其中滴入质量分数为10.6%的Na2CO3溶液,使其充分反应。加入Na2CO3溶液的质量和所得沉淀的质量关系如下图所示:

①当滴入10.6%的碳酸钠溶液至图中B点时,溶液中的溶质有______________ (填化学式)。
②计算恰好完全反应(至图中A点)时所得氢氧化钠的质量。(计算结果精确至0.1 g)____

(1)过程①所发生的反应属于
(2)写出过程③的化学方程式
(3)上述过程所涉及的物质中经常用作干燥剂的是
(4)为制取氢氧化钠,取一定质量的步骤②所得石灰乳,向其中滴入质量分数为10.6%的Na2CO3溶液,使其充分反应。加入Na2CO3溶液的质量和所得沉淀的质量关系如下图所示:

①当滴入10.6%的碳酸钠溶液至图中B点时,溶液中的溶质有
②计算恰好完全反应(至图中A点)时所得氢氧化钠的质量。(计算结果精确至0.1 g)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】4000多年前,我国就掌握了利用石灰石(主要成分CaCO3)烧制石灰并用于建筑的技术。文献中记载的烧制和应用过程合称“灰作六艺”,其过程如下图。
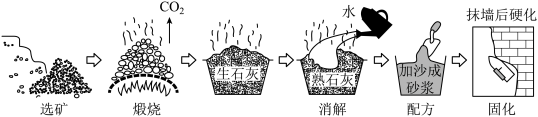
回答下列问题:
I、文献阅读理解
(1)煅烧过程中,矿石发生主要反应的化学方程式为______ 。
(2)生石灰变成熟石灰的过程是一个______ (填“吸热”或“放热”)反应。
(3)配方过程中,要制成合格的砂浆,需要把熟石灰和沙充分______ (填一操作名称)。
(4)固化过程中,最终生成的白色硬质物质的化学式是______ 。
Ⅱ、科学探究实验
选矿过程中,为测定石灰石主要成分的含量,某同学按下图装置进行实验。检查装置气密性,装入药品,移动量气管使左右液面相平。将足量稀盐酸缓慢推入烧瓶至反应完全,再次移动量气管,使左右液面相平,读数记录。
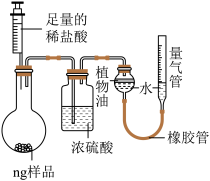
(5)检查装置气密性的方法是______ 。
(6)水层上面的植物油的作用是______ 。
(7)判断石灰石已经完全反应的现象是______ 。
(8)两次移动量气管调整液面的目的是______ 。
(9)浓硫酸的作用是______ ,如果没有浓硫酸,测定的结果会______ (填“偏大”“偏小”“不变”)。
(10)在该条件下,测定生成的二氧化碳气体(密度为dg/mL)体积为VmL,样品中CaCO3的含量为______ (写出表达式)。
(11)若要使测得的二氧化碳气体体积更加准确,你还可以补充哪些措施______ 。(写一条即可)

回答下列问题:
I、文献阅读理解
(1)煅烧过程中,矿石发生主要反应的化学方程式为
(2)生石灰变成熟石灰的过程是一个
(3)配方过程中,要制成合格的砂浆,需要把熟石灰和沙充分
(4)固化过程中,最终生成的白色硬质物质的化学式是
Ⅱ、科学探究实验
选矿过程中,为测定石灰石主要成分的含量,某同学按下图装置进行实验。检查装置气密性,装入药品,移动量气管使左右液面相平。将足量稀盐酸缓慢推入烧瓶至反应完全,再次移动量气管,使左右液面相平,读数记录。

(5)检查装置气密性的方法是
(6)水层上面的植物油的作用是
(7)判断石灰石已经完全反应的现象是
(8)两次移动量气管调整液面的目的是
(9)浓硫酸的作用是
(10)在该条件下,测定生成的二氧化碳气体(密度为dg/mL)体积为VmL,样品中CaCO3的含量为
(11)若要使测得的二氧化碳气体体积更加准确,你还可以补充哪些措施
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】化学影响着人们的衣食住行,使世界变得更加绚丽多彩。请回答下列问题:
(1)包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等,其中富含蛋白质的是______ ;
(2)生活中将硬水转化成软水的常用方法是______ ;
(3)在治疗胃酸过多症的药物成分中,含有的物质不可以是______(填字母)。
(4)“环境就是民生”。煤的大量使用导致空气质量下降,影响了生态环境,我市用天然气代替蜂窝煤作燃料,用天然气代替蜂窝煤后,空气中污染物明显减少的有______ (填一种)。
(1)包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等,其中富含蛋白质的是
(2)生活中将硬水转化成软水的常用方法是
(3)在治疗胃酸过多症的药物成分中,含有的物质不可以是______(填字母)。
| A.碳酸氢钠 | B.氢氧化铝 | C.氢氧化钠 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
解题方法
【推荐2】请沿用科学家认识事物的方式认识“空气”。
(1)从分类角度:空气属于_______ (填“混合物”或“纯净物”)。
(2)从微观角度:用“ ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。
”表示氧原子。
①用“ ”可表示的微粒是
”可表示的微粒是______________ (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图3可表示空气微观模型的是_________ (填标号)。

(3)从变化角度:
已知:常压下,氮气沸点-196℃,氧气沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是________________________ 。将该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是______________ 。
(4)从应用角度:利用空气制取氮肥的流程如图4所示。

①Ⅰ中参加反应的单质甲为________ 。
②Ⅱ中反应的化学方程式为____________________ 。
③物质所含元素化合价发生变化的反应称为氧化还原反应。反应Ⅲ________ (填“属于”或“不属于”)氧化还原反应。
(5)从环保角度:下列保护空气措施合理的是______(填标号)。
(1)从分类角度:空气属于
(2)从微观角度:用“
 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。
”表示氧原子。①用“
 ”可表示的微粒是
”可表示的微粒是②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图3可表示空气微观模型的是

(3)从变化角度:
已知:常压下,氮气沸点-196℃,氧气沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是
(4)从应用角度:利用空气制取氮肥的流程如图4所示。

①Ⅰ中参加反应的单质甲为
②Ⅱ中反应的化学方程式为
③物质所含元素化合价发生变化的反应称为氧化还原反应。反应Ⅲ
(5)从环保角度:下列保护空气措施合理的是______(填标号)。
| A.工厂通过加高烟囱直接排放废气 | B.推广使用乙醇汽油代替普通汽油 |
| C.提倡步行、骑自行车等“低碳”出行方式 | |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
【推荐3】工业用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙)。简易流程如右图,主要的反应为:2CaCO3+2SO2+O2=2CaSO4+2X。

(1)流程中石灰石加水制成石灰浆的目的是_________ 。反应中X的化学式为________ ,硫元素的化合价在反应前后的变化为__________ 。
(2)减少二氧化硫的排放,主要为了________ (填序号)。
A.减缓温室效应 B.减少酸雨形成 C.防止破坏臭氧层
(3)按上述方法处理2000吨废气中的二氧化硫,至少需要含5吨碳酸钙的石灰石浆。求废气中二氧化硫的质量分数。_______

(1)流程中石灰石加水制成石灰浆的目的是
(2)减少二氧化硫的排放,主要为了
A.减缓温室效应 B.减少酸雨形成 C.防止破坏臭氧层
(3)按上述方法处理2000吨废气中的二氧化硫,至少需要含5吨碳酸钙的石灰石浆。求废气中二氧化硫的质量分数。
您最近一年使用:0次



