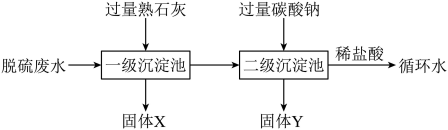
燃煤电厂产生的脱硫废水(含有CaCl2、MgCl2、MgSO4等物质)软化的一种工艺流程如下: 2CaSO4+2CO2 。R的化学式为
2CaSO4+2CO2 。R的化学式为_________ 。
(2)“沉淀”步骤需要不断搅拌,目的是______ 。
(3)写出“一级沉淀”中生成氢氧化镁的化学方程式:______ (任写一个)。
(4)“二级沉淀”中固体Y的化学式为________ ;加入稀盐酸的目的是__________ 。
(5)软化处理过程中,碳酸钠和熟石灰的添加顺序不能颠倒,原因是_______ 。
 2CaSO4+2CO2 。R的化学式为
2CaSO4+2CO2 。R的化学式为(2)“沉淀”步骤需要不断搅拌,目的是
(3)写出“一级沉淀”中生成氢氧化镁的化学方程式:
(4)“二级沉淀”中固体Y的化学式为
(5)软化处理过程中,碳酸钠和熟石灰的添加顺序不能颠倒,原因是
2022九年级下·江苏苏州·竞赛 查看更多[11]
(已下线)信息必刷卷05(无锡专用)-2024年中考化学考前信息必刷卷(已下线)专题10? 工业流程题(六大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)(已下线)2024年中考风向标-江苏-流程题山东省烟台市栖霞市2022-2023学年九年级下学期期中化学试题江苏省连云港市海州区新海初级中学2022-2023学年九年级下学期四月月考化学试题(已下线)专题09 流程图-2023年中考化学重点题型精准提分专练(全国通用)2023年江苏省镇江市部分学校3月月考化学试题(已下线)专题17 化学工艺流程题- 决胜2023年中考化学一轮地毯式复习(全国通用)(已下线)2023年中考风向标-江苏-流程题江苏省无锡市2022年中考化学真题2022年江苏省苏州市吴江区梅堰中学中、青年教师学科素养竞赛化学试题
更新时间:2022-09-20 15:21:29
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
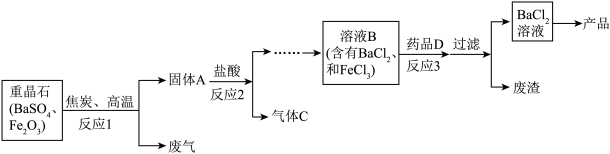
【推荐1】氯化钡广泛应用于化工领域。工业上以重晶石(主要成分BaSO4,杂质为Fe2O3)为原料,通过下列流程制备氯化钡晶体(BaCl2·2H2O)。
【查阅资料】
(1)反应1中焦炭与Fe2O3发生反应的化学方程式为________ ,体现了焦炭的________ 性。
(2)反应2中发生了多种化学反应,是因为固体A是混合物。
①硫化钡(BaS)与盐酸发生复分解反应,产生硫化氢气体(H2S),该反应的化学方程式为________ 。
②该反应过程要注意通风并远离明火,原因是气体C含有H2S、少量挥发出的HCl和水蒸气外,还含有________ 。(填化学式)
(3)反应3中药品D可选择Ba(OH)2不宜选用NaOH的原因是________ 。
(4)实验室中过滤过程要用到的玻璃仪器有烧杯、玻璃棒和________ 。
(5)上述生产过程中还要对“废气、废渣等”及时处理,否则会造成环境污染。下列做法符合“青山绿水就是金山银山”重要理念的是________。(可多选)

【查阅资料】

(1)反应1中焦炭与Fe2O3发生反应的化学方程式为
(2)反应2中发生了多种化学反应,是因为固体A是混合物。
①硫化钡(BaS)与盐酸发生复分解反应,产生硫化氢气体(H2S),该反应的化学方程式为
②该反应过程要注意通风并远离明火,原因是气体C含有H2S、少量挥发出的HCl和水蒸气外,还含有
(3)反应3中药品D可选择Ba(OH)2不宜选用NaOH的原因是
(4)实验室中过滤过程要用到的玻璃仪器有烧杯、玻璃棒和
(5)上述生产过程中还要对“废气、废渣等”及时处理,否则会造成环境污染。下列做法符合“青山绿水就是金山银山”重要理念的是________。(可多选)
| A.使用清洁能源,积极植树、造林 |
| B.对污染物处理使之符合排放标准后排放 |
| C.应用新技术、新工艺减少污染物的产生 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐2】在实验室中通常用氯酸钾和二氧化锰的混合物来制取氧气。在工业上,通过如下转化可制得KClO3晶体: 。
。
(1)完善过程Ⅰ中反应的化学方程式:NaCl+3H2O NaClO3 +3
NaClO3 +3_______ 。
(2)操作Ⅱ的名称为________ ,该反应过程能析出KClO3晶体而无其他晶体析出的原因是___________________ 。
(3)滤液中所含的溶质有_______________________ (少填或多填均不得分)。
 。
。(1)完善过程Ⅰ中反应的化学方程式:NaCl+3H2O
 NaClO3 +3
NaClO3 +3(2)操作Ⅱ的名称为
(3)滤液中所含的溶质有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】金属材料对人类的生产和生活起着重要的作用。请回答下列有关问题:
(1)合金具有许多特殊的性能,合金的硬度一般比各成分的金属的硬度___________ 。
(2)用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的原理是____________ (用化学方程式表示)。
(3)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、熟石灰加水配制面成。不能用铁桶配制波尔多液的原因是___________ 。
(4)铁生锈的现象随处可见。防止铁生锈的措施有___________ 。(写出一条即)
(5)用冰铜(主要成分为FeS和Cu2S)为原料制备CuSO4的主要工艺流程如下:

①冰铜属于___________ (填“纯净物”或“混合物”)。
②侧吹炉中发生反应: ,该反应所属的基本反应是
,该反应所属的基本反应是___________ ;SO2中S的化合价为___________ 。
③请补全酸浸槽中反应的化学方程式:
___________ 。
④酸浸槽中,搅拌的目的是___________ 。
(1)合金具有许多特殊的性能,合金的硬度一般比各成分的金属的硬度
(2)用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的原理是
(3)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、熟石灰加水配制面成。不能用铁桶配制波尔多液的原因是
(4)铁生锈的现象随处可见。防止铁生锈的措施有
(5)用冰铜(主要成分为FeS和Cu2S)为原料制备CuSO4的主要工艺流程如下:

①冰铜属于
②侧吹炉中发生反应:
 ,该反应所属的基本反应是
,该反应所属的基本反应是③请补全酸浸槽中反应的化学方程式:

④酸浸槽中,搅拌的目的是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E是初中化学常见的五种不同类别的物质。D和F的组成元素相同,A俗称纯碱,G可用于医疗急救。它们之间的反应关系如图所示: (“一”表示物质之间可以反应,“→”表示能生成:反应条件、部分反应物和生成物已省略)。
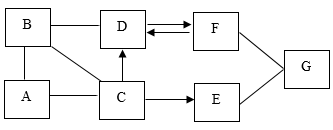
(1)写出A的化学式___________ 。
(2)写出物质D的一种用途_________ 。
(3)写出A与B反应的化学方程式____________ 。如图没有涉及到的基本反应类型是________ 。

(1)写出A的化学式
(2)写出物质D的一种用途
(3)写出A与B反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】铁黄(FeOOH)是重要的化工产品。实验室以废铁皮为原料制备铁黄的流程如图:
废铁皮→铁皮处理→制取氧气→制备铁黄→FeOOH
已知:①铁黄制备原理:4FeSO4+O2+6H2O 4FeOOH+4H2SO4。
4FeOOH+4H2SO4。
②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)铁皮处理:取一定量废铁皮,剪碎后用稀硫酸除去铁锈。该除锈反应的化学方程式为______ 。
(2)制取氧气:用KMnO4制O2。可从图1中选择装置______ (填字母)作发生装置。______ 。
②为提高产品纯度,需洗涤分离出的沉淀。检验沉淀表面附着的阴离子已洗净的方法是:取少量最后一次洗涤液于试管中,加入______ ,若无明显现象,则表明沉淀已洗净。
③实验中仅滴加少量FeSO4溶液,就能得到大量FeOOH沉淀,其原因是______ 。
(4)FeOOH可表示为xFe2O3•yH2O,则 =
=______ 。
废铁皮→铁皮处理→制取氧气→制备铁黄→FeOOH
已知:①铁黄制备原理:4FeSO4+O2+6H2O
 4FeOOH+4H2SO4。
4FeOOH+4H2SO4。②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)铁皮处理:取一定量废铁皮,剪碎后用稀硫酸除去铁锈。该除锈反应的化学方程式为
(2)制取氧气:用KMnO4制O2。可从图1中选择装置


②为提高产品纯度,需洗涤分离出的沉淀。检验沉淀表面附着的阴离子已洗净的方法是:取少量最后一次洗涤液于试管中,加入
③实验中仅滴加少量FeSO4溶液,就能得到大量FeOOH沉淀,其原因是
(4)FeOOH可表示为xFe2O3•yH2O,则
 =
=
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】绿矾(FeSO4·7H2O)是一种重要的食品添加剂。某工厂产生的炉渣主要含有FeO和Fe2O3,还有一定量的SiO2(SiO2不溶于水、不与稀硫酸反应)。实验室以此炉渣制备绿矾的流程如下:

(1)步骤①实验时需用到的玻璃仪器是___________ 、玻璃棒和烧杯。该过程发生反应的化学方程式为:①FeO+H2SO4=FeSO4+H2O,②__________________ 。
(2)滤液A中含有的溶质有FeSO4、_______________ 。
(3)加入试剂X的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是__________ 。
②若试剂X是Fe,转化原理为Fe+ Fe2(SO4)3=3FeSO4。测得反应后溶液的pH明显增大,其原因是__________________ 。
(4)步骤③的操作是蒸发浓缩、___________ 、过滤,即得到绿矾晶体。

(1)步骤①实验时需用到的玻璃仪器是
(2)滤液A中含有的溶质有FeSO4、
(3)加入试剂X的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是
②若试剂X是Fe,转化原理为Fe+ Fe2(SO4)3=3FeSO4。测得反应后溶液的pH明显增大,其原因是
(4)步骤③的操作是蒸发浓缩、
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐1】如图是初中化学常见六种物质之间的关系图 物质是溶液的只考虑溶质
物质是溶液的只考虑溶质 。图中用“
。图中用“ ”表示两种物质之间能发生化学反应,用“
”表示两种物质之间能发生化学反应,用“ ”表示一种物质可以转化为另一种物质
”表示一种物质可以转化为另一种物质 部分反应物或生成物及反应条件已略去
部分反应物或生成物及反应条件已略去 。
。

A常用于改良酸性土壤,B、C中不含相同元素,C、D中所含元素种类相同。
 请分别写出A、C物质的化学式:A.
请分别写出A、C物质的化学式:A.______ ;C.______ 。
 写出转化
写出转化 的化学方程式
的化学方程式______ 。
 写出转化
写出转化 的化学方程式
的化学方程式______ 。
 物质是溶液的只考虑溶质
物质是溶液的只考虑溶质 。图中用“
。图中用“ ”表示两种物质之间能发生化学反应,用“
”表示两种物质之间能发生化学反应,用“ ”表示一种物质可以转化为另一种物质
”表示一种物质可以转化为另一种物质 部分反应物或生成物及反应条件已略去
部分反应物或生成物及反应条件已略去 。
。
A常用于改良酸性土壤,B、C中不含相同元素,C、D中所含元素种类相同。
 请分别写出A、C物质的化学式:A.
请分别写出A、C物质的化学式:A. 写出转化
写出转化 的化学方程式
的化学方程式 写出转化
写出转化 的化学方程式
的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】如图所示,A−I是初中化学常见的物质,分别由C. H、O、S、Cl、Na、Ca、Fe中的一种或几种元素组成。A由一种元素组成,B. D. G、H、I均由两种元素组成,C. E. F均由三种元素组成。B中两种元素的质量比为7:3,B是红棕色固体,I中两种元素的原子个数比为1:4,固态G俗称“干冰”。图中“−”表示两物质间能反应,“→”表示两物质间的转化关系;反应条件已略去。______ 。
(2)A与C反应的基本反应类型是_____ 。
(3)C→D的化学方程式为______ 。
(4)E→F的化学方程式为______ 。

(2)A与C反应的基本反应类型是
(3)C→D的化学方程式为
(4)E→F的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】如图所示:已知A、B、C、D、E均为常见的物质,且A是一种最常用的溶剂,C可改良酸性土壤,B、C、D、E属于不同种类物质且含有相同的一种元素,图中“—”表示相连的物质在一定条件下可以反应,“→”表示物质间存在转化关系。请回答下列问题。

(1)D的化学式为__________ ,A→C反应的基本反应类型为__________ 。
(2)B与C反应的化学方程式为__________ 。
(3)C、E反应可用于制取烧碱,请写出该反应的化学方程式:__________ 。

(1)D的化学式为
(2)B与C反应的化学方程式为
(3)C、E反应可用于制取烧碱,请写出该反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:

(1)为了验证性质①,李华将紫色石蕊试液滴加到稀盐酸中,溶液变成_______ 色。
(2)李华将一枚生锈的铁钉放入足量的稀盐酸中,他首先观察到的现象是_____ ,过一会儿,他又观察到_____ 。发生以上反应现象的化学方程式分别为_______ 、_______ 。李华的这个实验体现了性质_______ (填序号,下同),其中性质_______ 在工业上可用于除铁锈。
(3)假设编号③反应的盐是AgNO3,则编号③对应的化学方程式是_______ 。
(4)物质组成和结构决定其性质。从微观进入宏观,探索物质变化规律。
例如:稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,写出化学方程式:_____ 。体现了不同的酸也具有各自的特性,原因是_______ 。
(5)通过分析组成和结构,可以预测物质的某些性质。根据如图硫酸氢钠溶液的微观图示,分析推断NaHSO4的性质,其中正确的是


(1)为了验证性质①,李华将紫色石蕊试液滴加到稀盐酸中,溶液变成
(2)李华将一枚生锈的铁钉放入足量的稀盐酸中,他首先观察到的现象是
(3)假设编号③反应的盐是AgNO3,则编号③对应的化学方程式是
(4)物质组成和结构决定其性质。从微观进入宏观,探索物质变化规律。
例如:稀盐酸不能与氯化钡溶液反应,而稀硫酸则能与之反应生成白色沉淀,写出化学方程式:
(5)通过分析组成和结构,可以预测物质的某些性质。根据如图硫酸氢钠溶液的微观图示,分析推断NaHSO4的性质,其中正确的是

| A.其水溶液能使紫色石蕊试液变蓝 |
| B.其水溶液能与金属镁粉反应 |
| C.其水溶液能与碳酸钠反应 |
| D.其水溶液能与硝酸钡溶液反应 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】向盛有稀盐酸和氯化钡的混合溶液的烧杯中逐滴加入碳酸钠溶液,直至过量,根据实验绘制如图所示的曲线,下列说法中正确的是 _

A a至b段有气泡产生
B d点溶质种类为三种
C b至c段,烧杯中水的质量不变
D c点所含的溶质为____________

A a至b段有气泡产生
B d点溶质种类为三种
C b至c段,烧杯中水的质量不变
D c点所含的溶质为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
【推荐3】(1)如图1是a、b、c三种物质的溶解度曲线,回答下列问题:

①t2℃时,a、b、c三种物质的溶解度由大到小的顺序为_______________ .
②P点的含义是_____________________ .
③t2℃时,将40ga物质加入50g水中,充分溶解后得到溶液的质量为_____ g.
④将a、b、c三种物质的饱和溶液从t2℃降温到t1℃时,溶液中溶质的质量分数不变的是______ .
(2)A﹣G是初中化学常见物质,A、C在常温下是气体且元素组成相同,B是铁锈的主要成分,E的相对分子质量为100,它们的相互转化关系如图2(部分反应物、生成物及反应条件已略去),请回答下列问题:

①写出物质E的化学式_____________ .
②写出有关反应的化学方程式:
(Ⅰ)A+B→_____________________ ;
(Ⅱ)G+Na2CO3溶液→__________________________ .
③写出F的一种用途_______________ .

①t2℃时,a、b、c三种物质的溶解度由大到小的顺序为
②P点的含义是
③t2℃时,将40ga物质加入50g水中,充分溶解后得到溶液的质量为
④将a、b、c三种物质的饱和溶液从t2℃降温到t1℃时,溶液中溶质的质量分数不变的是
(2)A﹣G是初中化学常见物质,A、C在常温下是气体且元素组成相同,B是铁锈的主要成分,E的相对分子质量为100,它们的相互转化关系如图2(部分反应物、生成物及反应条件已略去),请回答下列问题:

①写出物质E的化学式
②写出有关反应的化学方程式:
(Ⅰ)A+B→
(Ⅱ)G+Na2CO3溶液→
③写出F的一种用途
您最近一年使用:0次



