为测定金属镁和硫酸镁的固体混合物中镁元素的质量分数,先称取混合物10g,放入一个干净的烧杯中,然后取一定溶质质量分数的稀硫酸75g,平均分成五次加入其中,充分振荡,实验所得数据见表:
(1)表中x=___________ 。
(2)金属镁完全反应是第___________ 次。
(3)求固体混合物中镁元素的质量分数(写出计算过程,结果精确到0.1%)。
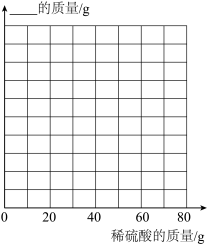
(4)已知图中纵坐标为某单质,请画出该单质的质量随加入稀硫酸质量的变化图像(标出必要的数据)。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀硫酸的质量/g | 15 | 15 | 15 | 15 | 15 |
| 生成氢气的总质量/g | 0.12 | x | 0.36 | 0.4 | 0.4 |

(1)表中x=
(2)金属镁完全反应是第
(3)求固体混合物中镁元素的质量分数(写出计算过程,结果精确到0.1%)。
(4)已知图中纵坐标为某单质,请画出该单质的质量随加入稀硫酸质量的变化图像(标出必要的数据)。
更新时间:2022-10-04 23:15:18
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐1】纯碱可用于造纸、玻璃生产等领域。纯碱产品中常含有少量的氯化钠杂质,某兴趣小组的同学为测定某品牌纯碱样品中碳酸钠的质量分数,设计了下图方案并进行实验。

(1)滤液B中含有的阳离子有_____________ (填化学符号)。
(2)若沉淀不经过操作b会使测定结果_____________ (填“偏大”、“偏小”或“无影响”)。
(3)根据以上数据计算该样品中碳酸钠的质量分数(写出计算过程,结果精确至0.1%)。

(1)滤液B中含有的阳离子有
(2)若沉淀不经过操作b会使测定结果
(3)根据以上数据计算该样品中碳酸钠的质量分数(写出计算过程,结果精确至0.1%)。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐2】实验室以某石灰石(含少量Fe2O3)为原料制备高纯CaCO3的步骤如下。
溶解:向石灰石样品中加入适量盐酸,至反应完全。
除铁:加入氨水调节pH,然后加入适量Ca(OH)2,充分反应后过滤。
沉淀:向滤液中补充氨水,通入CO2,反应一段时间。
分离:过滤、洗涤、干燥得高纯CaCO3。
(1)溶解时,CaCO3、Fe2O3分别与盐酸反应的化学方程式为_____ 、_____ 。判断样品已完全反应的实验现象是_____ 。
(2)除铁时,选用Ca(OH)2而不选用NaOH,其主要原因是Ca(OH)2价格低且来源广、_____ 、_____ ;过滤所得滤渣的主要成分为_____ 。
(3)沉淀时,其他条件相同,反应温度对CaCO3产率的影响如图。高于35℃时,CaCO3产率下降的主要原因是_____ 、_____ 。(已知: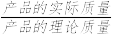 ×100%)
×100%)
(4)分离时,若向过滤所得滤液中加入_____ (填化学式)并加热,则可回收NH3。
(5)该实验中可以循环利用的物质有H2O和_____ 。
(6)石灰厂煅烧石灰石生产CaO,若要得到28t CaO,则至少需要含CaCO3 90%的石灰石____ 吨。(写出计算过程,保留一位小数。)

溶解:向石灰石样品中加入适量盐酸,至反应完全。
除铁:加入氨水调节pH,然后加入适量Ca(OH)2,充分反应后过滤。
沉淀:向滤液中补充氨水,通入CO2,反应一段时间。
分离:过滤、洗涤、干燥得高纯CaCO3。
(1)溶解时,CaCO3、Fe2O3分别与盐酸反应的化学方程式为
(2)除铁时,选用Ca(OH)2而不选用NaOH,其主要原因是Ca(OH)2价格低且来源广、
(3)沉淀时,其他条件相同,反应温度对CaCO3产率的影响如图。高于35℃时,CaCO3产率下降的主要原因是
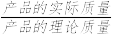 ×100%)
×100%)(4)分离时,若向过滤所得滤液中加入
(5)该实验中可以循环利用的物质有H2O和
(6)石灰厂煅烧石灰石生产CaO,若要得到28t CaO,则至少需要含CaCO3 90%的石灰石

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】某同学在实验室以石灰石(杂质不反应也不溶于水)为原料制取轻质碳酸钙和氢氧化钠。

(1)操作a的名称是_____ 。
(2)该流程中有两个反应,产物中均出现碳酸钙,这两个反应的化学方程式分别为:_____ 、_____ 。
(3)为了验证加入Na2CO3溶液后,溶液A中的溶质是否反应完全,可取过滤3的滤液加入_____ (填字母)进行检验。
A碳酸钠溶液 B铁粉 C无色酚酞 D足量盐酸
(4)工业上高温煅烧石灰石生产生石灰,若要生产含氧化钙5.6t的生石灰,需要含碳酸钙80%的石灰石的质量是多少?_____ (根据化学方程式计算,写出计算过程)

(1)操作a的名称是
(2)该流程中有两个反应,产物中均出现碳酸钙,这两个反应的化学方程式分别为:
(3)为了验证加入Na2CO3溶液后,溶液A中的溶质是否反应完全,可取过滤3的滤液加入
A碳酸钠溶液 B铁粉 C无色酚酞 D足量盐酸
(4)工业上高温煅烧石灰石生产生石灰,若要生产含氧化钙5.6t的生石灰,需要含碳酸钙80%的石灰石的质量是多少?
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
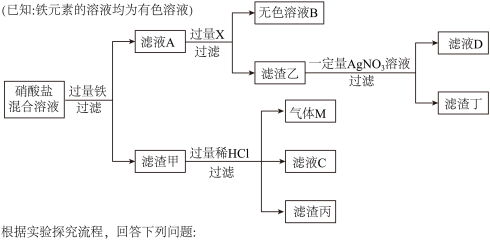
【推荐1】对金属材料的研究,在人类发展的历史长河中起着非常重要的作用。某研究小组对合成铜银元素新型复合材料的剩余溶液进行探究。已知该剩余溶液是含Cu(NO3)2、AgNO3、X(NO3)2的硝酸盐混合溶液,流程如下(X表示一种金属元素):______ (书写一个即可)。
(2)气体M的化学式为______ 。
(3)比较金属Fe、Cu、Ag、X的活动性,金属活动性最强的是______ 。
(4)滤液D中所含溶质的成分中一定含______(填选项)。
(5)将上述滤渣洗涤烘干后,可能得到纯净物的是滤渣______ (填“甲”、“乙”、“丙”或“丁”)。若想通过其他滤渣得到更多的该纯净物,请写出具体的实验步骤______ 。
(2)气体M的化学式为
(3)比较金属Fe、Cu、Ag、X的活动性,金属活动性最强的是
(4)滤液D中所含溶质的成分中一定含______(填选项)。
| A.Cu(NO3)2 | B.AgNO3 | C.X(NO3)2 | D.Fe(NO3)2 |
(5)将上述滤渣洗涤烘干后,可能得到纯净物的是滤渣
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】在实验课中,各小组作了如下实验。
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜。经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶液相同。
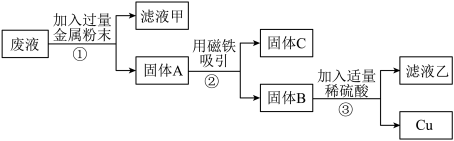
操作③的名称是_____ 实验中所加的过量金属粉末是_____ ,则固体C是_____ 。
| 实验编号 | 1 | 2 | 3 | 4 |
| 实验操作 | 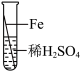 | 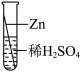 | 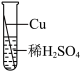 |  |

操作③的名称是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】工业上用FeCl3溶液蚀刻铜箔(Cu)制造印刷电路板,产生的蚀刻废液可以再处理,实现资源回收利用。下图是某兴趣小组设计的蚀刻废液处理流程图,已知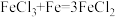 。请回答下列问题。
。请回答下列问题。

(1)步骤所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此判断步骤I中铜与FeCl3反应生成的两种产物是___________ (写化学式,下同)。
(2)固体A的成分为___________ 。
(3)步骤Ⅲ中加入适量稀盐酸的作用是___________ 。
(4)该流程中可以循环使用的物质是___________ 。
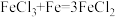 。请回答下列问题。
。请回答下列问题。
(1)步骤所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此判断步骤I中铜与FeCl3反应生成的两种产物是
(2)固体A的成分为
(3)步骤Ⅲ中加入适量稀盐酸的作用是
(4)该流程中可以循环使用的物质是
您最近一年使用:0次



