N(NO2)3是科学家2011年发现的一种新型火箭燃料。计算:
(1)N(NO2)3中氮原子和氧原子的个数比为______ (填最简比);
(2)N(NO2)3中氮元素和氧元素的质量比为______
(3)N(NO2)3的相对分子质量是______ ;
(4)下列化合物中,氮元素质量分数最小的是______(填字母)。
(1)N(NO2)3中氮原子和氧原子的个数比为
(2)N(NO2)3中氮元素和氧元素的质量比为
(3)N(NO2)3的相对分子质量是
(4)下列化合物中,氮元素质量分数最小的是______(填字母)。
| A.N(NO2)3 | B.N2O3 | C.N2O5 |
更新时间:2022-12-10 21:31:50
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】化学为航空、航天领域的发展提供了强有力的支撑,。
(1)“天宫课堂”中,航天员在水球光学实验中打入的“人造空气”与我们身边的空气成分含量基本相同,其中体积分数最大的是______ (写化学符号)。
(2)航天员用泡腾片演示了实验,泡腾片中含有维生素C(C6H8O6),下列说法正确的是______。
(3)北斗卫星导航系统(以下简称北斗系统)是我国自主建设运行的全球卫星导航系统,为服务全球、造福人类贡献了中国智慧和力量。
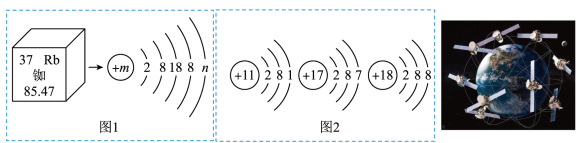
①北斗系统采用物原子钟提供精确时间,铷元素在元素周期表中的相关信息与铷原子的结构示意图如图1所示,铷的相对原子质量为______ 。
②图1中n=______ ,图2中与铷元素化学性质相似的元素是______ (填元素符号)。
③铷元素位于元素周期表的第______ 周期,属于______ 元素(选填“金属”或“非金属”)。
④铷原子在化学反应中容易______ (选填“失去”或“得到)电子,铷离子的符号为______ 。
(1)“天宫课堂”中,航天员在水球光学实验中打入的“人造空气”与我们身边的空气成分含量基本相同,其中体积分数最大的是
(2)航天员用泡腾片演示了实验,泡腾片中含有维生素C(C6H8O6),下列说法正确的是______。
| A.维生素C由6个碳原子、8个氢原子、6个氧原子构成 |
| B.维生素C由C、H、O三种元素组成 |
| C.维生素C中含有氧分子 |
(3)北斗卫星导航系统(以下简称北斗系统)是我国自主建设运行的全球卫星导航系统,为服务全球、造福人类贡献了中国智慧和力量。

①北斗系统采用物原子钟提供精确时间,铷元素在元素周期表中的相关信息与铷原子的结构示意图如图1所示,铷的相对原子质量为
②图1中n=
③铷元素位于元素周期表的第
④铷原子在化学反应中容易
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】在宏观、微观、符号、结构之间建立联系是化学特有的思维方式。回答下列有关溶液的问题:
(1)下列符号既能表示一种物质,又能表示一个原子的是______(填序号)。
(2)从宏观上观察:如图所示,试管a和b中产生气体的体积比约为_______ ,b中产生的气体是_______ (填化学式)
(4)从符号上表示:电解水的化学反应方程式为_______ ,反应的基本类型为_______ 。
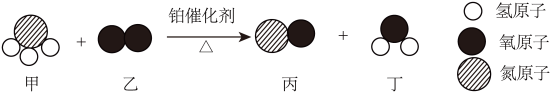
(5)模型认知是化学研究的重要科学方法。如图是工业制取硝酸第一步反应的微观示意图。
生成的丙、丁的分子个数比是_______ 。
(1)下列符号既能表示一种物质,又能表示一个原子的是______(填序号)。
A. | B. | C.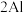 | D.N |
(2)从宏观上观察:如图所示,试管a和b中产生气体的体积比约为

| A.水是由氢气和氧气组成的 |
| B.水是由氢原子和氧原子构成的 |
| C.每个水分子是由2个氢原子和1个氧原子构成的 |
(4)从符号上表示:电解水的化学反应方程式为
(5)模型认知是化学研究的重要科学方法。如图是工业制取硝酸第一步反应的微观示意图。
生成的丙、丁的分子个数比是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】请根据所学化学知识填写下列空白:
(1)多步行,骑单车出行,能有效减少CO2、SO2、CO等气体的排放,这些气体中能引起温室效应的是___________ ,会造成酸雨的是SO2。
(2)氢气在空气中燃烧时,产生淡蓝色火焰,该反应的化学方程式是___________ 。混有一定量空气或氧气的氢气遇明火可能会发生爆炸,因此点燃氢气前一定要进行验纯。
(3)奥司他韦(化学式为:C16H28N2O4)是一种治疗流行性感冒的药物,它的一个分子中共含有50个原子,其中氢、氧元素的个数比为___________ 。
(1)多步行,骑单车出行,能有效减少CO2、SO2、CO等气体的排放,这些气体中能引起温室效应的是
(2)氢气在空气中燃烧时,产生淡蓝色火焰,该反应的化学方程式是
(3)奥司他韦(化学式为:C16H28N2O4)是一种治疗流行性感冒的药物,它的一个分子中共含有50个原子,其中氢、氧元素的个数比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】农作物秸秆属于农业生态系统中一种十分宝贵的生物质能资源。农作物秸秆综合利用对于促进农民增收、环境保护、资源节约以及农业经济可持续发展意义重大。秸秆的主要成分是纤维素【(C6H10O5)n】。
(1)纤维素分子的相对分子质量为_________ 。
(2)发电厂将秸秆粉碎压缩成颗粒,作为燃料用于发电。其主要成分充分燃烧反应生成的物质有________ 。(答案用化学式表示)
(3)根据《大气污染防治法》相关规定,为保护环境,我县辑庆、兴隆、龙台、永安等各乡镇严厉整治农田露天焚烧秸秆事件,农田露天荧烧秸秆主要危害是________。
(4)利用秸秆可生产乙醇,加入到汽油中制成乙醇汽油,可缓解能源危机。生产过程中涉及到如下两个化学反应,则X的化学式为_________ 。
 ;
;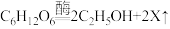
(5)在农村,秸秆曾经作为燃料广泛使用,但是有很多缺点。随着社会的进步,农村可以推广使用下列哪些能源替代秸秆作燃料________(填写正确的选项字母)。
(6)沼气、天然气、可燃冰的主要成分是甲烷,据央视2021年8月新闻报道,已探明四川中江天然气储量达1061亿立方米,彰显出中江的资源优势。根据所学知识写出甲烷完全燃烧的反应方程式:_________ 。
(1)纤维素分子的相对分子质量为
(2)发电厂将秸秆粉碎压缩成颗粒,作为燃料用于发电。其主要成分充分燃烧反应生成的物质有
(3)根据《大气污染防治法》相关规定,为保护环境,我县辑庆、兴隆、龙台、永安等各乡镇严厉整治农田露天焚烧秸秆事件,农田露天荧烧秸秆主要危害是________。
| A.焚烧过程中燃烧不充分,产生的浓烟使空气中可吸入颗粒物增多,造成空气能见度降低,将影响民航、高速公路运行安全 |
| B.焚烧过程中燃烧不充分,产生大量的一氧化碳,污染环境 |
| C.破坏土壤结构,影响土壤生态系统平衡,造成农田质量下降 |
| D.焚烧秸秆,容易“火烧连营”,引发火灾 |
 ;
;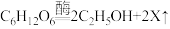
(5)在农村,秸秆曾经作为燃料广泛使用,但是有很多缺点。随着社会的进步,农村可以推广使用下列哪些能源替代秸秆作燃料________(填写正确的选项字母)。
| A.沼气 | B.天然气(或液化气) | C.太阳能 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】2019年3月13日,“玉兔二号”巡视器已完成三个月昼工作,于12时16分进入第三个月夜,累计行走163米,再一次创造奇迹。将“玉兔二号”运往月球的长征三号乙运载火箭的一、二子级推进剂都是偏二甲肼(C2H8N2)和四氧化二氮(N2O4)。请根据相关信息,回答下列问题:
①N2O4属于_____________ (选填“单质”、“氧化物”中的一种)。
②偏二甲肼中,碳元素和氢元素的质量之比为___________ (最简整数比)。
③偏二甲肼的相对分子质量是_______________ 。
①N2O4属于
②偏二甲肼中,碳元素和氢元素的质量之比为
③偏二甲肼的相对分子质量是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐3】莽草酸(化学式:C7H10O5)是制取抗“H1N1流感”药物“达菲”的原料。
请回答:
(1)莽草酸分子中C、H、O原子个数比为____________ 。
(2)174g莽草酸含氢元素质量为__________ g。
(3)对1岁以上的儿童推荐按照下列“体重—剂量表”服用“达菲”:
假如患病儿童的体重是35千克,在治疗过程中,需每天服用“达菲”胶囊(每颗胶囊含“达菲”75mg)2次,一个疗程5天,那么该患儿一个疗程共需服用__________ 颗。
请回答:
(1)莽草酸分子中C、H、O原子个数比为
(2)174g莽草酸含氢元素质量为
(3)对1岁以上的儿童推荐按照下列“体重—剂量表”服用“达菲”:
| 体重 | 小于等于15千克 | 15~23千克 | 23~40千克 | 大于40千克 |
| 每次用量 | 30mg | 45mg | 60mg | 60mg |
假如患病儿童的体重是35千克,在治疗过程中,需每天服用“达菲”胶囊(每颗胶囊含“达菲”75mg)2次,一个疗程5天,那么该患儿一个疗程共需服用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阿兹夫定(化学式为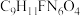 )是我国具有知识产权的口服小分子新冠病毒治疗药物,在抗击新冠病毒中发挥了重要作用。
)是我国具有知识产权的口服小分子新冠病毒治疗药物,在抗击新冠病毒中发挥了重要作用。
(1)阿兹夫定由_______ 种元素组成。
(2)阿兹夫定组成元素中,原子序数最大的是_______ 。
(3)在阿兹夫定中氮、氧元素的质量比为_______ 。
(4)由碳、氢元素组成的最简单的化合物的化学式是_______ 。
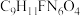 )是我国具有知识产权的口服小分子新冠病毒治疗药物,在抗击新冠病毒中发挥了重要作用。
)是我国具有知识产权的口服小分子新冠病毒治疗药物,在抗击新冠病毒中发挥了重要作用。(1)阿兹夫定由
(2)阿兹夫定组成元素中,原子序数最大的是
(3)在阿兹夫定中氮、氧元素的质量比为
(4)由碳、氢元素组成的最简单的化合物的化学式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】实验室可以用5%的过氧化氢溶液制取氧气。
(1)H2O2属于__________ (填“纯净物”或“混合物”)。
(2)H2O2中氢元素与氧元素的质量比为__________ ,其相对分子质量为__________ 。
(3)分解过氧化氢制氧气的反应中二氧化锰起__________ 作用,反应的符号表达式为__________ 。
(1)H2O2属于
(2)H2O2中氢元素与氧元素的质量比为
(3)分解过氧化氢制氧气的反应中二氧化锰起
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】空气是宝贵的自然资源,其组成如表
如图是空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去),请按要求回答相关问题:
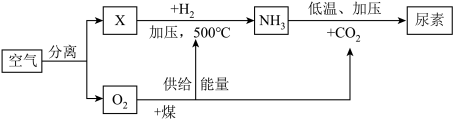
(1)X、Y气体名称分别是______ 、______ 。
(2)分离空气的常用方法有以下两种。
Ⅰ、将液态空气气化,首先分离出氮气,则沸点:X______ Y (选填"高于"、“等于”、“低于")。
Ⅱ、分子筛分离。分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:X______ O2(选填"大于"、“等于"、“小于")。
(3)结合流程和所学知识可以预测:化学反应中发生物质变化的同时一定还伴随有______ 变化。(选填"状态"、“能量”、"原子"、“压强")
(4)相同条件下气体体积之比等于分子之比,则空气中氮分子与氧分子总质量之比等于______ 。
| 空气组成 | X | O2 | Y | CO2 | 其它 |
| 体积分数 | 78% | 21% | 0.934% | 0.034% | 0.002% |

(1)X、Y气体名称分别是
(2)分离空气的常用方法有以下两种。
Ⅰ、将液态空气气化,首先分离出氮气,则沸点:X
Ⅱ、分子筛分离。分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:X
(3)结合流程和所学知识可以预测:化学反应中发生物质变化的同时一定还伴随有
(4)相同条件下气体体积之比等于分子之比,则空气中氮分子与氧分子总质量之比等于
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。
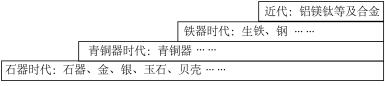
(1)金、银在自然界有单质形式存在,说明它们的化学性质都______ 。
(2)在生产生活实践中人类逐渐掌握了多种金属的技术。
①比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分:FeCO3),从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是______ 。
②近代工业上采用电解熔融氧化铝(Al2O3)的方法冶炼铝,Al2O3分解后得到两种单质,该反应的化学方程式为______ 。
(3)镁铝合金被誉为“21世纪绿色金属结构材料”,一种镁铝合金Mg17Al12是特殊的储氢材料,完全吸收氢气后得到MgH2和Al,该反应的化学方程式为______ 。
(4)钛和钛合金是21世纪的重要的金属材料,钛合金制品放在海水中数年取出后人光亮如新,是因为其______(填序号)非常好。
(5)铁在潮湿的空气中反应生成疏松的铁锈,已知:2FeCl3+Fe=3FeCl2;请问铁锈的主要成分是______ (填化学式):将生锈的铁制品放入一定量的稀盐酸中充分反应,变化过程中最多涉及______ 种化学反应基本类型。

(1)金、银在自然界有单质形式存在,说明它们的化学性质都
(2)在生产生活实践中人类逐渐掌握了多种金属的技术。
①比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分:FeCO3),从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是
②近代工业上采用电解熔融氧化铝(Al2O3)的方法冶炼铝,Al2O3分解后得到两种单质,该反应的化学方程式为
(3)镁铝合金被誉为“21世纪绿色金属结构材料”,一种镁铝合金Mg17Al12是特殊的储氢材料,完全吸收氢气后得到MgH2和Al,该反应的化学方程式为
(4)钛和钛合金是21世纪的重要的金属材料,钛合金制品放在海水中数年取出后人光亮如新,是因为其______(填序号)非常好。
| A.可塑性 | B.机械性能 | C.抗腐蚀性能 |
(5)铁在潮湿的空气中反应生成疏松的铁锈,已知:2FeCl3+Fe=3FeCl2;请问铁锈的主要成分是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】密闭容器中盛有22g丙烷(C3H8)和一定质量的氧气,点燃使其充分反应,丙烷全部转化为CO、CO2和H2O,待恢复至室温,测得容器内混合气体中氧元素的质量分数为64%。则参加反应的氧气的质量为:_______ ;该反应的化学方程式为_______ 。
您最近一年使用:0次
【推荐3】“价类二维图”(元素的化合价和物质类别的二维图)是学习化学的亠种重要方法。下图为硫元素的“价类二维图”回答下列问题:
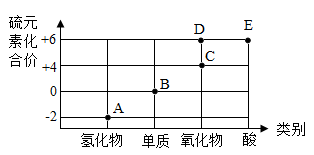
(1)已知:由两种元素组成的化合物中,其中一种元素是氢元素的叫做氢化物。则A点对位物质的化学式为___________ 。
(2)B点对应物质的颜色为___________ 。大量排放C点对应物质导致的危害有___________ (任写一条)。
(3)D点对应物质中氧元素的质量分数为___________ 。
(4) A、C两点对应的物质在常温下反应生成两种产物,其中一种为B点对应物质,另一种物质为常见液态氧化物。则该反应的符号表达式为___________ 。

(1)已知:由两种元素组成的化合物中,其中一种元素是氢元素的叫做氢化物。则A点对位物质的化学式为
(2)B点对应物质的颜色为
(3)D点对应物质中氧元素的质量分数为
(4) A、C两点对应的物质在常温下反应生成两种产物,其中一种为B点对应物质,另一种物质为常见液态氧化物。则该反应的符号表达式为
您最近一年使用:0次



