同学们从山上采集到一种石灰石样品。为了测定石灰石样品中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应),取四份样品分别加稀盐酸反应,其实验数据记录如下表。
请回答下列问题:
(1)分析在4份样品测得的数据,第_______ 份样品与稀盐酸恰好完全反应,生成CO2的质量为_______ g。
(2)列式计算所用的稀盐酸的溶质质量分数。
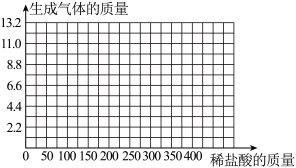
(3)请在下图中画出在40.0g石灰石样品中加稀盐酸的质量与产生气体质量变化关系的示意图____ (要标注样品与稀盐酸恰好完全反应时的坐标),
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀盐酸质量(g) | 100.0 | 200.0 | 300.0 | 400.0 |
| 产生气体质量(g) | 4.4 | 8.8 | 13.2 | 13.2 |
(1)分析在4份样品测得的数据,第
(2)列式计算所用的稀盐酸的溶质质量分数。
(3)请在下图中画出在40.0g石灰石样品中加稀盐酸的质量与产生气体质量变化关系的示意图

22-23九年级上·广东阳江·期末 查看更多[5]
广东省阳江市江城区2022-2023学年九年级上学期期末化学试题广东省阳江市2022-2023学年九年级上学期期末化学试题广东省阳江市江城区2022-2023学年九年级上学期期末化学试题(已下线)化学-2022-2023学年九年级下学期开学摸底考试卷(广东专用)(已下线)专题10 化学计算-【好题汇编】备战2023-2024学年九年级化学上学期期末真题分类汇编(广东专用)
更新时间:2022/12/22 21:30:10
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】为了测定某黄铜(铜锌合金)样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反映后用天平称量,几次试验数据如下
请回答下列问题并计算:
(1)50g样品与________g稀硫酸恰好完全反应;
(2)计算样品中锌的质量分数(写出具体计算过程)
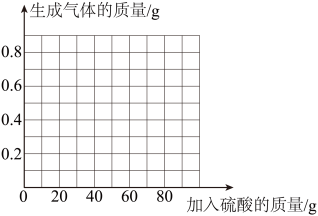
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系。
试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
生成气体的质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
(1)50g样品与________g稀硫酸恰好完全反应;
(2)计算样品中锌的质量分数(写出具体计算过程)
(3)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】向34g过氧化氢溶液中加入1g二氧化锰粉末。反应开始后产生氧气的总质量随时间的变化关系如图所示,请回答:
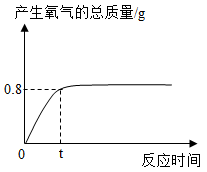
(1)从反应开始到t时,产生氧气的总质量是_________ g。
(2)请计算该过氧化氢溶液的溶质质量分数。

(1)从反应开始到t时,产生氧气的总质量是
(2)请计算该过氧化氢溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16克放入烧杯,把80克稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。
试计算:
(1)如表中n的数值为_________ ;
(2)样品中碳酸钙的质量分数为_________ (精确到0.1%)。(写出计算过程)
试计算:
| 序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸的质量/克 | 20 | 20 | 20 | 20 |
| 生成气体的质量/克 | 2.2 | n | 1.1 | 0 |
(2)样品中碳酸钙的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取15g石灰石样品研碎和100g稀盐酸放入烧杯中,两者恰好完全反应。在反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表(已知烧杯的质量为25g,样品中的杂质不溶于水、也不与稀盐酸反应)。请计算:
(1)表中的“m”为___________ g。
(2)该石灰石样品中碳酸钙的质量分数(计算结果精确至0.1%)。
| 反应时间/s | 20 | 40 | 60 | 80 | 100 |
| 烧杯和所盛药品质量/g | 137.8 | 135.6 | 134.5 | m | 134.5 |
(2)该石灰石样品中碳酸钙的质量分数(计算结果精确至0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为了节约林木资源,近几年兴起石头纸。石头纸可用沿海水产养殖中产生的大量废弃贝壳制得。为了测定某种贝壳中碳酸钙的质量分数,取贝壳15克,加入150克7.3%的盐酸溶液,充分反应后,称得剩余物质的总质量为159.72克。(假设贝壳中其它物质不与盐酸反应)有人认为,根据上述实验数据,可按如下方案计算:根据“150克7.3%的盐酸溶液”,得出参加反应的氯化氢质量,然后根据反应原理求得碳酸钙的质量,最后求出贝壳中碳酸钙的质量分数。
(1)以上方案是否正确?__________ ;理由是_______________
(2)计算贝壳中碳酸钙的质量分数。
(1)以上方案是否正确?
(2)计算贝壳中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下表所示:
回答下列问题:
(1)原固体混合物中,氧化铜的质量分数为_______ 。
(2)上表中,a的值为_____ 。
(3)计算该实验所用稀硫酸中溶质的质量分数_____ 。(写出计算过程,结果精确到0.1%)
| 次序 | ① | ② | ③ | ④ |
| 加入稀硫酸的质量/g | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 16 | a | 10 | 10 |
回答下列问题:
(1)原固体混合物中,氧化铜的质量分数为
(2)上表中,a的值为
(3)计算该实验所用稀硫酸中溶质的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】硫酸钠样品中含有少量的氯化钠,某同学为测定该样品中硫酸钠的含量,他取该样品8g,全部溶解在100g水中,再加入104g溶质质量分数为10%的氯化钡溶液,恰好完全反应,过滤,所得溶液为不饱和溶液(不考虑过程中物质质量的损失)。请计算:
(1)样品中硫酸钠的质量分数;(计算结果保留到0.1%)
(2)反应后所得溶液中溶质的质量分数(计算结果保留到0.1%)。
(1)样品中硫酸钠的质量分数;(计算结果保留到0.1%)
(2)反应后所得溶液中溶质的质量分数(计算结果保留到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某锥形瓶中盛有盐酸和氯化铜的混合溶液100g,向其中逐滴加入氢氧化钠溶液,锥形瓶内产生沉淀的质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)产生沉淀的质量为______g。
(2)计算100g混合溶液中HCl质量为多少?

(1)产生沉淀的质量为______g。
(2)计算100g混合溶液中HCl质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】第19届杭州亚运会主火炬塔燃烧的液体燃料是被称为“零碳甲醇”(化学式为CH3OH)的物质,“零碳甲醇”是利用氢气与二氧化碳合成的一种绿色能源,其生产过程如图甲所示。图乙是反应2在一定条件下,在有、无分子筛膜时,甲醇的产率随温度变化的关系。
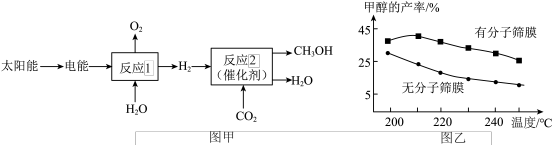
(1)由图乙可知,为提高甲醇的产窄,合成甲醇应选择的最佳条件为________ 。
(2)若要生产1000kg甲醇,可减少排放的二氧化碳气体的质量是多少________ ?(写出完整的解题过程)

(1)由图乙可知,为提高甲醇的产窄,合成甲醇应选择的最佳条件为
(2)若要生产1000kg甲醇,可减少排放的二氧化碳气体的质量是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】“化学氧自救呼吸器”是一种在缺氧环境中通过制氧剂临时供氧的装置。制氧剂的主要成分是超氧化钾(KO2),产生氧气的主要原理是超氧化钾与人体呼出的水汽反应,其化学方程式为 。制氧剂中其他成分不能生成氧气。
。制氧剂中其他成分不能生成氧气。
(1)若该呼吸器需为使用者提供48g氧气,则至少需要含超氧化钾80%的制氧剂多少克?
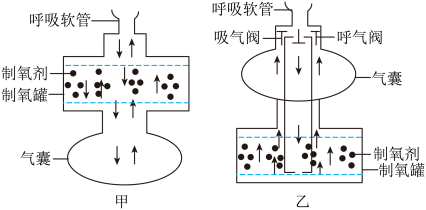
(2)小明设计了如图甲、乙两种化学氧自教呼吸器,其内部气体路径如图所示。你认为哪种方案更合理?理由是___________ 。
 。制氧剂中其他成分不能生成氧气。
。制氧剂中其他成分不能生成氧气。(1)若该呼吸器需为使用者提供48g氧气,则至少需要含超氧化钾80%的制氧剂多少克?

(2)小明设计了如图甲、乙两种化学氧自教呼吸器,其内部气体路径如图所示。你认为哪种方案更合理?理由是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】如图所示,在盛有稀盐酸的大烧杯中漂浮着一个塑料块,现向稀盐酸中逐渐加入6.5g锌粒,实验结束后观察到锌粒全部溶解。
(2)反应结束后,塑料块浸入溶液内的体积_______ (填“变大”或“变小”)。

(2)反应结束后,塑料块浸入溶液内的体积
您最近一年使用:0次